Hòa tan 2,4 g Mg trong 150ml dung dịch HCl 2M . Dung dịch thu đươc có pH bằng bao nhiêu ?
1
a) Tính pH của dung dịch sau: Trộn 100ml dung dịch Ba(OH)2 0,1M với 100ml KOH 0,1M.
b) Hòa tan 2,4 g Mg trong 150 ml dung dịch HCL 2M. Dung dịch thu được có pH bằng bao nhiêu?
a)
nBa(OH)2 = 0,1.0,1=0,01 mol
nKOH = 0,1.0,1=0,01 mol
nOH- = nBa(OH)2 .2 + nKOH = 0,01.2+0,01 =0,03 mol
P[OH]=0,82
=> pH = 14-p[OH] = 13,18
Tính C% chất tan trong dung dịch thu được trong các trường hợp sau:
a. Trộn 100 gam dung dịch HCl 10% với 150 gam dung dịch HCl 20%.
b. Hòa tan hoàn toàn 2,4 gam Mg bằng 100 gam dung dịch HCl 10,95%
\(a.m_{HCl}=100.10\%+150.20\%=40\left(g\right)\\ C\%_{ddHCl}=\dfrac{40}{100+150}.100=16\%\\ b.n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\\ n_{HCl}=\dfrac{10,95\%.100}{36,5}=0,3\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ Vì:\dfrac{0,1}{1}< \dfrac{0,3}{1}\Rightarrow HCldư\\ n_{HCl\left(dư\right)}=0,3-2.0,1=0,1\left(mol\right)\\ m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\\ n_{MgCl_2}=n_{Mg}=0,1\left(mol\right)\\ m_{MgCl_2}=0,1.95=9,5\left(g\right)\\ m_{ddsau}=2,4+100-0,1.2=102,2\left(g\right)\\ C\%_{ddHCl\left(dư\right)}=\dfrac{3,65}{102,2}.100\approx3,571\%\)
\(C\%_{ddMgCl_2}=\dfrac{9,5}{102,2}.100\approx9,295\%\)
Hòa tan 2,4 g magie bằng dung dịch HCl 2M vừa đủ thu được khí hiđro và muối clorua . Hỏi : a) Tính thể tích khí thoát ra ở đktc b) Tính thể tích dung dịch HCl 2M đã dùng
a, \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Theo PT: \(n_{H_2}=n_{Mg}=0,1\left(mol\right)\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
b, \(n_{HCl}=2n_{Mg}=0,2\left(mol\right)\Rightarrow V_{HCl}=\dfrac{0,2}{2}=0,1\left(l\right)\)
\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
PTHH :
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
0,1 0,2 0,1
\(a,V_{H_2}=0,1.22,4=2,24\left(l\right)\)
\(b,V=\dfrac{n}{C_M}=\dfrac{0,2}{2}=0,1\left(l\right)\)
hòa tan hoàn toàn 20 g hỗn hợp rắn X gồm Mg và Fe trong gam dung dịch HCl loãng dư thu được(m+19) dung dịch Y.Phần trăm khối lượng của Mg trong X là bao nhiêu
Hòa tan hoàn toàn 15,4 gam hỗn hợp mg và zn bằng dung dịch hcl 2M thì thu được 6,72 (đktc)
a) Tính khối lượng Mg và Zn trong hỗn hợp
b) Tính thể tích dung dịch HCL 1M cần dùng
Mg+2HCl->MgCl2+H2
x------------------------x
Zn+2HCl->ZnCl2+H2
y-----------------------y
=>Ta có :\(\left\{{}\begin{matrix}24x+65y=15,4\\x+y=0,3\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}x=0,1mol\\y=0,2mol\end{matrix}\right.\)
=>m Mg=0,1.24=2,4g
=>m Zn=0,2.65=13g
b)VHCl=\(\dfrac{0,1.2+0,2.2}{2}\)=0,3l=300ml
Hòa tan hoàn toàn 10g hỗn hợp X gồm Mg và Fe bằng dung dịch HCl 2M. Kết thúc thí nghiệm thu được dung dịch Y và 5,6l khí H2 (đktc). Để kết tủa hoàn toàn các cation có trong Y cần vừa đủ 300ml NaOH 2M. Xác định thể tích dung dịch HCl ban đầu.
Hòa tan hoàn toàn 20 gam hỗn hợp Fe và Mg trong dung dịch HCl thu 1 gam khí H2. Khi cô cạn dung dịch thu được bao nhiêu gam muối khan?
A. 54,5(g)
B. 55,5(g)
C. 56,5(g)
D. 57,5(g)
Đáp án B.
• Cách 1:
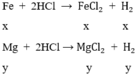
gọi x, y lần lượt là số mol của Fe và Mg trong hỗn hợp
số mol H2 là 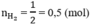
theo bài ra ta có hệ phương trình
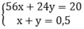
khối lượng muối khan là :
m = mFeCl2 + mMgCl2 = x(56 + 71) + y(24 + 71)
m = 56x + 24y + 71(x + y)
m = 20 + 71.0,5 = 55,5(g)
• Cách 2:
nmuối = 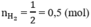
Khối lượng muối = m(kim loại) + m(gốc clorua) = 20,0 + 71. 0,5 = 55,5 (g)
Hòa tan 7,8g hỗn hợp Mg và Al bằng dung dịch HCl 2M,thu đc 8,96g lít khí đktc và dung dịch A a) tính số gam mỗi kim loại trong hỗn hợp ban đầu b)tính CM của chất có trong dung dịch HCl cần dùng để phản ứng hết hỗn hợp trên c)cho dung dịch A tác dụng với NaOH dư. Tính khối lượng kết tủa thu được
Đặt \(n_{Mg}=x(mol);n_{Al}=y(mol)\Rightarrow 24x+27y=7,8(1)\)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ PTHH:Mg+2HCl\to MgCl_2+H_2\\ 2Al+6HCl\to 2AlCl_3+3H_2\\ \Rightarrow x+1,5y=0,4(2)\\ (1)(2)\Rightarrow x=0,1(mol);y=0,2(mol)\\ a,m_{Mg}=0,1.24=2,4(g)\\ m_{Al}=7,8-2,4=5,4(g)\\ b,\Sigma n_{HCl}=2x+3y=0,8(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,8}{2}=0,4(l)\)
\(c,PTHH:MgCl_2+2NaOH\to Mg(OH)_2\downarrow+2NaCl\\ AlCl_3+3NaOH\to Al(OH)_3\downarrow+3NaCl\\ n_{MgCl_2}=n_{Mg(OH)_2}=x=0,1(mol)\\ n_{Al(OH)_3}=n_{AlCl_3}=y=0,2(mol)\\ \Rightarrow m_{Mg(OH)_2}=0,1.58=5,8(g)\\ m_{Al(OH)_3}=0,2.78=15,6(g)\\ m_{kết tủa}=5,8+15,6=21,4(g)\)
Hòa tan 2,4 gam kim loại Mg vào dung dịch HCl 2M vừa đủ a) viết phương trình hóa học phản ứng đã xảy ra b) tính thể tích dung dịch HCl 2M cần dùng tính khối lượng muối tạo thành ,c)Nếu m mg = 2,4 gam thể tích dung dịch HCl 2M phản ứng chỉ bằng 50ml thì cần dùng bao nhiêu gam dung dịch H2 SO4 10% hòa tan hết lượng mg dư
a.Mg+2HCl->MgCl2+H2
b.nMg=0,1(mol)=>nHCl=0,2(mol)
=>VHCl=0,2/2=0,1(l)=100(ml)
nMgCl2=0,1(mol)
=>mMgCl2=0,1*95=9,5(g)
c.nHCl pư=0,1(mol)
=>nMg dư=0,1-0,05=0,05(mol)
Mg+H2SO4->MgSO4+H2
nH2SO4=0,05(mol)=>mH2SO4=0,05*98=4,9(g)
mdd H2SO4=\(\dfrac{4,9\cdot100}{10}=49\left(g\right)\)