trộn 150 ml dd hỗn hợp hcl 0,3M và h2so4 0,1M với 100 ml dd hỗn hợp ba(0h)2 x M và koh 0,3M thu duoc dd có pH= 1,7 va m gam kết tủa ,Tính x và m
mn giup mik voi ạ
Trộn 250 ml dd hỗn hợp HCl 0,08 mol/l và H2SO4 0,01 mol/l với 250 ml dd Ba(OH)2 có nồng độ x mol/l thu được m gam kết tủa và 500 ml dd có pH = 12. Hãy tính m và x.
A. 0,06M và 5,825 gam
B. 0,01 M và 4,66 gam
C. 0,06M và 0,5825 gam
D. 0,0125M và 3,495 gam
Đáp án C
nBa(OH)2 = 0,25 x mol; nOH-= 0,5x mol
nH+ = 0,025 mol, nSO4(2-) = 0,0025 mol
H++ OH- → H2O
0,025 0,025 mol
Dung dịch sau phản ứng có pH = 12 nên OH- dư
nOH- dư = 0,5x- 0,025
[OH-] dư = nOH- dư/ Vdd = (0,5x- 0,025)/0,5 =10-2 suy ra a = 0,06 M
Ba2++ SO42- → BaSO4
0,015 0,0025 0,0025 mol
mBaSO4 = 0,5825 gam
Dung dịch X gồm NaHCO3 0,1M và K2CO3 0,2M. DD Y gồm HCL 0,4M và H2SO4 0,3M. Cho từ từ 20ml dd Y vào 60ml dd X,thu dk dd Z và Vml khí CO2. Cho 150ml dd hỗn hợp KOH 0,1M và BaCl2 0,25M vào Z, thu dk m gam kết tủa. Biết các phản ứng đều xảy ra hoàn toàn. Gía trị của V và m là:
nNaHCO3=0,006 mol=nHCO3-
nK2CO3=0,012 mol=nCO32-
nH2SO4=0,3.0,02=0,006 mol=nSO42-
Tổng nH+ trong dd Y=0,02.0,4+0,02.0,3.2=0,02 mol
Cho từ từ dd axit vào dd muối 1 lúc sau mới có khí xuất hiện
H+ +CO32- =>HCO3-
Bđ:0,02 mol 0,012 mol
Pứ:0,012 mol<=0,012 mol=>0,012 mol
Dư: 0,008 mol
H+ +HCO3- =>CO2 + H2O
0,008 mol 0,018 mol
0,008 mol =>0,008 mol=>0,008 mol
0,01 mol
V=0,008.22,4=0,1792 lit=179,2ml
nKOH =nOH-=0,015 mol
nBaCl2 =0,25.0,15=0,0375 mol=nBa2+
OH- + HCO3- => CO32- +H2O
0,015 mol. 0,01 mol
0,01 mol<=0,01 mol=>0,01 mol
0,005 mol
Ba2+ + CO32- =>BaCO3
0,0375 mol 0,01 mol
0,01 mol<=0,01 mol=>0,01 mol
0,0275 mol
Ba2+ + SO42- =>BaSO4
0,0275 mol 0,006 mol
0,006 mol =>0,006 mol
mBaSO4=1,398g
mBaCO3=0,01.197=1,97g
Tổng m=3,368g
ChọnB
Trộn 300 ml dd hh gồm H2SO4 0,1M và HCl 0, 15M với V ml dd hh gồm NaOH 0,3M và Ba(OH)2 0,1M, thu được dd X có pH = 12. Giá trị của V là:
\(n_{H^+}=0.3\cdot0.1\cdot2+0.3\cdot0.15=0.105\left(mol\right)\)
\(n_{OH^-}=0.001V\cdot0.3+0.001V\cdot2\cdot0.1=0.0032V\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(0.105.......0.105\)
\(n_{OH^-\left(dư\right)}=0.0032V-0.105\left(mol\right)\)
\(\left[OH^-\right]=\dfrac{0.0032V-0.105}{0.3+0.001V}\left(M\right)\)
\(pH=14+log\left[OH^-\right]=12\)
\(\Leftrightarrow log\left[OH^-\right]=-2\)
\(\Leftrightarrow log\left[\dfrac{0.0032V-0.105}{0.3+0.001V}\right]=-2\)
\(\Leftrightarrow V=33.85\left(ml\right)\)
nH+=0,3.0,1.2+0,3.0,15=0,105 mol
nOH- ban đầu =0,3V + 0,1.2V=0,5V mol
Sau phản ứng thu được dung dịch có pH=12
⇒OH- dư ⇒ pOH=2
⇒ [OH- ] dư = 0,01 M
nOH- dư = 0,01(0,3+V)=0,003+0,01V (mol)
nOH- phản ứng=nOH- ban đầu - nOH- dư
= 0,5V - 0,003 - 0,01V
= 0,49V - 0,003 (mol )
H+ + OH- → H2O
0,105 → 0,105
nOH- phản ứng = nH+
⇒0,49V - 0,003 =0,105
⇒ V≃0,22 lít=200ml
Trộn 3 dung dịch HCl 0,3M, HNO3 0,3M và H2SO4 0,2M vói thể thích bằng nhau thu được dung dịch X. Lấy 360 ml dung dịch X cho phản ứng dung dịch hỗn hợp Y gồm Ba(OH)2 0,08M và NaOH 0,23M thu được m gam kết tủa và dung dịch Z có pH = 2. Giá trị của m gần nhất với
A. 5,54
B. 5,42.
C. 5,59.
D. 16,61.
Trộn các dd axit HCl 0,3M; h2SO4 0,1M với những thể tích bằng nhau đc dd X. Dùng 300ml dd X trung hòa V ml dd B có NaOH 0,2M và KOH 0,15M thu đc dd Y.
1. Tính V
2. Cô cạn dd Y thu đc bao nhiêu gam muối khan
+nHCl=0.2*0.4=0.08(mol)
=>nH{+}=0.08(mol)
+nHNO3=0.1*0.4=0.04(mol)
=>nH{+}=0.04(mol)
+nH2SO4=0.15*0.4=0.06(mol)=nSO4{2-}
=>nH{+}=0.06*2=0.12(mol)
=>nH{+}(tổng)=0.08+0.04+0.12=0.24(mol)
+nNaOH=0.2*10^-3V(mol)
=>nOH{-}=2*10^-4V(mol)
+nBa(OH)2=0.05*10^-3V(mol)=nBa{2+}
=>nOH{-}=2*5*10^-5V=10^-4V(mol)
=>nOH{-}(tổng)=2*10^-4V+10^-4V=3*10^-4...
_Sau phản ứng thu được dung dịch có pH=13=>môi trường có tính bazơ.
=>pOH=14-13=1=>[OH-] dư=10^-1(M)
=>nOH{-} dư=10^-1*(0.4+10^-3V)(mol)
H{+}+OH{-}=>H2O
0.24->3*10^-4V...(mol)
0.24->0.24...........(mol)
0------>3*10^-4V-0.24.(mol)
=>3*10^-4V-0.24=0.04+10^-4V
<=>2*10^-4V=0.28
<=>V=1400(ml)
Vậy cần V=1400 ml
_Sau phản ứng kết tủa tạo thành là BaSO4:
+nBa{2+}=5*10^-5*(1400)=0.07(mol)
+nSO4{2-}=0.06(mol)
Ba{2+}+SO4{2-}=>BaSO4
0.07>0.06----------->0.06(mol)
=>mBaSO4=0.06*233=13.98(g)
Dung dịch X gồm NaHCO3 0,1M và K2CO3 0,2M. Dung dịch Y gồm HCl 0,4M và H2SO4 0,3M. Cho từ từ 20 ml Y vào 60 ml X, thu được dung dịch Z và V ml khí CO2 (đktc). Cho 150 ml dung dịch hỗn hợp KOH 0,1M và BaCl2 0,25M vào Z, thu được m gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của V và m là:
A. 44,8 và 4,353
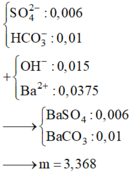
B. 179,2 và 3,368
C. 44,8 và 4,550
D. 179,2 và 4,353
Định hướng tư duy giải
Ta có:

Dung dịch Z chứa
Cho 100ml dd A chứa hỗn hợp HCl 0,1M và AlCl3 0,1M. Thêm V lít dd AgNO3 0,3M vào dd A thu được kết tủa lớn nhất là m gam. Tính giá trị nhỏ nhất của V và m
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4, 0,05M và HCL 0,1M với 100 ml dung dịch hỗn hợp NaOH 0,2M và Ba(OH)2 0,1M, được dung dịch X. Tính giá trị pH của dung dịch X và tính khối lượng kết tủa thu được.
`100mL=0,1L`
`n_{H^+}=0,1.0,05.2+0,1.0,1=0,02(mol)`
`n_{SO_4^{2-}}=0,1.0,05=0,005(mol)`
`n_{OH^-}=0,1.0,2+0,1.0,1.2=0,04(mol)`
`n_{Ba^{2+}}=0,1.0,1=0,01(mol)`
`Ba^{2+}+SO_4^{2-}->BaSO_4`
Do `0,01>0,005->` Tính theo `SO_4^{2-}`
`n_{BaSO_4}=n_{SO_4^{2-}}=0,005(mol)`
`->m_↓=0,005.233=1,165(g)`
`H^{+}+OH^{-}->H_2O`
Do `0,02<0,04->OH^-` dư
`n_{OH^{-}\ pu}=n_{H^+}=0,02(mol)`
`->n_{OH^{-}\ du}=0,04-0,02=0,02(mol)`
Trong X: `[OH^-]={0,02}/{0,1+0,1}=0,1M`
`->pH=14-pOH=14+lg[OH^-]=13`
Dung dịch X gồm NaHCO3 0,1M và K2CO3 0,2M. Dung dịch Y gồm dd HCl 0,4M và dd H2SO4 0,3M. Cho từ từ 20ml Y vào 60ml X thu được dd Z và V( ml) CO2. Cho 150ml dd hỗn hợp KOH 0,1M và BaCl2 0,25M vào Z thu được m(g) kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của V và m là?