Hoà tan hoàn toàn 6g hỗn hợp K và kl kiềm Mvào nước dư thì thấy có 4.48 lít h2 thoát ra.Xác định M

Những câu hỏi liên quan
Hoà tan hoàn toàn 6g hỗn hợp K và kl kiềm Mvào nước dư thì thấy có 4.48 lít h2 thoát ra.Xác định M
\(\overline{X}+H_2O\rightarrow\overline{X}OH+\frac{1}{2}H_2\)
\(n_{H_2}=0,2\) mol \(\Rightarrow n_{\overline{X}}=0,4\) mol
\(\Rightarrow\overline{X}=\frac{6}{0,4}=15\)
\(\Rightarrow M< 15\Rightarrow M\) là \(Li\)
P/s: đây là box Toán
Đúng 0
Bình luận (1)
khử hoàn toàn 2,4g hỗn hợp CuO và FexOy cùng số mol như nhau bằng hidro thu được 1,76g kim loại. Hoà tan kl đó = dung dịch HCL dư thấy thoát ra 0,448 lít H2 ở đktc.Xác định CTHH của oxit sắt
hòa tan hoàn toàn 8,8g hỗn hợp 2 kim loại Cu,Fe vào dung dịch HCl dư, sau phản ứng thấy còn lại 3,2g chất rắn không tan và có V lít khí ko màu(đktc) thoát ra.Xác định giá trị của V
Còn 3,2g chất rắn không tan chính là khối lượng Cu.
\(m_{Cu}=3,2g\Rightarrow m_{Fe}=8,8-3,2=5,6g\)
\(\Rightarrow n_{Fe}=\dfrac{5,6}{56}=0,1mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
Đúng 2
Bình luận (0)
hòa tan hoàn toàn 8,8g hỗn hợp 2 kim loại Cu,Fe vào dung dịch HCl dư, sau phản ứng thấy còn lại 3,2g chất rắn không tan và có V lít khí ko màu(đktc) thoát ra.Xác định giá trị của V
\(m_{rắn}=m_{Cu}=3,2\left(g\right)\\ \Rightarrow m_{Fe}=8,8-3,2=5,6\left(g\right)\\ \Rightarrow n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{H_2}=n_{Fe}=0,1\left(mol\right)\\ \Rightarrow V=V_{H_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\)
Đúng 2
Bình luận (0)
Ta có chất ko tan là Cu
=>m Fe=8,8-3,2=5,6g
=>n Fe=\(\dfrac{5,6}{56}\)=0,1 mol
Fe+HCl->FeCl2+H2
0,1---------------------0,1 mol
=>VH2=0,1.22,4=2,24l
Đúng 1
Bình luận (0)
khử hoàn toàn 2,4g hỗn hợp CuO và FexOy cùng số mol như nhau bằng hidro thu được 1,76g kim loại. Hoà tan kl đó = dung dịch HCL dư thấy thoát ra 0,448 lít H2 ở đktc.Xác định CTHH của oxit sắt
bt:Khử hoàn toàn 2,4g hỗn hợp CuO và FexOy cùng số mol như nhau bằng Hidro thu được 1,76 g kim loại , hòa tan kim loại đó =dung dịch HCl dư thấy thoát 448 cm3 khí Hidro(ở đktc).XĐCTHH của oxit sắt.
448 cm3 = 0,448 lít
PTHH:
CuO + H2 → Cu + H2O (1)
FexOy + yH2 → xFe + yH2O (2)
Sau khi phản ứng giữa CuO và FexOy kết thúc ta lấy Cu và Fe tác dụng với HCl. Nhưng Cu không tác dụng với HCl nên t có PTHH
Fe + 2HCl → FeCl2 + H2 (3)
Số mol Hidro là: 0,448 : 22,4 =0,2 mol
Theo PTHH (3):
Số mol Fe bằng số mol H2 nên số mol Fe là 0,02 mol
\Rightarrow Khối lượng Fe là: 0,02.56= 1.12 gam
Vì lượng sắt phản ứng hết nên khối lượng sắt ở phương trình 3 bằng khối lượng sắt ở phương trình 2
Mà khối lượng của Cu + Fe là 1,76g
\Rightarrow mCu = 1,76 - 1,12 = 0,64 g \Rightarrow Số mol Cu là 0,64 :64 = 0,01 mol
Theo PTHH (1)
Số mol CuO bằng số mol Cu nên
số mol CuO là 0,01 mol
\Rightarrow Khối lượng CuO là 0,01.80 = 0,8g
\Rightarrow Khối lượng FexOy là 2,4 - 0,8 = 1,6g
Vì số mol của CuO bằng số mol FexOy (giả thiết) nên số mol FexOy là 0,01 mol
\Rightarrow Khối lượng mol của FexOy là 1,6 : 0,01 = 160 (g)
Lập hệ phương trình về FexOy và giải hệ phương trình ta được( quan hệ về Khối lượng và khối lượng mol)
\Rightarrowx= 2
y= 3
Công thức hóa học của Oxit : Fe2O3
Đúng 0
Bình luận (0)
nH2= 0,448/22,4= 0,02(mol)
PTHH :
CuO + H2 -tdo--> Cu + H20
FexOy + yH2 -tdo-> xFe + yH20
Cu + HCl --> k pu
Fe + 2HCl ---> FeCl2 + H2
0,02 -- 0,04---> 0,02 --- 0,02 (mol)
mFe = 0,02 .56= 1,12(g)
=> mCu = 1,76 - 1,12= 0,64(g)
n Cu = 0,64 /64 =0,01(mol)
PTHH :
CuO + H2 -tdo-> Cu + H20
0,,01 --0,01 ----> 0,01(mol)
mCuO= 0,01 . 80 = 0,8(g)
=> mFexOy = 2,4-0,8= 1,6(g)
PTHH :
FexOy + yH2 ---> xFe + yH20
56x+ 16y ---------> 56x
1,6 (g) -------------> 1,12(g)
<=> 1,6 .56x = 1,12( 56x + 16y)
<=> 89,6x = 62,72 x + 17,92y
<=> 89,6x - 62,72x = 17,92y
<=> 26,88 x = 17,92y
=> x/y= 17,92 / 26,88 =2/3
Vậy công thức đúng là Fe203.
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn hỗn hợp X gồm 3 kim loại kiềm vào nước thu được 4,48 lít khí H2 (đktc). Nếu cũng cho lượng X như trên tác dụng với O2 dư thì thu được 3 oxit và thấy khối lượng chất rắn tăng m gam. Giá trị của m là: A. 3,2. B. 1,6. C. 4,8. D. 6,4.
Đọc tiếp
Hoà tan hoàn toàn hỗn hợp X gồm 3 kim loại kiềm vào nước thu được 4,48 lít khí H2 (đktc). Nếu cũng cho lượng X như trên tác dụng với O2 dư thì thu được 3 oxit và thấy khối lượng chất rắn tăng m gam. Giá trị của m là:
A. 3,2.
B. 1,6.
C. 4,8.
D. 6,4.
Đáp án A
Vì khối lượng hỗn hợp X sử dụng ở hai trường hợp là như nhau và hóa trị của các kim loại kiềm luôn là I không đổi nên số mol electron trao đổi ở hai trường hợp bằng nhau.
Áp dụng định luật bảo toàn mol electron ta có:
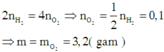
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 16,3g hỗn hợp Na và K vào 1500ml nước, thấy thoát ra 5,6 lít H2(đktc). % khối lượng của K là:
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 2Na + 2H2O → 2NaOH + H2
Mol: 2x x
PTHH: 2K + 2H2O → 2KOH + H2
Mol: 2y y
Ta có: \(\left\{{}\begin{matrix}2x+2y=16,3\\x+y=0,25\end{matrix}\right.\)
⇒ không giải đc (đề sai)
Đúng 0
Bình luận (0)
Hoà tan 18,2 gam hỗn hợp A gồm Fe và kim loại M hoá trị 3 không đổi bằng dung dịch HCL thì thoát ra 7,84 lít H2 ( đktc ). Xác định M, biết 1,4 gam M bị hoà tan hoàn toàn trong 70ml dung dung HCL 1 M
Hòa tan hoàn toàn 7,7g hỗn hợp gồm hai kim loại Al và Na bằng dung dịch HCl dư thấy thoát ra 7,84 lít khí H2 (ở đktc). Tính thể tích khí H2 thu được khi cho hỗn hợp trên vào lượng nước dư