Hòa tan hoàn toàn 10,6g Na2CO3 vào nước được 200ml dd Na2CO3.Tính nồng độ % và nồng độ mol của dd trên.Biết khối lượng riêng cuả dd là 1,05g/ml

Những câu hỏi liên quan
Hòa tan 21,2g Na2CO3 vào nước ta được 300ml dd Na2CO3. Biết D= 1,05g/ml. Tính nồng độ phần trăm và nồng độ mol của dung dịch.
\(n_{Na_2CO_3}=\dfrac{21,2}{106}=0,2\left(mol\right)\)
=> \(C_M=\dfrac{0,2}{0,3}=0,667M\)
\(m_{dd}=300.1,05=315\left(g\right)\)
=> \(C\%=\dfrac{21,2}{315}.100\%=6,73\%\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 10.6g Na2CO3 vào nước được 200ml dung dịch Na2CO3 . Tính nồng độ phần trăm và nồng độ mol của dung dịch trên. Biết khối lượng riêng của dung dịch là 1.05g/ml
\(n_{Na_2CO_3}=\dfrac{10,6}{106}=0,1\left(mol\right)\\ \rightarrow C_{M\left(Na_2CO_3\right)}=\dfrac{0,1}{0,2}=0,5M\)
Ta có: \(C\%=\dfrac{C_M.M}{10.D}\)
\(\rightarrow C\%=\dfrac{0,5.106}{10.1,05}=5,05\%\)
Đúng 1
Bình luận (0)
Cân 10,6g muối
N
a
2
C
O
3
cho vào cốc chia độ. Rót vào cốc khoảng vài chục ml nước cất, khuấy cho muối tan hết. Sau đó rót thêm nước vào cốc cho đủ 200ml. Ta được dung dịch
N
a
2
C
O
3
có khối lượng riêng là 1,05g/ml. Hãy tính nồng độ phần trăm và nồng độ mol của dung dịch vừa pha chế.
Đọc tiếp
Cân 10,6g muối N a 2 C O 3 cho vào cốc chia độ. Rót vào cốc khoảng vài chục ml nước cất, khuấy cho muối tan hết. Sau đó rót thêm nước vào cốc cho đủ 200ml. Ta được dung dịch N a 2 C O 3 có khối lượng riêng là 1,05g/ml. Hãy tính nồng độ phần trăm và nồng độ mol của dung dịch vừa pha chế.
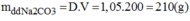
Nồng độ phần trăm của dung dịch pha chế:
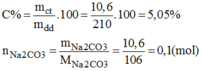
Nồng độ mol của dung dịch:
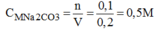
Đúng 0
Bình luận (0)
Cho 5.2g na2co3 vào nước thu được 100ml dd có khối lượng riêng là 1,05g/mol. Tính nồng độ phần trăm của dd thu được
$m_{dung\ dịch}= D.V = 1,05.100 = 105(gam)$
$C\%_{Na_2CO_3} = \dfrac{5,2}{105}.100\% = 4,95\%$
Đúng 1
Bình luận (0)
Ta có: mdd= D.V= 1,05.100= 105(g)
C%ddNa2CO3= 5.2.100%/105=4,95%
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 15,9g Na2C03 vào nước tạo ra 300m dung dịch có khối lượng riêng là D= 1,05g/ml. Tính nồng độ mol và nồng độ phần trăm của dung dịch Na2CO3 tạo thành. CÁC BẠN CÓ THỂ GIÚP MÌNH ĐƯỢC KHÔNG Ạ? MAI MÌNH THI RỒI Ạ.
Ta có: \(m_{dd}=300\cdot1,05=315\left(g\right)\) \(\Rightarrow C\%_{Na_2CO_3}=\dfrac{15,9}{315}\cdot100\%\approx5,05\%\)
Mặt khác: \(n_{Na_2CO_3}=\dfrac{15,9}{106}=0,15\left(mol\right)\) \(\Rightarrow C_{M_{Na_2CO_3}}=\dfrac{0,15}{0,3}=0,5\left(M\right)\)
Đúng 1
Bình luận (4)
Hòa tan hoàn toàn 28,6 g Na2CO3.10H2O vào đủ để tạo thành 200 ml dd. Xác định nồng độ % và nồng độ mol của dd. Biết dd này có KLR D = 1,05g/ml
$n_{Na_2CO_3} = n_{Na_2CO_3.10H_2O} = \dfrac{28,6}{286} = 0,1(mol)$
$C_{M_{Na_2CO_3}} = \dfrac{0,1}{0,2} = 0,5M$
$m_{dd} = D.V = 200.1,05 = 210(gam)$
$C\%_{Na_2CO_3} = \dfrac{0,1.106}{210}.100\% = 5,05\%$
Đúng 3
Bình luận (0)
\(m_{dd}\)=1,05.200=210 g
=>C%dd =\(\dfrac{28,6}{210}\) .100% =13,62%
Mặt khác : 200ml=0,2l
Mct=23.2+12+16.3+10.(1.2+16)=286 (M nguyên tử khối )
=>nct=\(\dfrac{28,6}{286}\) =0,1 mol
=>CM=\(\dfrac{0,1}{0,2}\) =0,5M
Đúng 1
Bình luận (0)
Cho 200ml dd Na2CO3 0.5M tác dụng vừa đủ với 200ml dd HCl , PƯ xảy ra hoàn toàn
a) Tính nồng độ mol của dd HCl
b) Tính khối lượng muối thu được
c) Tính nồng độ mol của dd thu đc
\(200ml=0,2l\\ n_{Na_2CO_3}=0,5.0,2=0,1\left(mol\right)\\ PTHH:Na_2CO_3+2HCl\rightarrow2NaCl+CO_2\uparrow+H_2O\\ \left(mol\right)........0,1\rightarrow...0,2.......0,2..........0,1.........0,1\\ a,C_{M_{HCl}}=\dfrac{0,2}{0,2}=1\left(M\right)\\ b,m_{NaCl}=0,2.58,5=11,7\left(g\right)\\c, V_{ddNaCl}=V_{ddNa_2CO_3}+V_{ddHCl}=0,2+0,2=0,4\left(l\right)\\ C_{M_{NaCl}}=\dfrac{0,2}{0,4}=0,5\left(M\right)\)
Đúng 3
Bình luận (1)
Na2CO3 + 2HCl → 2NaCl + H2O + CO2
a) nNa2CO3 = 0,2.0,5 = 0,1 mol
Theo tỉ lệ phản ứng => nHCl = 2nNa2CO3 = 0,1.2 = 0,2 mol
=> CHCl = \(\dfrac{n}{V}\) = \(\dfrac{0,2}{0,2}\)= 1M
b) nNaCl = 2Na2CO3 = 0,2 mol
=> mNaCl = 0,2.58,5 = 11,7 gam
c) Thể tích dung dịch sau phản ứng = 0,2 + 0,2 = 0,4 lít
=> CNaCl = \(\dfrac{0,2}{0,4}\)= 0,5M
Đúng 0
Bình luận (2)
Câu 1: Tính khối lượng muối NaNO3 cần lấy để khi hòa tan vào 170 g nước thì thu được dung dịch có nồng độ 15 %
Câu 2: Hòa tan 75 g tinh thể CuSO4.5H2O vào trong nước thu được 900 ml dd CuSO4. Tính CM dd này
Câu 3: Khối lượng riêng dd CuSO4 là 1,206 g/ml. Đem cô cạn 414,594 ml dd này thu được 140,625 g tinh thể CuSO4.5H2O . Tính nồng độ mol và nồng độ % dd nói trên.
Câu 1 :
Khối lượng dung dịch là : \(m_{ct}+170\)
Gọi khối lượng muối \(NaNO_3\)cần dùng là x
Ta có :\(m_{ct}=\frac{C\%.m_{dd}}{100}\)
hay \(x=\frac{15.\left(x+170\right)}{100}\)
Ta tính được x=30 (g)
Vậy khối lượng \(NaNO_3\)cần lấy là 30 g
Đúng 1
Bình luận (0)
Câu 2 :
Số mol \(CuSO_4.5H_2O\)là :
\(n_{CuSO_4.5H_2O}=\frac{m}{M}=\frac{75}{250}=0,3\left(mol\right)\)
\(\Rightarrow n_{CuSO_4}=0,3\left(mol\right);V_{dd}=900ml=0,9l\)
\(C_{M_{dd}}=\frac{n}{V}=\frac{0,3}{0,9}=\frac{1}{3}M\)
Vậy...
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 4,55g kim loại Zn vào 200 mL dd HCl (khối lượng riêng là 0,8 g/ml), sau PƯ thu đc V lít khí (đktc) và dd X
a) Tính nồng độ mol dd HCl tham gia PƯ
b) Tính giá trị V
c) Cô cạn dd X hoàn toàn, tính khối lượng chất rắn còn lại
d) Cho dd X PƯ đủ với 200g dd AgNO3, thu đc ddY. Tính nồng độ % dd Y
(Cho Zn=65, Cl=35.5, H=1)
\(n_{Zn}=\dfrac{4,55}{65}=0,07(mol)\\ Zn+2HCl\to ZnCl_2+H_2\\ a,n_{HCl}=0,14(mol)\\ \Rightarrow C_{M_{HCl}}=\dfrac{0,14}{0,2}=0,7M\\ b,n_{H_2}=0,07(mol)\\ \Rightarrow V_{H_2}=0,07.22,4=1,568(l)\\ c,n_{ZnCl_2}=0,07(mol)\\ \Rightarrow m_{ZnCl_2}=0,07.136=9,52(g)\\ c,ZnCl_2+2AgNO_3\to 2AgCl\downarrow+Zn(NO_3)_2\)
\(m_{dd_{ZnCl_2}}=200.0,8+4,55-0,07.2=164,41(g)\\ n_{AgCl}=0,14(mol);n_{Zn(NO_3)_2}=0,07(mol)\\ \Rightarrow C\%_{Zn(NO_3)_2}=\dfrac{0,07.189}{164,41+200-0,14.143,5}.100\%=3,84%\)
Đúng 3
Bình luận (0)

























