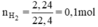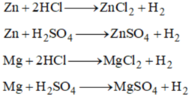1/ Có những chất sau : Fe, Al, dung dịch H2SO4 loãng và dung dịch HCl.
a ) Viết phương trình hóa học các phản ứng điều chế được khí hidro ?
b) cần điều chế 11,2 lít khí hidro (đktc) chọn kim loại nào để sử dụng khối lượng nhỏ nhất ?
2/ cho những hợp chất sau Na2O, HCl, ZnO, ZnSO4 , FeO, Fe(OH)2, H3PO4, CO, HNO3, AlCl3, Al2(SO4)3, FeSO4, NaPO4, NaH2PO4, Cu(NO3)2, Ba(OH)2.
Hợp chất nào thuộc loại : oxit, axit, bazo, muối ? Gọi tên
3/. Có 3 lọ đựng 3 chất lỏng không màu : nước, nước vôi trong, dung dịch axit sunfuric loãng. Hãy nêu phương trình hóa học nhận biết ba chất lỏng đựng trong mỗi lọ.
4/ viết phương trình hóa học biểu diễn các chất biến đổi sau :
a) KMn04 --> O2 --> SO2 --> SO3 --> H2SO4 --> Al2(SO4)3
b) Ca --> CaO --> Cả(OH)2 --> CaCo3 --> CaO
c) Al --> AlCl3 --> Al(OH)3 --> Al2O3 --> Al
5/. Trộn 2 lít dung dịch đường 0,5M với 3 lít dung dịch đường 1M. Tính nồng độ mol của dung dịch đường sau khi trộn.
6/. Hòa tan 50 gam đường vào nước được dung dịch nước đường có nồng độ 25% Hãy tính :
a) Khối lượng dung dịch đường pha chế được
b) Khối lượng nước cần dùng cho sự pha chế.
7. Cho 22,4 g sắt tác dụng với dung dịch loãng có chứa 24,5 g axit sunfuric
a) Tính khối lượng của chất còn dư sau phản ứng
b) tính thể tích khí hidro thu được sau phản ứng
c) Tính khối lượng muối thu được sau phản ứng