Khử 48 gam đồng (II) oxit bằng khí hiđro . Hãy :
a) Tính số gam đồng kim loại thu được
b) Tính thể tích khí hiđro (đktc) cần dùng
Khử 48 gam đồng(II) oxit bằng khí hiđro. Hãy:
a) Tính số gam đồng kim loại thu được.
b) Tính thể tích khí hiđro (đktc) cần dùng.
nCuO = 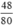 = 0,6 mol.
= 0,6 mol.
Phương trình hóa học của phản ứng khử CuO:
CuO + H2 → Cu + H2O.
nCu = 0,6mol.
mCu = 0,6 .64 = 38,4g.
Theo phương trình phản ứng trên:
nH2 = 0,6 mol
VH2 = 0,6 .22,4 = 13,44 lít.
Khử 48 gam đồng(II) oxit bằng khí hiđro. Hãy:
a) Tính khối lượng đồng thu được.
b) Tính thể tích khí hiđro (đktc) cần dùng.
Bài 6: Khử 48 gam đồng (II) oxit bằng khí hidro. Hãy:
a) Tính số gam đồng kim loại thu được
Tính thể tích khí hiđro (đktc) cần dùng
nCuO = 48 : 80 = 0,6 (Mol)
pthh : CuO + H2 -t--> Cu + H2O
0,6---->06------>0,6
=> mCu= 0,6 . 64 = 38,4 (G)
=> VH2 = 0,6 .22,4 = 13,44 (L)
a, \(n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
0,6 0,6 0,6
\(\rightarrow\left\{{}\begin{matrix}m_{Cu}=0,6.64=38,4\left(g\right)\\V_{H_2}=0,6.22,4=13,44\left(l\right)\end{matrix}\right.\)
PTHH : \(CuO+H_2\left(t^o\right)->Cu+H_2O\) (1)
a) \(n_{CuO}=\dfrac{m}{M}=\dfrac{48}{64+16}=0,6\left(mol\right)\)
Từ (1) -> \(n_{Cu}=n_{CuO}=n_{H_2}=0,6\left(mol\right)\)
-> \(m_{Cu}=n.M=0,6.64=38,4\left(g\right)\)
\(V_{H_2}=n.22,4=0,6.22,4=13,44\left(l\right)\)
khử 9,6 gam đồng (ll) oxit bằng khí hiđro. hãy:
a)tính số gam đồng kim loại thu được;
b)tính thể tích khí hiđro (đktc)cần dùng.
\(n_{CuO}=\dfrac{9,6}{80}=0,12mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,12 0,12 0,12
a)\(m_{Cu}=0,12\cdot64=7,68g\)
b)\(V=0,12\cdot22,4=2,688l\)
\(n_{CuO}=\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{9,6}{80}=0,12mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,12 0,12 0,12 ( mol )
\(m_{Cu}=n_{Cu}.M_{Cu}=0,12.56=6,72g\)
\(V_{H_2}=n_{H_2}.22,4=0,12.22,4=2,688l\)
1/ khử 48 gam đồng (II) Oxit bằng khí hiđro.hãy
tính số gam đồng kim loại thu được
tính thể tích khí hiđro (đktc) cần dùng
2/ tính số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít khí oxi (các thể tích khí đo ở đktc)
1/ \(CuO+H_2-^{t^o}\rightarrow Cu+H_2O\)
\(n_{Cu}=n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\)
=> \(m_{Cu}=0,6.64=38,4\left(g\right)\)
\(n_{H_2}=n_{CuO}=0,6\left(mol\right)\)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
2. \(2H_2+O_2-^{t^o}\rightarrow2H_2O\)
\(n_{H_2}=0,375;n_{O_2}=0,125\)
Lập tỉ lệ \(\dfrac{0,375}{2}>\dfrac{0,125}{1}\)
=> Sau phản ứng H2 dư, tính theo số mol O2
\(n_{H_2O}=2n_{O_2}=0,25\left(mol\right)\)
=> \(m_{H_2O}=0,25.18=4,5\left(g\right)\)
Khử 0,8g đồng (II) oxit bằng khí hiđro. (Cho Cu = 64; H = 1; O = 16; Cl = 35,5).Hãy: a/Tính số gam đồng kim loại thu được? b/Tính thể tích khí hiđro (đktc) cần dùng? c/Để có lượng H2 đó phải lấy bao nhiêu gam Fe cho tác dụng vừa đủ với bao nhiêu gam dd axit HCl 20
`n_[CuO]=[0,8]/80=0,01(mol)`
`H_2 + CuO` $\xrightarrow{t^o}$ `Cu + H_2 O`
`0,01` `0,01` `0,01` `(mol)`
`a)m_[Cu]=0,01.64=0,64(g)`
`b)V_[H_2]=0,01.22,4=0,224(l)`
`c)`
`Fe + 2HCl -> FeCl_2 + H_2`
`0,01` `0,02` `0,01` `(mol)`
`@m_[Fe]=0,01.56=0,56(g)`
`@m_[dd HCl]=[0,02.36,5]/20 . 100=3,65(g)`
Ta có: \(n_{Fe_2O_3}=\dfrac{48}{160}=0,3\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
_____0,3_____0,9___0,6____0,9 (mol)
a, \(m_{Fe}=0,6.56=33,6\left(g\right)\)
b, \(V_{H_2}=0,9.22,4=20,16\left(l\right)\)
c, PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{H_2O}=0,9\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,9.22,4=20,16\left(l\right)\)
\(a)\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ n_{Cu} = n_{CuO} = \dfrac{4}{80} = 0,05(mol)\\ \Rightarrow m_{Cu} = 0,05.64 = 3,2(gam)\\ b)\\ n_{H_2} = n_{CuO} = 0,05(mol)\\ V_{H_2} = 0,05.22,4 = 1,12(lít)\)
Khử 21,7 gam thủy ngân(II) oxit bằng hiđro. Hãy:
a) Tính số gam thủy ngân thu được.
b) Tính số mol và thể tích khí hiđro (đktc) cần dùng.
nHgO = 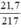 = 0,1 mol.
= 0,1 mol.
Phương trình hóa học của phản ứng khử HgO:
HgO + H2 → Hg + H2O
nHg = 0,1 mol.
mHg = 0,1 .201 = 20,1g.
nH2 = 0,1 mol.
VH2 = 0,1 .22,4 =2,24l.
9,6 gam đồng (2) = khí hiđro hãy
a)tính số gam đồng kim loại thu đc
b) tích thể tích khí hiđro (đktc)cần dùng
a, nCuO = 9,6/80 = 0,12 (mol)
PTHH: CuO + H2 -> (t°) Cu + H2O
Mol: 0,12 ---> 0,12 ---> 0,12
mCu = 0,12 . 64 = 7,68 (g)
b, VH2 = 0,12 . 22,4 = 2,688 (l)