Tính lượng tinh thể CuSO4.5H2O cần dùng để điều chế 500ml dung dịch CuSO4 8% (D=1,1 g/mol)

Những câu hỏi liên quan
Tính khối lượng tinh thể CuSO4.5H2O cần dùng hòa tan hoàn toàn vào 400 gam dung dịch CuSO4 2% để thu được dung dịch CuSO4 1M ( D = 1,1 g/ml).
Gọi số mol CuSO4.5H2O cần lấy là x (mol) => nCuSO4 = x (mol)
Khối lượng CuSO4 2% có trong 400 gam dung dịch là:
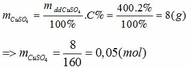
Tổng số mol CuSO4 sau khi hòa tan là: x + 0,05 (mol)
=> thể tích dung dịch sau khi hòa tan:

Từ (1) và (2)
=> (x+ 0,05).1000
=> 1100x + 55 = 160x + 400
=> 850x = 345
=> x ≈0, 406 (mol)
=> mCuSO4.5H2O = 0,406.250 = 101,47 (g)
Đúng 1
Bình luận (0)
a) Cần lấy bao nhiêu gam tinh thể CuSO4.5H2O và bao nhiêu gam dung dịch CuSO4 8% để điều chế được 280g dung dịch CuSO4 15%
b) Khối lượng riêng của một dung dịch CuSO4 là 1,206 g/ml. Đem cô cạn 414,594 ml dung dịch này thu được 140,625g tinh thể CuSO4.5H2O. Tính nồng độ C% và CM của dung dịch nói trên.
a)
Gọi $n_{CuSO_4.5H_2O} = a(mol) ; m_{dd\ H_2SO_4\ 8\%} = b(gam)$
Sau kho pha :
$m_{dd} = 250a + b = 280(1)$
$m_{CuSO4} = 160a + b.8\% = 280.15\%(2)$
Từ (1)(2) suy ra a = 0,14; b = 245(gam)
$m_{CuSO4.5H_2O} = 0,14.250 = 35(gam)$
Đúng 3
Bình luận (5)
b)
$n_{CuSO_4} = n_{CuSO_4.5H_2O} = \dfrac{140,625}{250} = 0,5625(mol)$
414,594 ml = 0,414594 lít
Suy ra :
$C_{M_{CuSO_4}} = \dfrac{0,5625}{0,414594} = 1,36M$
$m_{dd} = D.V = 1,206.414,594 = 500(gam)$
Suy ra :
$C\%_{CuSO_4} = \dfrac{0,5625.160}{500}.100\% = 18\%$
Đúng 3
Bình luận (0)
Để điều chế 560 g dung dịch CuSO4 16% cần phải lấy bao nhiêu gam dung dịch CuSO4 8% và bao nhiêu gam tinh thể CuSO4.5H2O
Để điều chế 560g dung dịch CuSO4 16% cần phải lấy bao nhiêu gam dung dịch CuSO4 8% trộn với bao nhiêu gam tinh thể CuSO4.5H2O.
\(m_{dd_{CuSO_4}}=a\left(g\right)\)
\(\Rightarrow m_{CuSO_4}=0.08a\left(g\right)\)
\(m_{CuSO_4\cdot5H_2O}=b\left(g\right)\)
\(\Rightarrow m_{CuSO_4}=\dfrac{b}{250}\cdot160=0.64b\left(g\right)\)
\(m_{dd_{CuSO_4\left(15\%\right)}}=a+b=560\left(g\right)\left(1\right)\)
\(m_{CuSO_4\left(15\%\right)}=0.08a+0.64b=560\cdot16\%=89.6\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=480,b=80\)
Đúng 5
Bình luận (0)
Gọi $m_{dd\ CuSO_4\ 8\%} = a(gam) ; n_{CuSO_4.5H_2O} = b(mol)$
Sau khi pha :
$m_{CuSO_4} = a.8\% + 160a = 560.16\% = 89,6(gam)$
$m_{dung\ dịch} = a + 250b = 560(gam)$
Suy ra a = 480(gam) ; b = 0,32(mol)$
$m_{CuSO_4.5H_2O} = 0,32.250 = 80(gam)$
Đúng 4
Bình luận (0)
câu 1 : Hòa tan 5,72g Na2CO3.xH2O trong 44,28g nước ta được dung dịch có nồng độ 4,24% . Xác định công thức của hidrat trên
câu 2 : Tính khối lượng CuSO4.5H2O tách ra khi làm lạnh 1877g dung dịch bão hòa của CuSO4 Ở 850C xống 12 oC biết độ tan của CuSO4 ở 85 oC và 12oC lần lượt là 87,7 g và 35,5 g
câu 3 : Điều chế 560g dung dịch CuSO4 16% cần phải lấy bao nhiêu gam dung dịch CuSO4 8% và bao nhiêu gam tinh thể CuSO4.5H2O
câu 4 : Hòa tan 0,35g Na2CO3.102O vào 234,9 g nước đước dung dịch A
a, T...
Đọc tiếp
câu 1 : Hòa tan 5,72g Na2CO3.xH2O trong 44,28g nước ta được dung dịch có nồng độ 4,24% . Xác định công thức của hidrat trên
câu 2 : Tính khối lượng CuSO4.5H2O tách ra khi làm lạnh 1877g dung dịch bão hòa của CuSO4 Ở 850C xống 12 oC biết độ tan của CuSO4 ở 85 oC và 12oC lần lượt là 87,7 g và 35,5 g
câu 3 : Điều chế 560g dung dịch CuSO4 16% cần phải lấy bao nhiêu gam dung dịch CuSO4 8% và bao nhiêu gam tinh thể CuSO4.5H2O
câu 4 : Hòa tan 0,35g Na2CO3.102O vào 234,9 g nước đước dung dịch A
a, Tính C% dung dịch A
b, Tính nồng độ mol dung dịch A
c, Tính khối lượng riêng của dung dịch A
câu 5 : Tính lượng tinh thể CuSO4.HH2O cần dùng để điều chế 500ml dung dịch CuSO4 8% (D=1,1g/ml)
Câu 4:
mdd = 0.35*106+0.35*10*18+234.9=335g
=> C% dd Na2CO3 = 0.35*106*100/335 = 11.07%
Vdd = 0.35*10*18+234.9=297.9ml (coi như Na2CO3 có thể tích ko đáng kể)
=> CmddNa2CO3 = 0.35/0.2979=1.17M
=> D = m/V = 335/297.9 = 1.12 g/ml
Đúng 0
Bình luận (0)
Câu 3:
:trong 560g d^2CuSO4 16%
\(mct=\dfrac{16.560}{100}=89,6g\)
Đặt mCuSO4.5H2O = x(g)
1mol(hay 250g) CuSO4.5H2O chứa 160g CuSO4
Vậy x(g) // chứa = (g)
mdd CuSO4 8% có trong dd CuSO4 16% là ( 560 - x ). g
mct CuSO4( có trong dd CuSO4 8%) là = \(\dfrac{8\left(560-x\right)}{100}=\dfrac{2\left(560-x\right)}{25}\left(g\right)\)
Ta có phương trình: \(\dfrac{560-x)2}{25}+\dfrac{16x}{25}=89,6\)
Giải phương trình được: x = 80.
Vậy cần lấy 80g tinh thể CuSO4.5H2O và 480g dd CuSO4 8% để pha chế thành 560g dd CuSO4 16%.
Ta có phương trình:
Đúng 0
Bình luận (0)
Câu 4)
mdd = 0,35 . 106 + 0,35 . 10 . 18 + 234,9=335g
=> C%\(_{Na_2CO_3}\) = 0,35 . 106 . \(\dfrac{100}{355}\) = 11,07%
V\(_{dd}\) = 0,35 . 10 . 18 + 234,9 = 297,9ml
=> CM\(_{Na_2CO_3}\) = \(\dfrac{0,35}{0,2979}\)=1.17M
=> D = \(\dfrac{m}{V}\) = \(\dfrac{355}{297,9}\) = 1.12 (g/ml)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Dung dịch CuSO4 loãng được dùng làm thưốc diệt nấm. Để điều chế 800 gam dung dịch CuSO4 5% thì khối lượng CuSO4.5H2O cần dùng là?
A. 62,5 gam
B. 40,0 gam
C. 32,0 gam
D. 25,6 gam
Đáp án : A
nCuSO4 = nCuSO4.5H2O = 0,25 mol
=> mCuSO4.5H2O = 62,5g
Đúng 0
Bình luận (0)
Cần lấy ?g tinh thể CuSO4.5H2O và ?g dd CuSO4 4% để điều chế 500g dd CuSO4 8%
Gọi mCuSO4.5H2O=a (a>0)
mdung dịch CuSO4(4%)=b (b>0)
mdung dịch sau pha trộn=mCuSO4.5H2O+mdung dịch CuSO4(4%)
= a+b=500(g) (1)
nCuSO4(4%)=nCuSO4.5H2O=\(\frac{a}{250}\) (mol)
mchât tan sau pha trộn=mchất tan 1+mchất tan 2
= \(\frac{a}{250}.160+\frac{4\%.b}{100\%}\)
=\(\frac{a}{250}.160+\frac{4b}{100}=40\left(g\right)\) (2)
Từ (1) và (2)
=> a=33,33g và b=466,67g
Vậy m CuSO4.5H2O=33,33g và mdd CuSO4 4%= 466,67g
Đúng 0
Bình luận (0)
CuSO4.5H2O→ddCuSO4
250....................160
100%..............→64%
m1 CuSO4 64%..........8
.......................16%......=1/6
m2 CuSO4 8%...........48
6m1=m2
m1+m2=280
=>m1=40
m2 = 240
Đúng 0
Bình luận (0)
CuSO4.5H2O→ddCuSO4
250....................160
100%..............→64%
m1 CuSO4 64%..........8
.......................16%......=1/6
m2 CuSO4 8%...........48
6m1=m2
m1+m2=280
=>m1=40
m2 = 240
Đúng 0
Bình luận (0)
1. Nêu cách phân biệt CaO, MgO, Na2O đều là chất bột màu trắng bằng thuốc thử tự
chọn.
2. Cần lấy bao nhiêu gam tinh thể CuSO4.5H2O và bao nhiêu gam dung dịch CuSO4 4%
để điều chế 500 gam dung dịch CuSO4 8%.
Câu 2.
Gọi \(m_{CuSO_4.5H_2O}=x\left(g\right);m_{CuSO_44\%}=y\left(g\right)\)
\(\Rightarrow x+y=500\left(1\right)\)
Khối lượng \(CuSO_4\) có trong tinh thể \(CuSO_4.5H_2O\) là:
\(m=\dfrac{x}{250}\cdot160=\dfrac{16}{25}x\left(g\right)\)
Khối lượng \(CuSO_4\) có trong \(CuSO_44\%\) là:
\(m=\dfrac{y\cdot4\%}{100\%}=\dfrac{y}{25}\left(g\right)\)
Khối lượng \(CuSO_4\) có trong \(CuSO_48\%\) là:
\(m=\dfrac{500\cdot8\%}{100\%}=40g\)
Bảo toàn cơ năng:
\(\Rightarrow\dfrac{16}{25}x+\dfrac{y}{25}=40\Rightarrow16x+y=1000\left(2\right)\)
Từ (1) và (2)\(\Rightarrow\left\{{}\begin{matrix}x=\dfrac{100}{3}\approx33,33g\\y=\dfrac{1400}{3}\approx466,67g\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Xác định khối lượng tinh thể CuSO4.5H2O và khối lượng nước cần lấy đủ để pha chế thành 400g dung dịch CuSO4 4%
e cần gấp nha
Đặt x,y lần lượt là khối lượng tinh thể và khối lượng nước cần lấy (x,y>0) (g)
Ta sẽ có hpt:
\(\left\{{}\begin{matrix}x+y=400\\\dfrac{160}{250}x=4\%.400\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x+y=400\\0,64x=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=25\\y=375\end{matrix}\right.\)
Vậy: Cần lấy 25 gam tinh thể và 375 gam nước để pha chế thành 400 gam dd CuSO4 4%
Đúng 2
Bình luận (0)


























