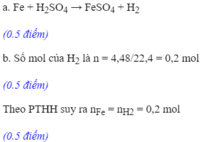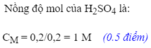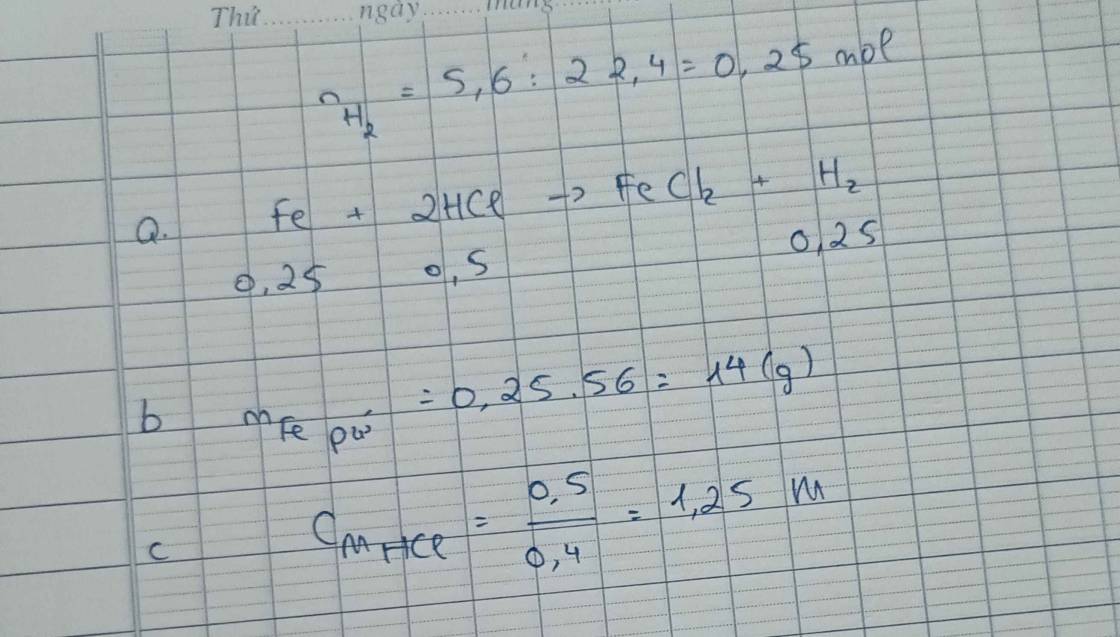cho 1 lượng bột Zn dư vào 70ml dung dịch HCl,phản ứng xong thu được 4,48l khí thoát ra (đktc)
a)viết phương trình phản ứng?
b)tính khối lượng Zn đã phản ứng?
c)tính nồng độ mol của dung dịch muối sau phản ứng? help me!!!

Những câu hỏi liên quan
cho 1 lượng bột Zn dư vào 70ml dung dịch HCl,phản ứng xong thu được 4,48l khí thoát ra (đktc)
a)viết phương trình phản ứng?
b)tính khối lượng Zn đã phản ứng?
c)tính nồng độ mol của dung dịch muối sau phản ứng?
HELP ME!!!!!!!!!!!!!!
a) Zn + 2HCl \(\rightarrow\) ZnCl2 + H2\(\uparrow\)
b) \(n_{H_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo phương trình: \(n_{Zn}=1\) ; \(n_{H_2}=1\) ; \(n_{HCl}=2\)
Mà \(n_{H_2}=0,2\left(mol\right)\Rightarrow n_{Zn}=0,2\left(mol\right)\) ; \(n_{HCl}=0,4\left(mol\right)\)
Ta có: \(m_{Zn}=n_{Zn}.M_{Zn}=0,2.65=13\left(g\right)\)
c) Đổi: 70ml = 0,07l
\(C_M=\dfrac{n}{V}=\dfrac{0,4}{0,07}\approx5,7\left(M\right)\)
Đúng 0
Bình luận (1)
cho 1 lượng bột Zn dư vào 70ml dung dịch HCl,phản ứng xong thu được 4,48l khí thoát ra (đktc)
a)viết phương trình phản ứng?
b)tính khối lượng Zn đã phản ứng?
c)tính nồng độ mol của dung dịch muối sau phản ứng? còn cái ni mới khó nè!!!!
a, Zn + 2HCl--> ZnCl2 + H2
b , Ta có nH2=4,48/22,4=0,2 mol
Ta có nZn PỨ = nH2= 0,2 mol
=> mZn PỨ= 0,2.65=13 g
c, Ta có nMgCl2=mH2=0,2 mol
=> CM dd MgCl2=0,2/0,07=2,857 M
Đúng 0
Bình luận (0)
Câu 3. Cho 1 lượng kẽm (Zn) dư tác dụng với 100 ml dung dịch axit HCI, phản ứng kết thúc thu được 6,72 lít khí (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính khối lượng kẽm đã tham gia phản ứng.
c) Tính nồng độ mol của dung dịch HCl
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,3.65=19,5\left(g\right)\)
c, \(n_{HCl}=2n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,6}{0,1}=6\left(M\right)\)
Đúng 1
Bình luận (0)
Cho 1 ít viên kẽm(zinc) dư vào 100ml dung dịch acid HCl. Phản ứng xong thu được 2,479 lít khí (đkc)
a/ viết phương trình hóa học xảy ra
b/ tính khối lượng kẽm tham gia phản ứng?
c/ tính nồng độ mol của dung dịch HCl đã dùng?
Cho Zn=65, Cl=35,5, O=16, H=1
\(n_{H_2}=\dfrac{2,479}{22,4}=\dfrac{2479}{22400}mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo pt ta có: \(n_{Zn}=n_{H_2}=\dfrac{2479}{22400}mol\)\(\approx0,11mol\)
\(\Rightarrow m_{Zn}\approx7,2g\)
\(n_{HCl}=2n_{H_2}=0,22mol\) \(\Rightarrow C_{M_{HCl}}=\dfrac{0,22}{0,1}=2,2M\)
Đúng 0
Bình luận (0)
Cho một lượng bột sắt dư vào 200ml dung dịch axit H 2 S O 4 . Phản ứng xong thu được 4,48 lít khí hiđrô (đktc)
a. Viết phương trình phản ứng hoá học
b. Tính khối lượng sắt đã tham gia phản ứng
c. Tính nồng độ mol của dung dịch axit H 2 S O 4 đã dùng
Cho 6,5gam Zn tác dụng với 100gam dung dịch HCl 14,6%a, Viết phương trình phản ứng xảy ra. b, Chất nào dư ? Tính thể tích khí thoát ra (ở đktc), khối lượng muối thu đượcc, Tính nồng độ phần trăm của các chất có trong dung dịch sau khi phản ứng kết thúc
\(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(n_{HCl}=\dfrac{100\cdot14.6\%}{36.5}=0.4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(1........2\)
\(0.1......0.4\)
\(LTL:\dfrac{0.1}{1}< \dfrac{0.4}{2}\Rightarrow HCldư\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(m_{\text{dung dịch sau phản ứng}}=6.5+100-0.1\cdot2=106.3\left(g\right)\)
\(C\%ZnCl_2=\dfrac{0.1\cdot136}{106.3}\cdot100\%=12.79\%\)
\(C\%HCl\left(dư\right)=\dfrac{\left(0.4-0.2\right)\cdot36.5}{106.3}\cdot100\%=6.87\%\%\)
Đúng 3
Bình luận (1)
Cho bột nhôm dư vào 500 ml dung dịch HCl. Phản ứng xong, thu được 16,8 lít khí H2 (đktc).
a/ Viết PTHH
b/ Tính khối lượng bột nhôm đã tham gia phản ứng
c/ Tính nồng độ mol của dung dịch HCl đã dùng
Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
a) Pt : 2Al +6HCl → 2AlCl3 + 3H2\(|\)
2 6 2 3
0,5 1,5 0,75
a) Số mol của nhôm
nAl = \(\dfrac{0,75.2}{3}=0,5\left(mol\right)\)
Khối lượng của nhôm
mAl = nAl . MAl
= 0,5 .27
= 13,5 (g)
c) Số mol của dung dịch axit clohidric
nHCl = \(\dfrac{0,5.6}{2}=1,5\left(mol\right)\)
500ml = 0,5l
Nồng độ mol của dung dịch axit clohdric đã dùng
CMHCl = \(\dfrac{n}{V}=\dfrac{1,5}{0,5}=3\left(M\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
2Al+6HCl->2AlCL3+3H2
=>nAl=\(\dfrac{2}{3}\)nH2=\(\dfrac{2}{3}\).16,8/22.4=0,5mol
=>mAl=27.0,5=13,5g
=>nHCl=2nH2=2.16,8/22,4=1,5mol
\(=>Cm=\dfrac{1,5}{\dfrac{500}{1000}}=3M\)
Đúng 2
Bình luận (0)
Câu 6: Cho một lượng mạt sắt dư vào 400 ml dung dịch HCl. Phản ứng xong, thu được 5,6 lít khí (đktc).a) Viết phương trình phản ứng.b) Tính khối lượng mạt sắt đã phản ứng.c) Tìm nồng độ mol của dung dịch HCl đã dùng.
Đọc tiếp
Câu 6: Cho một lượng mạt sắt dư vào 400 ml dung dịch HCl. Phản ứng xong, thu được 5,6 lít khí (đktc).
a) Viết phương trình phản ứng.
b) Tính khối lượng mạt sắt đã phản ứng.
c) Tìm nồng độ mol của dung dịch HCl đã dùng.
Cho một khối lượng mạt sắt dư vào 50 ml dung dịch HCl .Phản ứng xong thu được 3,36 lít khí (đktc) . Viết phương trình hóa học .Tính khối lượng mạt sắt đã tham gia phản ứng Tính nồng độ mol của dung dịch HCl đã dùng .
Giải giúp mik với ạ
\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,15 0,3 0,15
b) \(n_{Fe}=\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
⇒ \(m_{Fe}=0,15.56=8,4\left(g\right)\)
c) \(n_{HCl}=\dfrac{0,15.2}{1}=0,3\left(mol\right)\)
50ml = 0,05l
\(C_{M_{ddHCl}}=\dfrac{0,3}{0,05}=6\left(M\right)\)
Chúc bạn học tốt
Đúng 4
Bình luận (0)