Cho 5,6 g CaO vào nước tạo thành dung dịch A.Tính số g kết tủa tạo thành khi đem dung dịch A hấp thụ hoàn toàn 2,8 lít khí ccacbonic.
Các bn giúp mk cái nha ! Mai mk phải nộp bài rồi
Cho 5,6 gam CaO vào nước tạo thành dung dịch A. Hấp thụ hoàn toàn 2,8 lít khí S O 2 (đktc) vào dung dịch A thu được m gam kết tủa. Giá trị của m là
A. 9 gam
B. 3 gam
C. 7 gam
D. 10 gam
Chọn A
n C a O = 0 , 1 m o l ; n S O 2 = 0 , 125 m o l
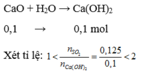
=> phản ứng sinh ra 2 muối CaS O 3 (x mol) và Ca(HS O 3 ) 2 (y mol)

Cho 2,8 g CaO vào H2O vào dung dịch A cho A hấp thụ 1,68 lít CO2 ( dktc ) Hỏi khối lượng kết tủa tạo thành
Các bạn ơi giúp mk vs nha
tom tat:
\(m_{CaO}=2,8g\)
\(V_{CO2}=1,68l\) \(\left(dktc\right)\)
\(m_{CaCO3}=?\)
bai giai
\(n_{CaO}=\frac{m_{CaO}}{M_{CaO}}=\frac{2,8}{40+16}=0,05\)
\(CaO+H20\rightarrow Ca\left(OH\right)_2\)
theo phuong trinh \(1mol\) \(1mol\)\(1mol\)
theo dau bai \(0,05mol\)
\(n_{CO2}=V.22,4=1,68.22,4=37,632\left(mol\right)\)
\(CO2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Theo phuong trinh \(1mol\) \(1mol\) \(1mol\) \(1mol\)
Theo dau bai \(37,632mol\) \(37,632mol\)
\(m_{CaCO3}=n.M=37,632.\left(40+12+16.3\right)\)
\(=37,632.100\)
\(=3763,2\left(g\right)\)
sua lai nha
\(n_{CO2}=\frac{V}{22,4}=\frac{1,68}{22,4}=0,075\)
\(m_{CaCO3}=n.M=0,075.\left(40+12+16.3\right)\)
\(=0,075.100\)
\(=7,5\left(g\right)\)
Mọi người ơi giải hộ em 2 bài hóa này với em cần phải nộp trong 1 ngày nữa
1, Người ta dùng 200 gam dung dịch NaOH 10% để hấp thụ hoàn toàn 5,6 lít khí CO2(đktc) . Muối nào được tạo thành, khối lượng là bao nhiêu ?
2, Cho 16,8 lít khí CO2(đktc) hấp thụ hoàn toàn vào 600 ml dung dịch NaOH 2M thu được dung dịch A .
a, Tính khối lượng muối trong dung dịch A
b, Lấy dung dịch A cho tác dụng với dung dịch BaCl2 dư . Tính khối lượng kết tủa tạo thành .
MỌI NGƯỜI GIÚP EM VỚI !!! EM CẦN NỘP BÀI SỚM EM CẢM ƠN TRƯỚC Ạ !!!!!!
1,
Có \(m_{ct_{NaOH}}=\frac{200.10}{100}=20g\)
\(\rightarrow n_{NaOH}=\frac{m}{M}=\frac{20}{40}=0,5mol\)
\(n_{CO_2}=\frac{V}{22,4}=\frac{5,6}{22,4}=0,25mol\)
Lập tỷ lệ \(T=\frac{n_{NaOH}}{n_{CO_2}}\)
\(\rightarrow T=\frac{0,5}{0,25}=2\)
Vậy sản phẩm là muối trung hoà duy nhất là \(Na_2CO_3\)
PTHH: \(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
Phản ứng xảy ra hết bởi vì \(\frac{n_{NaOH}}{2}=n_{CO_2}\)
\(\rightarrow n_{Na_2CO_3}=0,25mol\)
\(\rightarrow m_{Na_2CO_3}=0,25.106=26,5g\)
2,
a. Có \(n_{CO_2}=\frac{V}{22,4}=\frac{16,8}{22,4}=0,75mol\)
\(600ml=0,6l\)
\(n_{NaOH}=C_M.V=0,6.2=1,2mol\)
Xét tỷ lệ số mol \(T=\frac{n_{NaOH}}{n_{CO_2}}\)
\(\rightarrow T=\frac{1,2}{0,75}=1,6\)
\(\rightarrow1< T< 2\)
Vậy sản phẩm tạo thành hai muối là \(NaHCO_3;Na_2CO_3\)
Với PTHH có sản phẩm là \(Na_2CO_3\) đặt a là số mol của \(CO_2\)
Với PTHH có sản phẩm là \(NaHCO_3\) đặt b là số mol của \(CO_2\)
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\left(1\right)\)
\(NaOH+CO_2\rightarrow NaHCO_3\left(2\right)\)
Do vậy \(\hept{\begin{cases}2a\left(mol\right)=n_{NaOH}\left(1\right)\\b\left(mol\right)=n_{NaOH}\left(2\right)\end{cases}}\)
Có các biểu thức về số mol
\(∑n_{CO_2}=0,75mol\)
\(\rightarrow a+b=0,75\left(3\right)\)
\(∑n_{NaOH}=1,2mol\)
\(\rightarrow2a+b=1,2\left(4\right)\)
Từ (3) và (4), có hệ phương trình
\(\hept{\begin{cases}a+b=0,74\\2a+b=1,2\end{cases}}\)
\(\rightarrow\hept{\begin{cases}a=0,45mol\\b=0,3mol\end{cases}}\)
Thay số mol vào (1) \(\rightarrow m_{Na_2CO_3}=0,45.106=47,7g\)
Thay số mol vào (2) \(\rightarrow m_{NaHCO_3}=0,3.84=25,2g\)
Vậy tổng khối lượng mối trong dung dịch A sẽ là: \(m_A=m_{Na_2CO_3}+m_{NaHCO_3}=25,2+47,7=72,9g\)
b. Vì \(Na_2CO_3\) tác dụng với \(BaCl_2\) nên ta có
PTHH: \(BaCl_2+Na_2CO_3\rightarrow BaCO_3\downarrow+2NaCl\)
\(n_{BaCO_3}=n_{Na_2CO_3}=0,45mol\)
\(\rightarrow m_{BaCO_3}=0,45.197=88,65g\)
Hòa tan 2,8 gam Cao vào nước được dung dịch A a.Cho 1,68 lít khí CO2 hấp thụ hoàn toàn vào dung dịch A.Tính Khối lượng muối thu được b.Nếu dẫn khí CO2 qua dung dịch A và sau khi kết thúc thí nghiệm thu được 1 gam chất kết tủa.Tính khối lượng muối tạo thành. Tính thể tích khí CO2 tham gia phản ứng (đktc)
\(n_{CaO}=\dfrac{2,8}{56}=0,2\left(mol\right)\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
0,2 0,2
a. \(n_{CO_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,075 0,075
vì \(\dfrac{0,075}{1}< \dfrac{0,2}{1}\) => dd \(Ca\left(OH\right)_2\) dư sau pứ.
=> \(m_{CaCO_3}=0,075.100=7,5\left(g\right)\)
b. \(n_{CaCO_3}=\dfrac{1}{100}=0,01\left(mol\right)\)
Thấy: \(n_{CaCO_3}< n_{Ca\left(OH\right)_2}\)
Nên ta có 2 trường hợp.
TH 1: \(dd.Ca\left(OH\right)_2.dư\)
Có:
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,1 0,1
m muối tạo thành là m kt = 1 (g)
\(V_{CO_2}=0,1.22,4=2,24\left(l\right)\)
TH 2: khí \(CO_2\) dư
Có:
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,2 0,2 0,2
\(CO_2+CaCO_3+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
0,1 0,1 0,1
\(m_{muối}=m_{CaCO_3}+m_{Ca\left(HCO_3\right)_2}=1+0,1.162=17,2\left(g\right)\)
\(V_{CO_2}=0,3.22,4=6,72\left(l\right)\)
Hoà tan 2,8g CaO vào nước ta được dung dịch A. a. Cho 1,68 lít khí CO2 hấp thụ hoàn toàn vào dung dịch A. Hỏi có bao nhiêu gam kết tủa tạo thành b. Nếu cho khí CO2 sục qua dung dịch A. Tính thể tích khí CO2 tối đa có thể tham gia phản ứng ( các thể tích khí đó ở đktc)
nCaO=0,05(mol)
nCO2=0,075(mol)
a) PTHH: Ca + 2 H2O -> Ca(OH)2 + H2
nCa(OH)2=nCa=0,05(mol)
Ta có: 1< nCO2/nCa(OH)2= 0,075/0,05=1,5<2
=> Sp thu được là hỗn hợp 2 muối: CaCO3 và Ca(HCO3)2
PTHH: Ca(OH)2+ CO2 -> CaCO3 + H2O
x____________x________x(mol)
Ca(OH)2 + 2 CO2 -> Ca(HCO3)2
y________2y_______y(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}x+y=0,05\\x+2y=0,075\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,025\\y=0,025\end{matrix}\right.\)
=> m(kt)=mCaCO3=0,025.100=2,5(g)
b) V(CO2,tối đa)= 1,68(l)
M.n giúp e vs ạ. Mai nộp bài rùi
hòa tan 2,8g CaO vào trog nước thu được dd A. Cho 1,68 lít khí CO2 hấp thụ hoàn toàn vào dd A. Hổi có bao nhiêu gam kết tủa tạo thành?
cao+ h2o-> ca(oh)2
ncao=2,8/40=0,07 mol
nca(oh)2=ncao=0,07 mol
cho co2 hấp thụ hết dung dịch A có thể có các pư sau:
ca(oh)2+ co2-> caco3+ h2o (1)
a <-a-> a
ca(oh)2+ 2co2-> ca(hco3)2 (2)
0,5b <-b
nco2=1,68/22,4=0,075
thấy nco2/nca(oh)2=0,075/0,07=15/14 >1
=> pư tạo 2 muối
đặt nco2(1)=a, nco2(2)=b
=> a+ 0,5b=0,07
a+b=0,075
=> a=0,065, b=0,01
=> m↓= 0,065*100=6,5g
Cho V lít khí CO (đktc) qua ống sứ đựng m gam CuO nung nóng. Sau khi kết thúc phản ứng, dẫn khí tạo thành hấp thụ vào dung dịch NaOH dư. Sau đó cho thêm vào dung dịch thu được dung dịch BaCl2 dư thấy tạo thành n gam kết tủa. a. Viết các phương trình hoá học xảy ra. b. Tính hiệu suất của phản ứng khử CuO theo V, m, n. c. Nếu thay khí CO bằng khí H2 thì kết quả thay đổi như thế nào
a)
$CO + CuO \xrightarrow{t^o} Cu + CO_2$
$CO_2 + 2NaOH \to Na_2CO_3 + H_2O$
$Na_2CO_3 + BaCl_2 \to BaCO_3 + 2NaCl$
b)
n CO2 = n BaCO3 = n/197 (mol)
Nếu V/22,4 > m / 80 thì H =( m/80 : n/197) .100% = 197m/80n .100%
Nếu V/22,4 < m / 80 thì H =( V/22,4 : n/197) .100% = 197V/22,4m .100%
c)
Nếu thay CO bằng khí H2 thì kết quả thay đổi hoàn toàn ra khí sinh ra hấp thụ vào NaOH không tạo kết tủa với BaCl2
Đốt cháy hoàn toàn m g hỗn hợp C gồm FeS2 và Cu2S thu được khí SO2 và hỗn hợp rắn D gồm Fe2O3 và CuO .Chuyển toàn bộ SO2 thành SO3 rồi hấp thụ hết vào nước được dung dịch E . Cho toàn bộ D vào cốc chứa dung dịch E sau đó phải cho tiếp 375 ml dung dich HCL 2M vào cốc thì D mới vừa đủ tan hết tạo ra dung dịch F . Cho dung dịch F tác dụng với BaCl2 dư thu đc 116,5 g kết tủa
a) viết phương trình phản ứng xaỷ ra
b) tính m
Đốt cháy hoàn toàn m gam FeS2 rồi cho toàn bộ sản phẩm khí tạo thành hấp thụ hết vào 200 ml dung dịch Ba(OH)2 0,75M thấy tạo ra 21,7 gam kết tủa. Tính m
\(n_{BaSO_3}=\dfrac{21.7}{217}=0.1\left(mol\right)\)
\(BTBa:\)
\(n_{Ba\left(HSO_3\right)_2}=0.2\cdot0.75-0.1=0.05\left(mol\right)\)
\(BTS:\)
\(n_{FeS_2}=\dfrac{0.1+0.05\cdot2}{2}=0.1\left(mol\right)\)
\(m_{FeS_2}=0.1\cdot120=12\left(g\right)\)
$n_{Ba(OH)_2} = 0,2.0,75 = 0,15(mol)$
$n_{BaSO_3} = 0,1(mol)$
TH1: $Ba(OH)_2$ dư
Ba(OH)2 + SO2 → BaSO3 + H2O
0,1..............0,1.........0,1........................(mol)
Bảo toàn nguyên tố với S :
$n_{FeS_2} = \dfrac{1}{2}n_{SO_2} = 0,05(mol)$
$m = 0,05.120 = 6(gam)$
TH2 : Có tạo muối axit
Ba(OH)2 + SO2 → BaSO3 + H2O
0,1..............0,1.........0,1........................(mol)
Ba(OH)2 + 2SO2 → Ba(HSO3)2
0,05.............0,1........................................(mol)
$n_{SO_2} = 0,2(mol)$
$n_{FeS_2} = \dfrac{1}{2}n_{SO_2} = 0,1(mol)$
$m = 0,1.120 = 12(gam)$