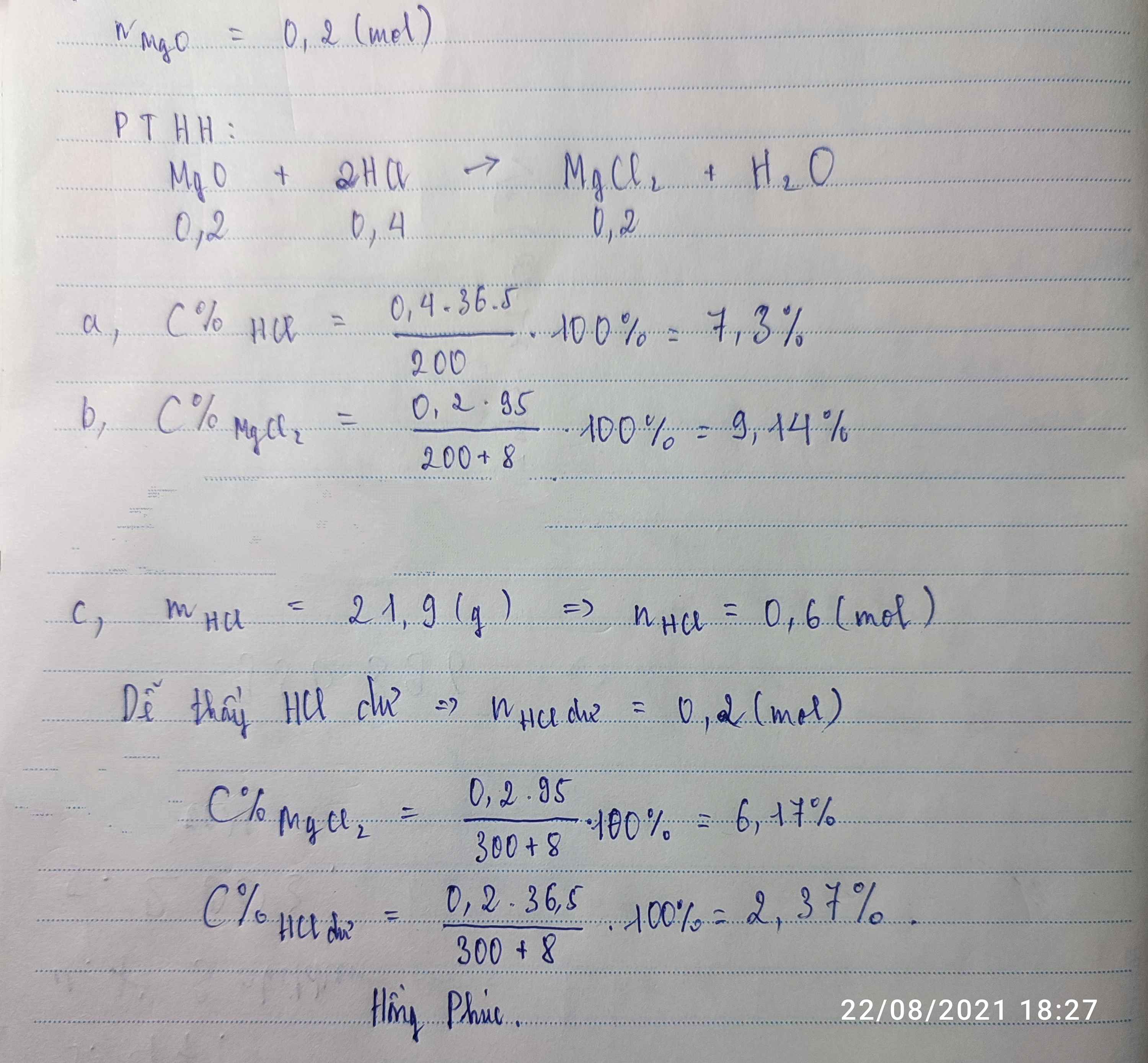Hòa tan hoàn toàn 40 g NaOH vào 98g dd H2SO4 . Tính C% của dung dịch sau phản ứng

Những câu hỏi liên quan
Hòa tan hoàn toàn 1,6 g CuO vào 300 gam dd H2SO4
. Tính nồng độ phần trăm dung dịch muối thu được sau phản ứng
\(n_{CuO}=\dfrac{1,6}{80}=0,02\left(mol\right)\)
Pt : \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O|\)
1 1 1 1
0,02 0,02
\(n_{CuSO4}=\dfrac{0,02.1}{1}=0,02\left(mol\right)\)
⇒ \(m_{CuSO4}=0,02,160=3,2\left(g\right)\)
\(m_{ddspu}=1,6+300=301,6\left(g\right)\)
\(C_{CuSO4}=\dfrac{3,2.100}{301,6}=1,6\)0/0
Chúc bạn học tốt
Đúng 2
Bình luận (1)
1. Hòa tan hoàn toàn 16,2(g) kẽm oxit trong 196(g) dung dịch H2SO4 12% sau phản ứng thu được dung dịch X. Tính C% các chất có trong dung dịch X?2. Hòa tan hoàn toàn 16(g) CuO trong 245(g) dung dịch H2SO4 12% sáu phản ứng thu được dung dịch A?3. Hòa tan 16(g) NaOH(rắn) vào nước được 200ml dung dịch NaOH có nồng độ a(M).a) Tìm a?b) Phải thêm vào dung dịch trên bao nhiêu ml nước để thu được dung dịch NaOH 0,5(M)
Đọc tiếp
1. Hòa tan hoàn toàn 16,2(g) kẽm oxit trong 196(g) dung dịch H2SO4 12% sau phản ứng thu được dung dịch X. Tính C% các chất có trong dung dịch X?
2. Hòa tan hoàn toàn 16(g) CuO trong 245(g) dung dịch H2SO4 12% sáu phản ứng thu được dung dịch A?
3. Hòa tan 16(g) NaOH(rắn) vào nước được 200ml dung dịch NaOH có nồng độ a(M).
a) Tìm a?
b) Phải thêm vào dung dịch trên bao nhiêu ml nước để thu được dung dịch NaOH 0,5(M)
2: Hòa tan hoàn toàn 8 (g) Fe2O3 vào 500 (g) dd HCl. Sau phản ứng thu được m (g) muối FeCl3.
a) Tính m?
b) Tính C% của chất có trong dung dịch sau phản ứng?
\(n_{Fe_2O_3}=\dfrac{8}{160}=0,05\left(mol\right)\\ Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\\ n_{FeCl_3}=2.0,05=0,1\left(mol\right)\\ a,m=m_{FeCl_3}=162,5.0,1=16,25\left(g\right)\\b,m_{ddFeCl_3}=8+500=508\left(g\right)\\ C\%_{ddFeCl_3}=\dfrac{16,25}{508}.100\approx 3,199\%\)
Đúng 3
Bình luận (0)
Nhỏ từ từ dung dịch NaOH 1 m vào 50 ml vào dung dịch H2SO4 khi H2SO4 được trung hòa hoàn toàn thì thấy dùng hết 40 ml dung dịch NaOH A viết BTHH của phản ứng Tính nồng độ dung dịch H2SO4 ban đầu Nêu cách nhận biết thời điểm H2SO4 trung hòa hoàn toàn
\(A.2NaOH+H_2SO_4\rightarrow Na_2SO_4+H_2O\\ n_{NaOH}=0,04.1=0,04mol\\ n_{H_2SO_4}=0,04:2=0,02mol\\ C_{M\left(H_2SO_4\right)}=\dfrac{0,02}{0,05}=0,4M\)
Cho quỳ tím vào dd \(H_2SO_4\) rồi nhỏ từ từ dd \(NaOH\) vào. Đến khi thấy quỳ tím từ màu đỏ trở về màu tím thì đó là thời điểm \(H_2SO_4\) được trung hoà hoàn toàn.
Đúng 4
Bình luận (2)
B1: Hòa tan hoàn toàn 2,3 (g) Na vào 200 (g) nước thu được dung dịch NaOH và V(l) khí H2 (đktc).
a) Tính V?
b) Tính C% của dung dịch thu được sau phản ứng?
c) Cho quỳ tím vào dung dịch thu được sau phản ứng thì quỳ tím chuyển màu gì?
a, \(2Na+2H_2O\rightarrow2NaOH+H_2\)
Ta có: \(n_{Na}=\dfrac{2,3}{23}=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{200}{18}=\dfrac{100}{9}\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1}{2}< \dfrac{\dfrac{100}{9}}{2}\), ta được H2O dư.
Theo PT: \(n_{H_2}=\dfrac{1}{2}n_{Na}=0,05\left(mol\right)\Rightarrow V_{H_2}=0,05.22,4=1,12\left(l\right)\)
b, Theo PT: \(n_{NaOH}=n_{Na}=0,1\left(mol\right)\)
Ta có: m dd sau pư = 2,3 + 100 - 0,05.2 = 102,2 (g)
\(\Rightarrow C\%_{NaOH}=\dfrac{0,1.40}{102,2}.100\%\approx3,91\%\)
c, - Dung dịch làm quỳ tím hóa xanh.
Đúng 0
Bình luận (2)
\(n_{Na}=\dfrac{2,3}{23}=0,1\left(mol\right)\\ 2Na+2H_2O\rightarrow2NaOH+H_2\\ n_{H_2}=\dfrac{0,1}{2}=0,05\left(mol\right);n_{NaOH}=n_{Na}=0,1\left(mol\right)\\ a,V=V_{H_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\\ b,m_{ddNaOH}=m_{Na}+m_{H_2O}-m_{H_2}=2,3+200-0,05.2=202,2\left(g\right)\\ C\%_{ddNaOH}=\dfrac{40.0,1}{202,2}.100\approx1,978\%\\ c,NaOH-Tính.bazo\Rightarrow Quỳ.tím.hoá.xanh\)
Đúng 1
Bình luận (0)
hoà tan hoàn toàn 10,2g một oxit kim loại có hoá trị 3 vào 100g dung dụng h2so4 vừa đủ sau khi phản ứng xảy ra hoàn toàn thu được 34,2 g muối sunfat a)xác định tên kim loại b) tính nồng độ % của dung dịch h2so4 c) tính thể tích dung dịch NaOH 1,5 M cần dùng để kết tủa hoàn toàn dung dịch muối trên
\(Đặt.oxit:A_2O_3\\ A_2O_3+3H_2SO_4\rightarrow A_2\left(SO_4\right)_3+3H_2O\\ n_{Al_2O_3}=\dfrac{34,2-10,2}{96.3-16.3}=0,1\left(mol\right)\\ M_{A_2O_3}=\dfrac{10,2}{0,1}=102\left(\dfrac{g}{mol}\right)=2M_A+48\\ \Rightarrow M_A=27\left(\dfrac{g}{mol}\right)\\ a,\Rightarrow A.là.nhôm\left(Al=27\right)\\ b,n_{H_2SO_4}=3.0,1=0,3\left(mol\right)\\ C\%_{ddH_2SO_4}=\dfrac{0,3.98}{100}.100=29,4\%\\ c,n_{Al_2\left(SO_4\right)_3}=n_{Al_2O_3}=0,1\left(mol\right)\\ Al_2\left(SO_4\right)_3+6NaOH\rightarrow2Al\left(OH\right)_3+3Na_2SO_4\\ n_{NaOH}=6.0,1=0,6\left(mol\right)\\ V_{ddNaOH}=\dfrac{0,6}{1,5}=0,4\left(l\right)\)
Đúng 3
Bình luận (0)
hòa tan hoàn toàn 26,2g hỗn hợp bột Al2O3 và Fe2O3 vào 120 g dung dịch HCL 36,5% đc dung dịch A.
a)Tính thành phần % theo khối lượng mỗi oxit trong hỗn hợp đầu.
b)(Al=27,O=16,Fe=56,H=1,S=32)
c)Cho dd a phản ứng với dd NaOH 0,75M.tính thể tích dd NaOH 0,75M tối thiểu để thu được lượng kết tủa không đổi (1,4 mol NaOH)
a,\(m_{HCl}=120.36,5\%=43,8\left(g\right)\Rightarrow n_{HCl}=\dfrac{43,8}{36,5}=1,2\left(mol\right)\)
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
Mol: x 6x
PTHH: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Mol: y 6y
Ta có:\(\left\{{}\begin{matrix}102x+160y=26,2\\6x+6y=1,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\%m_{Al_2O_3}=\dfrac{0,1.102.100\%}{26,2}=38,93\%;\%m_{Fe_2O_3}=100\%-38,93\%=61,07\%\)
câu c tương tự câu a
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.
Đọc tiếp
Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.
a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.
c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.
a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.
c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.
Hòa tan hoàn toàn a gam sắt vào dung dịch H2SO4 loãng thu được 4,48 lít khí. Mặt khác cũng hòa tan hết a gam sắt vào H2SO4 đặc nóng dư được V lít khí. Cho khí này phản ứng với dung dịch KMnO4 2M vừa đủ. Viết các phương trình phản ứng, tính V và V dd KMnO4 2M
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\) (1)
\(2Fe+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\) (2)
\(5SO_2+2KMnO_4+2H_2O\rightarrow2MnSO_4+K_2SO_4+2H_2SO_4\) (3)
Ta có: \(n_{H_2}=0,2\left(mol\right)\)
Theo PT (1): \(n_{Fe}=n_{H_2}=0,2\left(mol\right)\)
Theo PT (2): \(n_{SO_2}=\dfrac{3}{2}n_{Fe}=0,3\left(mol\right)\)
\(\Rightarrow V_{SO_2}=0,3.22,4=6,72\left(l\right)\)
Theo PT (3): \(n_{KMnO_4}=\dfrac{2}{5}n_{SO_2}=0,12\left(mol\right)\)
\(\Rightarrow V_{KMnO_4}=\dfrac{0,12}{2}=0,06\left(l\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)