Fe + 2HCl -> FeCl2 + H2
Nếu có 2,8 g sắt tham gia phản ứng, em hãy tìm:
a) Thể tích khí hidro thu được ở đktc.
b) Khối lượng axit clohidric cần dùng.
Sắt tác dụng axit clohiđric : Ta có phương trình hóa học sau : Fe + 2HCl → FeCl2 + H2
Nếu 1,4g Fe tham gia phản ứng hết với lượng dung dịch axít trên. Hãy tính :
a) Khối lượng axit Clohiđric cần dùng .(1,825g)
b) Thể tích khí H2 thu được đktc .(0,56 lít)
\(n_{Fe}=\dfrac{1.4}{56}=0.025\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.025.....0.05...............0.025\)
\(m_{HCl}=0.05\cdot36.5=1.825\left(g\right)\)
\(V_{H_2}=0.025\cdot22.4=0.56\left(l\right)\)
Sắt tác dụng với axit clohiđric : Fe + 2HCl → FeCl2 + H2↑.
Nếu có 2,8g sắt tham gia phản ứng em hãy tìm:
a) Thể tích khí hiđro thu được ở đktc.
b) Khối lượng axit clohiđric cần dùng.
a) PTPU

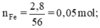
Theo pt: nH2 = nFe = 0,05 (mol)
VH2 = 22,4.n = 22,4.0,05 = 1,12 (l)
b) nHCl = 2.nFe = 2. 0,05 = 0,1 (mol)
mHCl = M.n = 0,1.36,5 = 3,65 (g)
a)
\(n_{Fe} = \dfrac{14}{56} = 0,25(mol)\)
Phương trình hóa học : \(Fe + H_2SO_4 \to FeSO_4 + H_2\)
Theo PTHH : \(n_{H_2} = n_{Fe} = 0,25(mol)\\ \Rightarrow V_{H_2} = 0,25.22,4 = 5,6(lít)\)
b)
Có : \(n_{H_2SO_4} = n_{H_2} = 0,25(mol)\\ \Rightarrow m_{H_2SO_4} = 0,25.98 = 24,5(gam)\)
cho sắt tác dụng với axit sunfuric loãng H2SO4: Fe + H2SO4 -> FeSO4 + H2. Nếu có 14g sắt tham gia phản ứng, em hãy tìm:a. thể tích khí hiđro thu được ở đktcb khối lượng Axit sunfuric cần dùng
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Ta có: \(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{H_2SO_4}=n_{Fe}=0,25\left(mol\right)\)
a, \(V_{H_2}=0,25.22,4=5,6\left(l\right)\)
b, \(m_{H_2SO_4}=0,25.98=24,5\left(g\right)\)
Bạn tham khảo nhé!
nFe = \(\dfrac{14}{56}\)= 0,25 mol
Fe + H2SO4 → FeSO4 + H2
Theo pt : 1 1 1 1 mol
Theo đề bài : 0,25 0,25 0,25 0,25 mol
=> V H2 = 0,25 . 22,4 = 5,6 lít
mH2SO4 = 0,25 . 98 = 24,5 gam
5/Cho sơ đồ phản ứng sau : Zn + HCl - - > ZnCl2 + H2
Nếu có 6,5 g Zn tham gia phản ứng, hãy tìm:
a) Thể tích khí H2 thu được ở điều kiện tiêu chuẩn.
b) Khối lượng axit HCl cần dùng .
c) Khối lượng ZnCl2 tạo thành sau phản ứng ( theo 2 cách)
\(nZn=\dfrac{6,5}{65}=0,1mol\)
PTHH:
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
0,1--->0,2------->0,2------>0,1
a, \(VH_2=0,1.22,4=2,24lít\)
b, \(mHCl=0,2.36,5=3,65g\)
c, cách 1:
\(mZnCl_2=0,2.136=27,2gam\)
cách 2 :
\(mH_2=0,1.2=0,2gam\)
BTKL: mZn+mHCl=mZnCl2+H2
6,5+3,65 =mZnCl2+0,2
sao cái cách 2 btkl mình cs tính kq mà s nhìn nó lạ lắm
5/
a) \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2
0,1 0,2 0,1 0,1
\(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
b) \(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
c) \(m_{ZnCl_2}=0,1.136=13,6\left(g\right)\)
sắt tác dụng với axit clohidric HCL theo sơ đồ phản ứng sau fe + HCL ---> FeCl2 +H2
nếu có 11,2 gam sắt tham gia phản ứng Hãy tính
a. khối lượng axit chohidric HCL cần dùng
b. thể tích khí hidro tạo thành ở đktc
( cho biết Fe = 56 ; Zn = 65 ; S=32; O = 16 ; K= 39; H=1 ; C=12; CL=35)
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
_____0,2_____0,4__________0,2 (mol)
a, \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
b, \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
Sắt tác dụng với axit clohiđric theo PTHH:
Fe + 2HCl -> FeCl2 + H2
Nếu có 2,8g Fe tham gia phản ứng, khối lượng khí H2 thu được là:
A. 0,3g H2
B. 0,2g H2
C. 1,0 g H2
D. 0,1g H2
\(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Fe}=0,05\left(mol\right)\)
\(\Rightarrow m_{H_2}=0,05.2=0,1\left(g\right)\)
Chọn D
Sắt tác dụng với axit clohiđric:
Fe + 2HCl → FeCl2 + H2.
Nếu có 2,8 g sắt tham gia phản ứng, em hãy tìm:
a) Thể tích khí hiđro thu được ở đktc.
b) Khối lượng axit clohiđric cần dùng.
Số mol sắt tham gia phản ứng:
nFe = 0,05 mol
a) Thể tích khí hiđro thu được ở đktc:
Fe + 2HCl → FeCl2 + H2.
Theo phương trình hóa học, ta có: = nFe = 0,05 mol
Thể tích khí thu được ở đktc là: = 22,4 . n = 22,4 . 0,05 = 1,12 lít
b) Khối lượng axit clohiđric cần dùng
Theo phương trình hóa học, ta có:
nHCl = 2nFe = 2 . 0,05 = 0,1 mol
Khối lượng HCl cần dùng là: mHCl = M . n = 0,1 . 36,5 = 3,65 g
a) nFe = 2,8 / 56 = 0,05 mo
l Phương trình hoá học:
Fe + 2HCl -----> FeCl2 + H2
0, 05 mol 2.0,05 mol 0,05 mol
Theo phương trình trên ta có
nFe = nH = 0,05 VH2= 0,05 x 22,4 = 1,12 l.
b) nHCl = 2nFe = 2 x 0,05 = 0,1 mol
mHCl cần dùng: 0,1 x 36,5 = 3,65 g.
Sắt tác dung với axit clohidric:
Ta có phương trình hóa học sau : Fe + 2HCl -----> \(FeCl_2+H_2\)
Nếu 1,4g Fe tham gia phản ứng hết với lượng dung dịch axit trên.
Hãy tính:
a,Khối lượng axit clohidric cần dùng.
b,Thể tích khí \(H_2\) thu được ở đktc.(0,56 lít)
![]()
a)
\(n_{Fe} = \dfrac{1,4}{56} = 0,025(mol)\)
Theo PTHH : \(n_{HCl} = 2n_{Fe} = 0,05(mol)\\ \Rightarrow m_{HCl} = 0,05.36,5 = 1,825(gam)\)
b)
Ta có :
\(n_{H_2} = n_{Fe} = 0,025(mol)\\ \Rightarrow V_{H_2} = 0,025.22,4 = 0,56(lít)\)