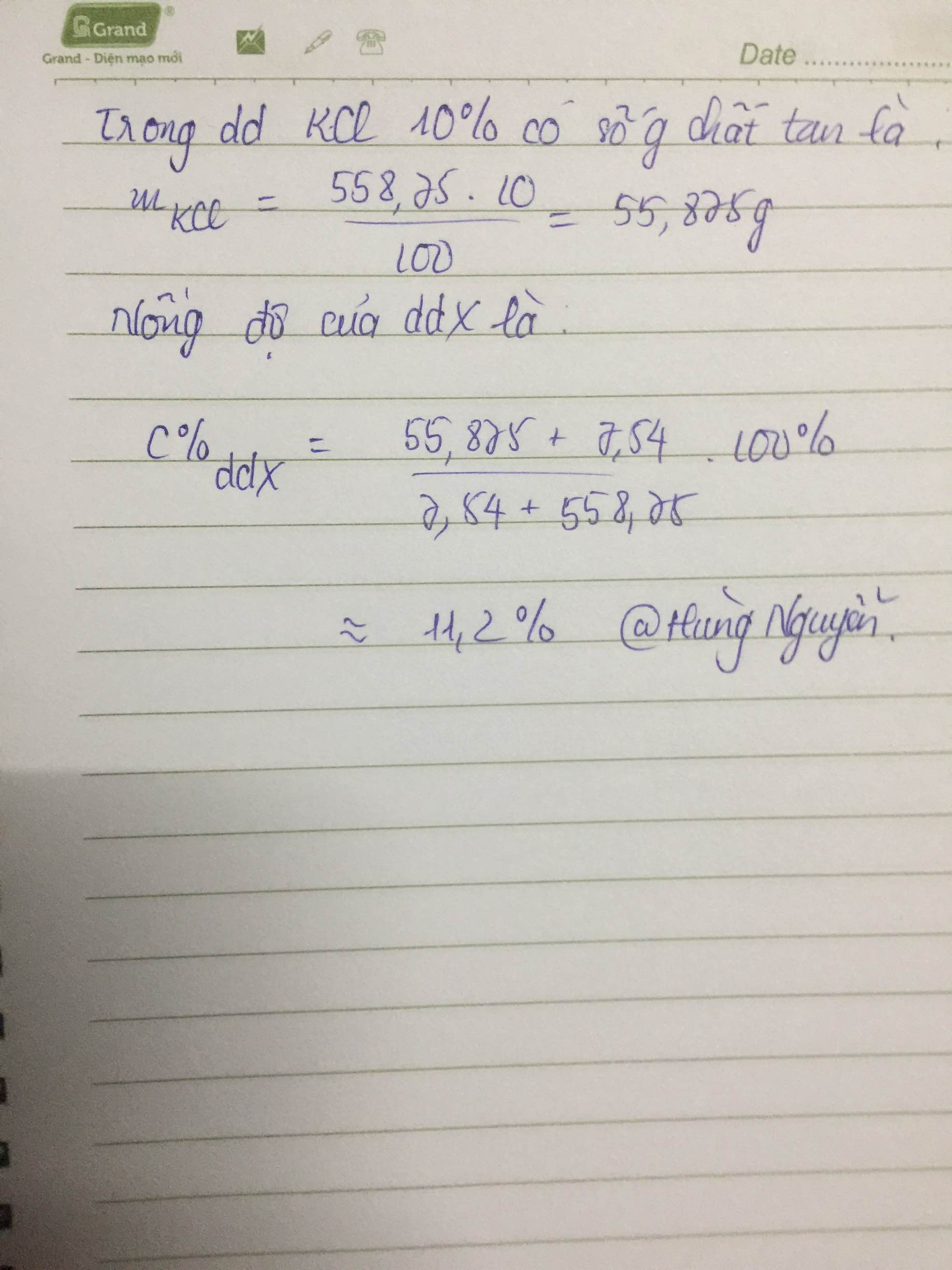đem trộn 3 dd KCl : dd(1) ; dd(2) ; dd(3) có nồng độ 0,4M ; 0,8M ; 2M với thể tích dung dịch lần lượt là 400ml; 300ml; 100ml thì thu được dd KCl mới có nồng độ mấy M?

Những câu hỏi liên quan
Trộn 200ml dd H2,So4,O2.M vào 400ml dd H2,So4 0,1M.Thu đuoc dd có nồng độ là bao nhiêu sau khi pha trộn.
Ta có: \(n_{H_2SO_4\left(0,2M\right)}=0,2.0,2=0,04\left(mol\right)\)
\(n_{H_2SO_4\left(0,1M\right)}=0,4.0,1=0,04\left(mol\right)\)
\(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,04+0,04}{0,2+0,4}=\dfrac{2}{15}\left(M\right)\)
Đúng 2
Bình luận (0)
\(n_{H_2SO_4\left(sau\right)}=0,2.2+0,4.0,1=0,08mol\\ V_{H_2SO_4\left(sau\right)}=0,4+0,2=0,6l\\ C_{M\left(H_2SO_4\right)}=\dfrac{0,08}{0,6}=0,13M\)
Đúng 0
Bình luận (0)
trộn 100ml dd hcl 0,05m với 100ml ddnaoh0.07m,tính ph của dd sau phản ứng
\(n_{HCl}=0,1\cdot0,05=0,005mol\)
\(n_{NaOH}=0,1\cdot0,07=0,007mol\)
\(H^+\) + \(OH^-\) \(\rightarrow\) \(H_2O\)
0,005 0,007
0,005 0,005 0,005
0 0,002 0,005
\(\Rightarrow OH^-\) dư và dư \(0,002mol\)
\(\Rightarrow C_M=\dfrac{0,002}{0,1+0,1}=0,01M\)
\(\Rightarrow pH=-log\left(\dfrac{10^{-14}}{0,01}\right)=12\)
Đúng 1
Bình luận (0)
Có 3 bình đựng dd KOH nồng độ 1M,2M,3M,mỗi bình chứa một lít dd.Hãy trộn các dd này như thế nào để thu được dd KOH 1,8M có thể tích lớn nhất
Để được như vậy thì phải có chắc chắc 1l 1M. Giả sử cho tiếp 1 lít 2M thì Cm lúc này mới là 1,5M. Gọi x là lít 3M.
Ta có: 3 + 3x = 1,8(2 + x) --> x = 0,5.
Vậy: 1l 1M, 1l 2M, 0,5l 3M.
Đúng 0
Bình luận (1)
1)Cần bao nhiêu gam dd NaCl 20% pha với 400g dd NaCl 15% để đc dd NaCl 16%
2) Cần pha thêm bao nhiêu lít nước vào 400 ml dd NaOH 3M để đc dd NaOH 1,2 M
3) Trộn 300g dd KCl 4% với 200g dd KCl 10%. Tính nồng độ % của dd thu dc
1)Cần bao nhiêu gam dd NaCl 20% pha với 400g dd NaCl 15% để đc dd NaCl 16%
2) Cần pha thêm bao nhiêu lít nước vào 400 ml dd NaOH 3M để đc dd NaOH 1,2 M
3) Trộn 300g dd KCl 4% với 200g dd KCl 10%. Tính nồng độ % của dd thu dc
Xem thêm câu trả lời
Hòa tan hoàn toàn 7,45g KCl vào 558,75g dd KCl 10% thu được dd X. Tính nồng độ % của dd X
a)cần thêm bao nhiêu gam KCl vào 200g dd KCl 10% để được dd KCl 15%
b)cần thêm bao nhiêu ml Hl vào 100 ml dd HCl 1M để thu đc HCl 1,5M
a)
Gọi m KCl = a(gam)
Sau khi thêm :
m KCl = a + 200.10% = a + 20(gam)
m dd = a + 200(gam)
Suy ra :
C% = (a + 20) / (a +200) .100% = 15%
=> a = 11,76(gam)
b)
(Thiếu dữ kiện)
Đúng 3
Bình luận (0)
Hòa tan hoàn toàn 24.625g hh gồm KCl, MgCl2, NaCl vào nước, rồi thêm vào đó 300ml dd AgNO3 1.5M. Sau PỨ thu được dd A, kết tủa B. Cho Cho 2.4g Mg vào dd A, PỨ kết thúc lọc tách riêng chất rắn C và dd D. Cho toàn bộ chất rắn vào dd HCl loãng dư, sau PỨ thấy khối lượng chất rắn C giảm 1.92g. Thêm dd NaOH dư vào dd D, lọc lấy kết tủa đem nung đến khối lượng không đổi được 4g chất rắn E. Tính %m các muối có trong hh đầu.
Đọc tiếp
Hòa tan hoàn toàn 24.625g hh gồm KCl, MgCl2, NaCl vào nước, rồi thêm vào đó 300ml dd AgNO3 1.5M. Sau PỨ thu được dd A, kết tủa B. Cho Cho 2.4g Mg vào dd A, PỨ kết thúc lọc tách riêng chất rắn C và dd D. Cho toàn bộ chất rắn vào dd HCl loãng dư, sau PỨ thấy khối lượng chất rắn C giảm 1.92g. Thêm dd NaOH dư vào dd D, lọc lấy kết tủa đem nung đến khối lượng không đổi được 4g chất rắn E. Tính %m các muối có trong hh đầu.
Trong dd ban đầu:
K+_____a mol
Mg2+___b mol
Na+____c mol
Cl-_____a + 2b + c mol
mhhbđ = 74.5a + 95b + 58.5c = 24.625 g______(1)
nAgNO3 = 0.3*1.5 = 0.45 mol
Cho Mg vào A có phản ứng (theo gt) nên Ag(+) còn dư, Cl(-) hết. Rắn C gồm Ag và có thể cả Mg còn dư nữa. Thật vậy, khi cho rắn C vào HCl loãng thì khối lượng rắn bị giảm đi, chính do Mg pư, Ag thì không. Vậy mrắn C giảm = mMg chưa pư với A = 1.92 g.
=> nMg dư = 1.92/24 = 0.08 mol
=> nMg pư với A = 2.4/24 - 0.08 = 0.02 mol________(*)
Khi cho Mg vào A có pư:
Mg + 2Ag(+) ---> 2Ag(r) + Mg(2+)
0.02__0.04
=> nAg(+) pư với dd ban đầu = 0.45 - 0.04 = 0.41 mol
Ag(+) + Cl(-) ---> AgCl(r)
0.41___0.41
Có: nCl(-) = a + 2b + c = 0.41_____________(2)
Trong các cation trên, Mg(2+) và Ag(+) có pư với OH(-), tuy nhiên trong D chỉ có Mg(2+) nên kết tủa là Mg(OH)2:
Mg(2+) + 2OH(-) ---> Mg(OH)2
Khi nung:
Mg(OH)2 ---> MgO + H2O
Ta có: nMg(2+)trongD = nMgO = 4/40 = 0.1 mol
Trong đó 0.02 mol Mg(2+) được thêm vào bằng cách cho kim loại Mg vào (theo (*)), vậy còn lại 0.08 mol Mg(2+) là thêm từ đầu, ta có:
b = 0.08 mol_________________________(3)
(1), (2), (3) => a = 0.15, b = 0.08, c = 0.1
mKCl = 74.5*0.15 = 11.175 g
mMgCl2 = 95*0.08 = 7.6 g
mNaCl = 58.5*0.1 = 5.85 g
Đúng 0
Bình luận (0)
Hãy tính nồng độ phần trăm của dd KCL .Khi cho 20g KCL trong 600g dd
\(C\%_{KCl}=\dfrac{20}{600}.100\%=3,33\%\)
Đúng 3
Bình luận (0)