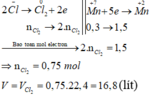HCl+KMnO4→Cl2+MnO2+KCl+H2O
tính thể tích khí clo (đktc) thu được 31,6g KMnO4 với HCl đặc dư với hiệu suất phản ứng 80%
Cho 60 g dd HCl 36,5% phản ứng với 31,6 g KMnO4 với hiệu suất phản ứng đạt 80%. Tính thể tích khí clo thu được ở đktc.
PT: \(2KMnO_4+16HCl\rightarrow2MnCl_2+2KCl+5Cl_2+8H_2O\)
Ta có: \(n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(mol\right)\)
\(m_{HCl}=\dfrac{60.36,5}{100}=21,9\left(g\right)\Rightarrow n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{2}>\dfrac{0,6}{16}\), ta được KMnO4 dư.
Theo PT: \(n_{Cl_2\left(LT\right)}=\dfrac{5}{16}n_{HCl}=0,1875\left(mol\right)\)
Mà: H% = 80%
\(\Rightarrow n_{Cl_2\left(TT\right)}=0,1875.80\%=0,15\left(mol\right)\)
\(\Rightarrow V_{Cl_2}=0,15.22,4=3,36\left(l\right)\)
Bạn tham khảo nhé!
Kmno4+ HCl —> kcl + MnCl + Cl + H2O Giả sử hiệu suất phản ứng là 80% . Tính khối lượng của KMnO4 cần dùng để thu được 2,479 lít Cl2 (đktc) (1mol chất khí —> 24,79 lít)
\(n_{Cl_2}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\)
PTHH: \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
0,04<-----------------------------------------------0,1
\(\Rightarrow n_{KMnO_4\left(c\text{ần}.d\text{ùng}\right)}=\dfrac{0,04}{80\%}=0,05\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=0,05.158=7,9\left(g\right)\)
PT: \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
Ta có: \(n_{Cl_2}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\)
Theo PT: \(n_{KMnO_4\left(LT\right)}=\dfrac{2}{5}n_{Cl_2}=0,04\left(mol\right)\)
Mà: H% = 80% \(\Rightarrow n_{KMnO_4\left(TT\right)}=\dfrac{0,04}{80\%}=0,05\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=0,05.158=7,9\left(g\right)\)
Cho 47,4g KMnO4 phản ứng với dd chứa (2,5 mol HCl đặc) thu được V lít khí Cl2 (đktc). Biết hiệu suất phản ứng là 80%. Giá trị của V là (Mn=55, K=39):
\(n_{KMnO_4}=\dfrac{m_{KMnO_4}}{M_{KMnO_4}}=\dfrac{47,4}{158}=0,3mol\)
\(n_{KMnO_4}=\dfrac{0,3}{80\%}=0,375mol\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
2 16 2 2 5 8 ( mol )
0,375 > 2,5 ( mol )
0,375 0,9375 ( mol )
\(V_{Cl_2}=n_{Cl_2}.22,4=0,9375.22,4=21l\)
\(n_{KMnO_4\left(bd\right)}=\dfrac{47,4}{158}=0,3\left(mol\right)\) => \(n_{KMnO_4\left(pư\right)}=\dfrac{0,3.80}{100}=0,24\left(mol\right)\)
PTHH: 2KMnO4 + 16HCl --> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,24------------------------------------->0,6
=> \(V=0,6.22,4=13,44\left(l\right)\)
1) Cho 39,15 gam MnO2 tác dụng với dd HCl đặc, khí sinh ra cho tác dụng với một lượng sắt dư thì thu được bao nhiêu gam muối. Biết hiệu suất của cả quá trình là 86%.
2) để điều chế được đủ lượng khí Clo tác dụng vừa đủ với 14,4 gam Mg thì người ta cần dùng bao nhiêu gam KMnO4. Biết hiệu suất phản ứng điều chế cho Clo là 80%.
3) Người ta có thể điều chế được bao nhiêu lít khi Clo (đktc) từ 63,2 gam KMnO4. Biết hiệu suất phản ứng là 75%.
4) Cho 13,05 gam MnO2 tác dụng với dd HCl đặc dư thì thu được 8,52 gam khí Clo. Tính hiệu suất cảu phản ứng.
5) Đun nóng 6,125 gam KClO3 với HCl đặc. Biết hiệu suất phản ứng là 85%. Thể tích Cl2 thu được ở ĐKTC là bao nhiêu.
6) Có 12 litts hỗn hợp 2 khí Cl2 và H2 đựng trong bình thạch anh đậy kín. Chiếu sáng để phản ứng sảy ra thì thu được một hỗn hợp khí chứa 30% thể tích là khí sản phẩm, lượng Cl2 còn lại 20% so với ban đầu (các thể tích khí đo ở cùng nhiệt độ và áp suất)
a) Tính % thể tích của hỗn hợp trước và sau phản ứng.
b) Tính hiệu suất phản ứng.
MnO\(_2\)+4HCl\(\rightarrow\)MnCl\(_2\)+Cl\(_2\)+2H\(_2O\)
0,45 0,45 (mol)
n\(_{MnO_2}\)=\(\dfrac{39,15}{87}\)=0,45(mol)
2Fe + 3Cl\(_2\)\(\rightarrow\)2FeCl\(_3\)
0,3 0,45 0,3 (mol)
m\(_{FeCl_3}\)=0,3.162,5=48,75(g)
vì hiệu suất phản ứng là 86% nên:
m\(_{FeCl_3}\)=\(\dfrac{86.48,75}{100}\)=41,925(g)
2/
Mg+Cl\(_2\)\(\rightarrow\)MnCl\(_2\)
0,6 0,6
n\(_{Mg}\)=\(\dfrac{14,4}{24}\)=0,6(mol)
2\(KMnO_4+16HCl\rightarrow2MnCl_2+2KCl+5Cl_2\uparrow+8H_2O\)
0,24 0,6
vì hiệu suất phản ứng bằng 80%,nên để điều chế 0,6 mol Cl\(_2\)thì cần số mol \(KMnO_4\) là:
n\(_{KMnO_4}\)=\(\dfrac{0,24.100}{80}\)=0,3(mol)
m\(KMnO_4\)=0,3.158=47,4(g)
3/
2KMnO4+16HCl→2MnCl2+2KCl+5Cl2↑+8H2O
0,4 1 (mol)
n\(_{KMnO_4}\)=\(\dfrac{63,2}{158}\)=0,4(mol)
V\(_{Cl_2}\)=1.22,4=22,4(l)
vì Hiệu suất phản ứng là 75% nên:
V\(_{Cl_2}\)=\(\dfrac{75.22,4}{100}\)=16,8(l)
Tính hiệu suất của phản ứng điều chế khí clo khi cho 17,4g Mno2 tác dụng với Hcl đặc dư thì thu được 3,584 lít khí clo (đktc).giúp mình với
\(n_{MnO_2}=\dfrac{17,4}{87}=0,2\left(mol\right)\\ PTHH:MnO_2+4HCl_{đặc,nóng}\rightarrow MnCl_2+Cl_2+2H_2O\\ n_{Cl_2\left(TT\right)}=\dfrac{3,584}{22,4}=0,16\left(mol\right)\\ n_{Cl_2\left(LT\right)}=n_{MnO_2}=0,2\left(mol\right)\\ \Rightarrow H=\dfrac{n_{Cl_2\left(TT\right)}}{n_{Cl_2\left(LT\right)}}.100\%=\dfrac{0,16}{0,2}.100=80\%\)
Bài 8. a) Cho 200ml dung dịch HCl 2M tác dụng với lượng dư KMnO4 thu được dung dịch A, V1 lít khí Cl2 (đktc). b) Cho 200ml dung dịch HCl 2M tác dụng với lượng dư MnO2 thu được dung dịch B, V2 lít khí Cl2 (đktc). - Viết PTHH của phản ứng xảy ra. - Tính thể tích khí Cl2 thu được (V1, V2). Mọi người giúp mình với ạ mình thật sự rất cần
- PT: a, \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\) (1)
\(MnO_2+4HCl_đ\underrightarrow{t^o}MnCl_2+Cl_2+2H_2O\) (2)
- Ta có: \(n_{HCl\left(1\right)}=n_{HCl\left(2\right)}=0,2.2=0,4\left(mol\right)\)
Theo PT (1): \(n_{Cl_2}=\dfrac{5}{16}n_{HCl\left(1\right)}=0,125\left(mol\right)\Rightarrow V_1=0,125.22,4=2,8\left(l\right)\)
(2): \(n_{Cl_2\left(2\right)}=\dfrac{1}{4}n_{HCl\left(2\right)}=0,1\left(mol\right)\Rightarrow V_2=0,1.22,4=2,24\left(l\right)\)
14. Thể tích khí Clo(đktc) thứ đc khi cho dung dịch đặc chứa 21,9g HCl tác dụng hết với KMnO4 là?
17. Hòa tan 23,7g Kmno4 vào dung dịch HCl đặc dư thì thu đc V lít khí Clo (đktc) . Biết rằng phản ứng xảy ra hoàn toàn , giá trị V là?
24. Cho 12,5g MnO2 ( có chứa 30,4% tạp chất trơ) , tác dụng với HCl đặc dư sinh ra V lít khí Clo(đktc). Biết hiệu suất phản ứng là 85%. V có giá trị là?
bài 17
nKMnO4=23,7\158=0,15 mol
| 16HCl | + | 2KMnO4 | → | 5Cl2 | + | 8H2O | + | 2KCl | + | 2MnCl2 |
2KMnO4 + 16HCl = 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,6 ----------------------- 0,1875 mol
nHCl=21,9\36,5=0,6 mol
=>VCl2=0,1875.22,4=4,2 l
\(\left(1\right)\) \(n_{HCl}=\frac{21,9}{36,5}=0,6\left(mol\right)\)
\(PTHH:2KMnO_4+16HCl_{\left(\text{đ}\right)}\underrightarrow{t^o}2KCl+2MnCl_2+5Cl_2+8H_2O\)
(mol)________________0,6__________________________3/16___________
\(V_{Cl_2}=22,4.\frac{3}{16}=4,2\left(l\right)\)
\(\left(2\right)\) \(n_{KMnO_4}=\frac{23,7}{158}=0,15\left(mol\right)\)
\(PTHH:2KMnO_4+16HCl_{\left(\text{đ}\right)}\underrightarrow{t^o}2KCl+2MnCl_2+5Cl_2+8H_2O\)
(mol)_______0,15________________________________0,375____________
\(V_{Cl_2}=22,4.0,375=8,4\left(l\right)\)
1/ Tính khối lượng khí Clo thu đc khi cho 174g MnO2 hoa tan hoàn toàn vào HCL đã nóng , biết hiệu suất phản ứng là 70%.
2/ Cho dd air HCL đảm đặc vào 31,6g KMnO4 thu đc 8,96 lít Cl2 ở dktc . Tình hiệu suất phản ứng.
3/ Cho 13,6 g hơn hợp X gỗ Để và Fe2O3 tác dụng vừa đủ với 91,25 g dd HCL 20% . Tính % khối lượng từng chất trong X
1. Ta có:
\(n_{MgO2}=\frac{174}{87}=2\left(mol\right)\)
\(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
Mà H = 70%
\(\Rightarrow n_{Cl2}=70\%.2=1,4\left(mol\right)\)
\(\Rightarrow m_{Cl2}=1,4.71=99,1\left(g\right)\)
2. \(PTHH:2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
Ta có:
\(n_{Cl2}=\frac{8,96}{22,4}=0,4\left(mol\right)\)
\(n_{KMnO4}=\frac{2}{5}n_{Cl2}=0,16\left(mol\right)\)
\(\Rightarrow m_{KMnO4}=0,16.158=25,28\left(g\right)\)
\(\Rightarrow H=\frac{25,28}{31,6}.100\%=80\%\)
3.
\(n_{HCl}=\frac{91,25.20\%}{36,5}=0,5\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{Fe}:a\left(mol\right)\\n_{Fe2O3}:b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow56a+160b=13,6\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
a____2a_____________
\(Fe_3O_4+6HCl\rightarrow2FeCl_3+3H_2O\)
b________6b________________
\(\Rightarrow2a+6b=0,5\)
\(\Rightarrow\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\frac{0,1.56}{13,6}=41,18\%\\\%m_{Fe3O4}=100\%-41,18\%=58,82\%\end{matrix}\right.\)
Cho 47,4 gam KMnO 4 phản ứng hết với dung dịch HCl đặc dư thu được V lít khí Cl 2 (đktc). Giá trị của V là
A. 33,6.
B. 2,69.
C. 6,72.
D. 16,80.
Đáp án D
Số mol KMnO 4 là
![]()
Sơ đồ phản ứng:
K Mn + 7 O 4 ⏟ 0 , 3 mol + H Cl - 1 → Mn + 2 Cl 2 + Cl 2 ⏟ V lit 0 + KCl + H 2 O
Các quá trình nhường, nhận electron: