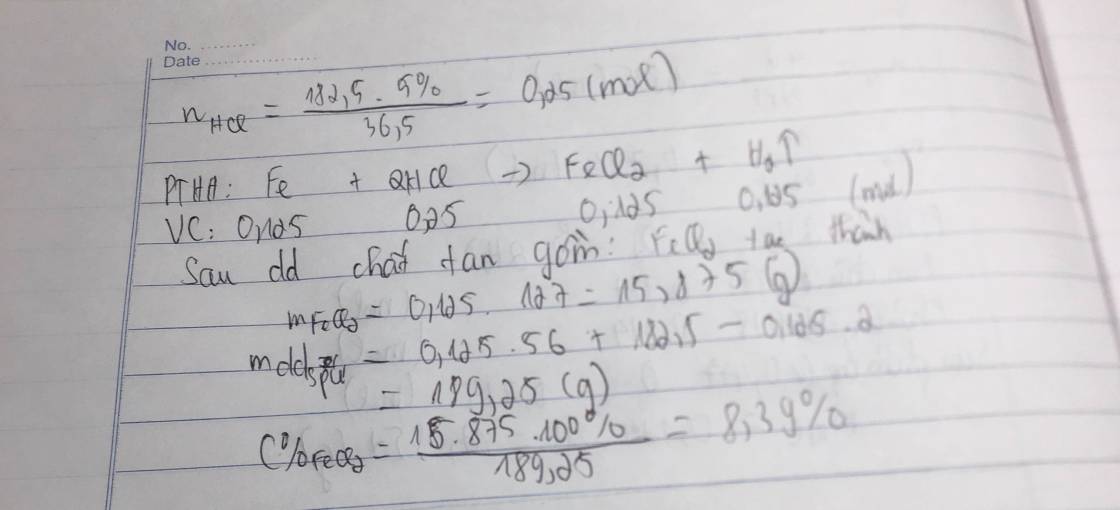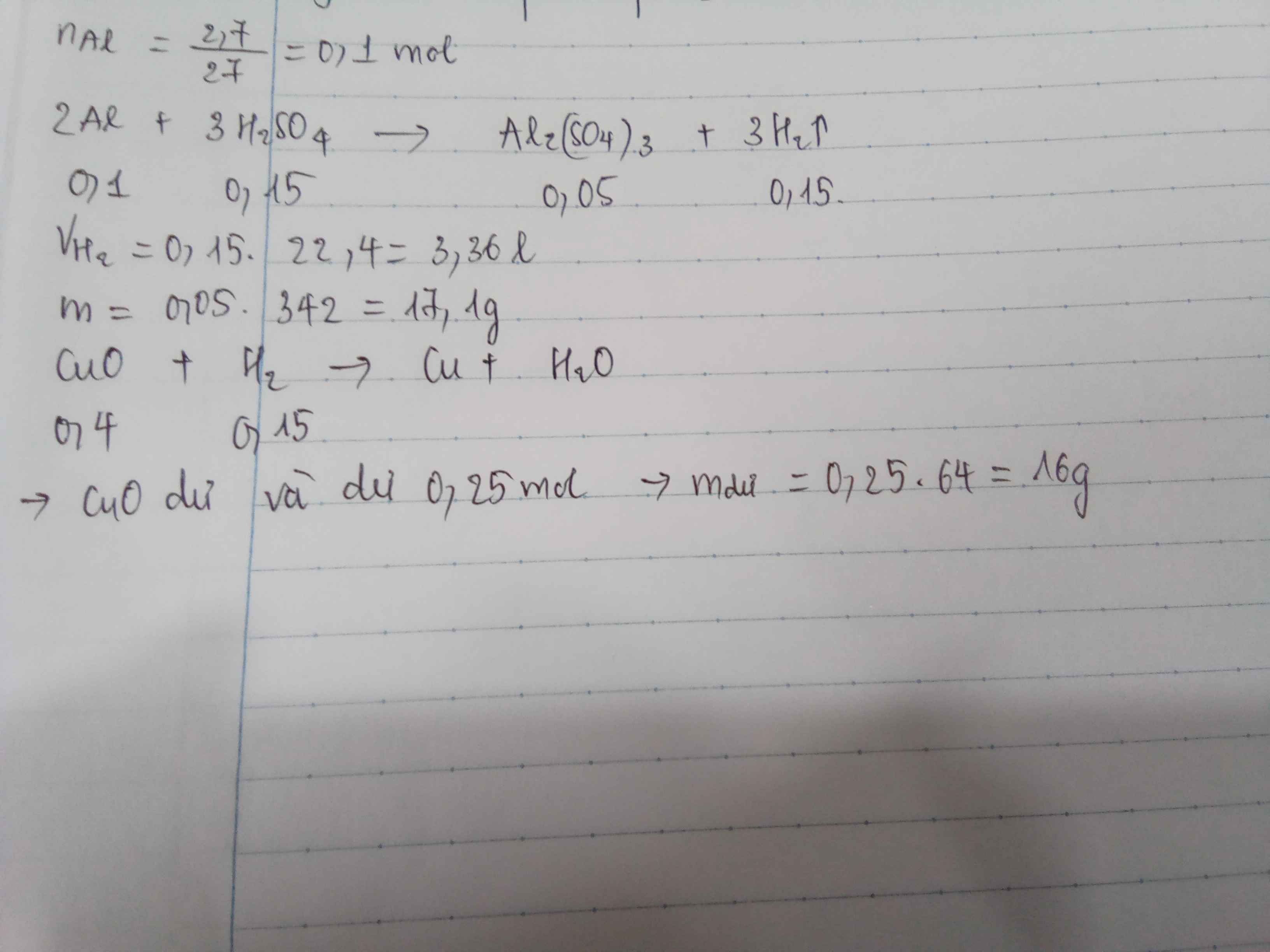Cho 0,65 gam Zn phan ung hết với 200 gam dung dịch HCl thì thu được m gam muối và v lít khí ở điều kiện tiêu chuẩn. a) Viết phương trình phản ứng xảy ra. B) Tính m, V c )Tính nồng độ phần trăm của dung dịch HCl đã dùng

Những câu hỏi liên quan
Cho m gam sắt vào 200 gam dung dịch HCL 71% thu được v1 lít khí ở điều kiện tiêu chuẩn
Viết phương trình hóa học
Tính m
Tính V
Tính c phần trăm dung dịch muối sau phản ứng
Xem chi tiết
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Ta có: \(n_{HCl}=\dfrac{200\cdot71\%}{36,5}=\dfrac{284}{73}\left(mol\right)\)
\(\Rightarrow n_{Fe}=n_{FeCl_2}=n_{H_2}=\dfrac{142}{73}\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=\dfrac{142}{73}\cdot56\approx108,93\left(g\right)\\m_{FeCl_2}=\dfrac{142}{73}\cdot127\approx247,04\left(g\right)\\m_{H_2}=\dfrac{142}{73}\cdot2\approx3,89\left(g\right)\\V_{H_2}=\dfrac{142}{73}\cdot22,4\approx43,57\left(l\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd}=m_{Fe}+m_{ddHCl}-m_{H_2}=305,04\left(g\right)\)
\(\Rightarrow C\%_{FeCl_2}=\dfrac{247,04}{305,04}\cdot100\%\approx80,99\%\)
Đúng 1
Bình luận (0)
Fe + 2HCl ➝ FeCl2 + H2
mHCl = 200.71% = 142 (g) => nHCl = \(\dfrac{284}{73}\) (mol)
nFe = \(\dfrac{1}{2}\) nHCl = \(\dfrac{142}{73}\) (mol) => m ≃ 108,9 (g)
nH2 = nFe => V ≃ 43,57 (l)
nFeCl2 = nFe => C% ≃ 80%
(Mk nghĩ bạn nên kiểm tra lại đề vì số liệu không được đẹp cho lắm)
Đúng 1
Bình luận (1)
1. Cho m gam Magie phản ứng với 100 gam dung dịch HCl dư sau phản ứng thu được dung dịch y và 11,2 l khí H2 ở điều kiện tiêu chuẩn a Viết phương trình phản ứng và Tính m b Tính nồng độ phần trăm (C%)của muối có trong dung dịch Y 2. Chỉ dùng một thuốc thử phân biệt các chất sau: Na2CO3 BaCl2 NaNO3
(1)
$n_{H_2} = \dfrac{11,2}{22,4} = 0,5(mol)$
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,5 1 0,5 0,5 (mol)
Sau phản ứng : $m_{dd} = 0,5.24 + 100 - 0,5.2 = 111(gam)$
$C\%_{MgCl_2} = \dfrac{0,5.95}{111}.100\% = 42,79\%$
(2)
Trích mẫu thử
Cho dung dịch $H_2SO_4$ tới dư vào mẫu thử :
- mẫu thử tạo khí không màu là $Na_2CO_3$
$Na_2CO_3 + H_2SO_4 \to Na_2SO_4 + CO_2 + H_2O$
- mẫu thử tạo kết tủa trắng là $BaCl_2$
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
- mẫu thử không hiện tượng là $NaNO_3$
Đúng 2
Bình luận (0)
cho 20g hỗn hợp gồm Zn và ZnO tác dụng hết với 100 gam dung dịch HCL thu được 2,24 lít khí ở điều kiện tiêu chuẩn a) viết phương trình hóa học. Tính phần trăm khối lượng mỗi chất trong hỗn hợp. b) Tính nồng độ phần trăm dung dịch muối thu được sau phản ứng. c) nếu cho hỗn hợp tác dụng với H2 SO4 đặc nóng thì thu được bao nhiêu lít khí ở điều kiện tiêu chuẩn.
a) PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
\(ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
b) Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)=n_{Zn}\) \(\Rightarrow n_{ZnO}=\dfrac{20-0,1\cdot65}{81}=\dfrac{1}{6}\left(mol\right)\)
\(\Rightarrow n_{ZnCl_2}=n_{Zn}+n_{ZnO}=\dfrac{4}{15}\left(mol\right)\)
Mặt khác: \(m_{H_2}=0,1\cdot2=0,2\left(g\right)\)
\(\Rightarrow m_{dd}=m_{hh}+m_{ddHCl}-m_{H_2}=119,8\left(g\right)\) \(\Rightarrow C\%_{ZnCl_2}=\dfrac{\dfrac{4}{15}\cdot136}{119,8}\cdot100\%\approx30,27\%\)
c) Giả sử khí là SO2
PTHH: \(Zn+H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}ZnSO_4+SO_2\uparrow+H_2O\)
Theo PTHH: \(n_{SO_2}=n_{Zn}=0,1\left(mol\right)\) \(\Rightarrow V_{SO_2}=0,1\cdot22,4=2,24\left(l\right)\)
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn 7,2 gam magiê vào 300ml dụng dịch HCL thu được V lít H2 ở điều kiện tiêu chuẩn A / viết phương trình phản ứng hóa học xảy ra B/ tính V h2 sinh ra ở điều kiện tiêu chuẩn C/ tính nồng độ mol dung dịch HCL đã dùng
`a)PTHH:`
`Mg + 2HCl -> MgCl_2 + H_2`
`0,3` `0,6` `0,3` `0,3` `(mol)`
`b) n_[Mg] = [ 7,2 ] / 24 = 0,3 (mol)`
`=> V_[H_2] = 0,2 . 22,4 =6,72 (l)`
`c) C_[M_[HCl]] = [ 0,6 ] / [ 0,3 ] = 2 (M)`
Đúng 3
Bình luận (0)
Cho bột nhôm và 300 gam dung dịch axit clohiđric sau phản ứng thu được 26,7 gam muối nhôm clorua và khí h2 thoát ra ngoài a viết phương trình hóa học b tính thể tích khí hidro được sinh ra ở điều kiện tiêu chuẩn c tính nồng độ phần trăm của dung dịch axit clohiđric phản ứng
\(n_{AlCl_3}=\dfrac{26.7}{133.5}=0.2\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(.........0.6......0.2.......0.3\)
\(V_{H_2}=0.3\cdot22.4=6.72\left(l\right)\)
\(C\%HCl=\dfrac{0.6\cdot36.5}{300}\cdot100\%=7.3\%\)
Đúng 1
Bình luận (0)
Cho 10,8 gam nhôm tác dụng hết với 200 gam dung dịch HCl Hãy cho biết thể tích khí H2 sinh ra ở điều kiện tiêu chuẩn Tính khối lượng muối tạo thành tính nồng độ phần trăm của dung dịch HCl tham gia phản ứng
\(n_{Al} = \dfrac{10,8}{27} = 0,4(mol)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ n_{AlCl_3} = n_{Al} = 0,4(mol)\\ m_{AlCl_3} = 0,4.133,5 = 53,4(gam)\\ n_{HCl} =3 n_{Al} = 1,2(mol)\\ C\%_{HCl}= \dfrac{1,2.36,5}{200}.100\% = 21,9\%\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 13 gam Zn cần dùng vừa đủ dung dịch HCl 7,3 % thu được dung dịch X và thấy thoát ra V lít khí H2 (ở đktc)
a. Viết phương trình phản ứng hóa học?
b. Tính giá trị của V?
c. Tính khối lượng muối thu được?
d. Tính nồng độ phần trăm muối trong X?
Đọc tiếp
Hòa tan hoàn toàn 13 gam Zn cần dùng vừa đủ dung dịch HCl 7,3 % thu được dung dịch X và thấy thoát ra V lít khí H2 (ở đktc)
a. Viết phương trình phản ứng hóa học?
b. Tính giá trị của V?
c. Tính khối lượng muối thu được?
d. Tính nồng độ phần trăm muối trong X?
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c, \(n_{ZnCl_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
d, \(n_{HCl}=2n_{Zn}=0,4\left(mol\right)\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{14,6}{7,3\%}=200\left(g\right)\)
⇒ m dd sau pư = 13 + 200 - 0,2.2 = 212,6 (g)
\(\Rightarrow C\%_{ZnCl_2}=\dfrac{27,2}{212,6}.100\%\approx12,79\%\)
Đúng 3
Bình luận (0)
Cho săt tác dụng vừa đủ với 182,5 gam dung dịch HCl 5% đến khi phản ứng kết thúc thu được V lít khí ở đktc?
a.Viết phương trình hóa học xảy ra?
b. Tính khối lượng sắt đã phản ứng và tính V?
c.Tính nồng độ phần trăm của dung dịch muối thu được?
Fe+2HCl->FeCl2+H2
0,125--0,25---0,125-0,125
m HCl=9,125 g=>n HCl=\(\dfrac{9,125}{26,5}\)=0,25 mol
=>m Fe=0,125.56=7g
=>VH2=0,125.22,4=2,8l
=>C%FeCl2=\(\dfrac{0,125.127}{7+182,5-0,25}\).100=8,388%
Đúng 4
Bình luận (0)
Cho 2,7 gam nhôm tác dụng hết với dung dịch H2SO4 sau phản ứng thu được với V lít khí H2 ở điều kiện tiêu chuẩn và m gam muối.
a/ Viết phương trình hóa học
b/ Tính giá trị V
c/ Tính giá trị m
d/ Lượng khí Hidro thu được ở trên qua bình đựng 32 g CuO nung nóng. Hỏi chất nào còn dư sau phản ứng?