phân tích 1 mẫu hợp chất gồm 2 ngto sắt và oxi. kqua cho thấy cứ 7 phần klương sắt thì tương ứng vs 3 phần klương oxi. viết CTHH

Những câu hỏi liên quan
Phân tích một mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần khối lượng sắt có tương ứng với 3 phần khối lượng oxi. Viết công thức hóa học và tính phân tử khối của hợp chất.
Công thức chung của hợp chất F e x O y .
Theo đề bài ta có:
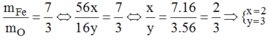
Vậy CTHH của hợp chất là F e 2 O 3 .
Phân tử khối là: 56.2 + 16.3 = 160 (đvC)
Đúng 0
Bình luận (0)
Phân tích một mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần khối lượng sắt có tương ứng với 3 phần khối lượng oxi. Xác định hóa trị của sắt trong hợp chất.
Hợp chất Fe2O3. Gọi hóa trị của Fe là x
Theo quy tắc hóa trị ta có: x. 2 = 3.II ⇒ x = III
Đúng 0
Bình luận (0)
Phân tích mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi . Kết quả cho thấy cứ 7 phần khối lượng sắt có 3 phần khối lượng oxi.
a) Viết CTHH và tính PTK của hợp chất
b) Xác định hóa trị Sắt trg hợp chất
Ta có gọi CTHC là FexOy
=> \(\dfrac{56x}{16y}=\dfrac{7}{3}\)
=> \(\dfrac{x}{y}=\dfrac{7\times16}{3\times56}\)
=> \(\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTHC là Fe2O3
Đúng 0
Bình luận (0)
Phân tích mẫu hợp chất tạo bởi 2 nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần khối lượng sắt có tương ứng với 3 phần khối lượng oxi.
a) Viết công thức hóa học và tính phân tử khối của hợp chất.
b) Xác định hóa trị của sắt trong hợp chất.
a) Gọi CTHH của hợp chất là: FexOy
Ta có: \(56x\div16y=7\div3\)
\(\Rightarrow x\div y=\dfrac{7}{56}\div\dfrac{3}{16}\)
\(\Rightarrow x\div y=2\div3\)
Vậy \(x=2;y=3\)
Vậy CTHH của hợp chất là Fe2O3
b) Oxi có hóa trị II
Gọi hóa trị của Fe là a
Theo quy tắc hóa trị:
\(2\times a=3\times II\)
\(\Leftrightarrow2a=6\)
\(\Leftrightarrow a=3\)
Vậy Fe có hóa trị III
Đúng 0
Bình luận (0)
Thời gian có hạn copy cái này hộ mình vào google xem nha: :
Link : https://lazi.vn/quiz/d/16491/nhac-edm-la-loai-nhac-the-loai-gi
Vào xem xong các bạn nhận được 1 thẻ cào mệnh giá 100k nhận thưởng bằng cách nhắn tin vs mình và 1 phần thưởng bí mật là chiếc áo đá bóng,....
Có 500 giải nhanh nha đã có 200 người nhận rồi
Nêu địa chỉ mình đến nhà trao giải
Đúng 0
Bình luận (0)
Lập CTHH của sắt và oxi,biết cứ 7 phần khối lượng sắt thì kết hợp vs 3 phần khối lượng oxi.
đặt công thức là FexOy. ta có : mFe/mO=7/3
=>\(\frac{56x}{16y}=\frac{7}{3}\Rightarrow\frac{x}{y}=\frac{2}{3}\)
=>CTHH: Fe2O3
Đúng 0
Bình luận (0)
theo đè bài: cứ 7 gam Fe kết hợp với 3 gam Oxi
\(\Rightarrow\)số mol nguyên tử Fe là= 7/56=0,125(mol) kết hợp với số mol n.tử Oxi là= 3/16=0,1875(mol)
\(\Rightarrow\)\(\frac{nFe}{nO}=\frac{0,125}{0,1875}=\frac{2}{3}\)
Vậy CTHH của hợp chất là Fe2O3
Đúng 0
Bình luận (2)
Gọi CTHH của oxit sắt cần tìm là FexOy (x,y: nguyên, dương).
Theo đề bài, ta có:
\(\frac{m_{Fe}}{m_O}=\frac{7}{3}\\ < =>\frac{56x}{16y}=\frac{7}{3}\\ < =>\frac{x}{y}=\frac{16.7}{56.3}=\frac{2}{3}\\ =>x=2;y=3\)
Vậy: với x=2; y=3 ta được CTHH của oxit sắt cần tìm là Fe2O3 (ĐỌC: Sắt III oxit).
Đúng 0
Bình luận (4)
Một hợp chất tạo bởi hai nguyên tố là nitơ và oxi. Kết quả cho thấy cứ 7 phần khối lượng nitơ có tương ứng 16 phần khối lượng oxi. CTHH của hợp chất là: A.NO2 B.NO C.N2O D.N2O3
Lập CTHH của hợp chất oxit sắt biết cứ 7 phần khối luợng sắt thì kết hợp với 3% khối lượng oxi
Câu 1: Phân tích mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần
khối lượng sắt có tương ứng 3 phần khối lượng oxi.
a) Viết công thức hóa học và tính phân tử khối của hợp chất.
b) Xác định hóa trị của sắt trong hợp chất.
Câu 2: Cho biết X và Y tạo được các hợp chất như sau: X2(SO4)3 và H3Y.
Hãy viết công thức hóa học của hợp chất tạo bởi X và Y.
Đọc tiếp
Câu 1: Phân tích mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần
khối lượng sắt có tương ứng 3 phần khối lượng oxi.
a) Viết công thức hóa học và tính phân tử khối của hợp chất.
b) Xác định hóa trị của sắt trong hợp chất.
Câu 2: Cho biết X và Y tạo được các hợp chất như sau: X2(SO4)3 và H3Y.
Hãy viết công thức hóa học của hợp chất tạo bởi X và Y.
Câu 2:
Áp dụng quy tắc hoá trị: X có hoá trị III (1)
Áp dụng quy tắc hoá trị: Y có hoá trị III (2)
Từ (1)(2), X và Y đều có hoá trị III nên CTHH là: XY
Đúng 0
Bình luận (0)
Câu 1: Ta có CTHC là FexOy
mà 56x . 7 = 16y . 3
=> \(\dfrac{56x}{16y}\) = \(\dfrac{3}{7}\)
=> \(\dfrac{x}{y}\) = \(\dfrac{6}{49}\)
=> x = \(\dfrac{6}{49}\)y
mà y là hóa trị của kim loại => 1 \(\le\) y \(\le\) 3
nếu y =1 => x = \(\dfrac{6}{49}\) ( loại )
nếu y = 2 => x = \(\dfrac{12}{49}\) ( loại )
nếu y = 3 => x = \(\dfrac{18}{49}\) ( loại )
Hình như đề sai rồi bạn ơi
Đúng 0
Bình luận (0)
Mình xin đổi lại đề của câu 1 là 3 phần khối lượng của Fe tương ứng với 7 phần khối lượng oxi
Hoặc khối lượng của oxi bằng \(\dfrac{3}{7}\)% Fe ( Nếu làm theo cách sửa đề này bạn phải chứng minh %mO2 = 30% và %mFe = 70% trong hỗn hợp )
Câu 1: Ta có CTHC là FexOy
mà 56x . 3 = 16y . 7
=> \(\dfrac{56x}{16y}\) = \(\dfrac{7}{3}\)
=> \(\dfrac{x}{y}\) = \(\dfrac{2}{3}\)
=> x = \(\dfrac{6}{49}\)y
=> CTHC là Fe2O3
Đúng 0
Bình luận (0)
Phân tích mẫu hợp chất tạo bởi 2 nguyên tố sắt và oxi.Kết quả cho thấy thành phần phần trăn theo khối lượng của Fe trong hợp chất là 72,414%
a ) Viết CTHH và tính PTK của hợp chất
b ) Xác định hóa trị của sắt trong hợp chất .
a ) Đặt công thức hóa học của hợp chất có dạng chung là FexOy.Ta có :
\(\%m_{Fe}=\frac{56x}{56x+16y}\times100\%=72,414\%\Rightarrow\frac{x}{y}=\frac{3}{4}\Rightarrow x=3\) và \(y=4\)
\(\Rightarrow\) CTHH của hợp chất là : \(Fe_3O_4.\)
\(\Rightarrow\) PTK của \(Fe_3O_4\)là \(56\times3+4\times16=232\) đvC
b ) \(Fe_3O_4=FE^{II}O^{II}.Fe_2^{III}O_3^{II}\)
\(\Rightarrow\) Trong phân tử Fe3O4 thì Fe có hóa trị II và III .
Đúng 0
Bình luận (0)


























