Nguyên tử nguyên tố Z có tổng số hạt là 28, trong đó hạt mang điện nhiều hơn hạt không mang điện là 8 hạt. Tìm số hạt mỗi loại

Những câu hỏi liên quan
4. Nguyên tử nguyên tố M có tổng số hạt là 93. Trong đó hạt không mang điện có nhiều hơn hạt mang điện tích dương là 6A. Tìm số hạt mỗi loại ?B. Tìm số khối , tên nguyên tố ? 5. Nguyên tử nguyên tố X có tổng số hạt là 36. Trong đó skks hạt trong nhân nhiều hơn số hạt ở vỏ là 12A. Tính số hạt mỗi loại ?B. Tính số khối , tìm tên nguyên tố ?MỌI NGƯỜI GIÚP EM VỚI ĐANG CẦN GẤP Ạ
Đọc tiếp
4. Nguyên tử nguyên tố M có tổng số hạt là 93. Trong đó hạt không mang điện có nhiều hơn hạt mang điện tích dương là 6
A. Tìm số hạt mỗi loại ?
B. Tìm số khối , tên nguyên tố ?
5. Nguyên tử nguyên tố X có tổng số hạt là 36. Trong đó skks hạt trong nhân nhiều hơn số hạt ở vỏ là 12
A. Tính số hạt mỗi loại ?
B. Tính số khối , tìm tên nguyên tố ?
MỌI NGƯỜI GIÚP EM VỚI ĐANG CẦN GẤP Ạ
4.
Ta có: \(\left\{{}\begin{matrix}p+e+n=93\\n-p=6\\p=e\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=29\\n=35\end{matrix}\right.\)
\(\Rightarrow A=p+n=29+35=64\left(u\right)\)
⇒ M là đồng (Cu)
5.
Ta có: \(\left\{{}\begin{matrix}p+e+n=36\\p=e\\p+n-e=12\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=12\\n=12\end{matrix}\right.\)
\(\Rightarrow A=p+n=12+12=24\left(u\right)\)\
⇒ X là magie (Mg)
Đúng 3
Bình luận (0)
Nguyên tử của nguyên tố x có tổng số hạt là 34 trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10 tìm số hạt mỗi loại
\(X(2p; n)\\ X: 2p+n=34(1)\\ MĐ>KMĐ: 2p-n=10(2)\\ (1)(2)\\ p=e=11\\ n=12\\ \Rightarrow Na\)
Đúng 1
Bình luận (2)
Nguyên tố X có tổng số hạt trong nguyên tử là 40, trong đó số hạt mang điện nhiều hơn hạt không mang điện là 12. Nguyên tố Y có tổng số hạt nguyên tử là 52. Số hạt mang điện nhiều hơn hạt mang điện trong X là 8. xác định Ct hợp chất gồm hai nguyên tố x và y
Do nguyên tử X có tổng số hạt trong nguyên tử là 40
=> 2pX + nX = 40 (1)
Do nguyên tử X có số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt
=> 2pX - nX = 12 (2)
(1)(2) => \(\left\{{}\begin{matrix}e_X=p_X=13\\n_X=14\end{matrix}\right.\) => X là Al
Nguyên tử X có số hạt mang điện là 13 + 13 = 26 (hạt)
=> Nguyên tử Y có số hạt mang điện là 26 + 8 = 34 (hạt)
=> eY = pY = 17 (hạt)
=> Y là Cl
CTHH hợp chất 2 nguyên tố X, Y có dạng AlxCly
Có: \(Al^{III}_xCl^I_y\)
=> Theo quy tắc hóa trị, ta có: x.III = y.I
=> \(\dfrac{x}{y}=\dfrac{I}{III}=\dfrac{1}{3}\)
=> CTHH: AlCl3
Đúng 8
Bình luận (0)
ta có : số hạt mạng điện tích ở X nhiều hơn số hạt ko mạng điện tích là 12
=> p+e-n = 12
<=> 2p-n=12 (p=e)
<=> n = 2p - 12 (1)
mà tổng số hạt ở X là 40
=> 2p+n=40 (2)
thay (1)vào (2) ta đc
2p+2p-12 = 40
<=> 4p = 52
<=> p = 13
=> X là nhôm : Al
Đúng 2
Bình luận (0)
Cho biết tổng số hạt p, e, n trong 2 nguyên tử của 2 nguyên tố A và B là 78,trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 26 hạt. Số hạt mang điện của nguyên tử nguyên tố A nhiều hơn số hạt mang điện của B là 28 hạt. Xác định số p trong 2 nguyên tố A và B. Giúp mình với ạ, các bn viết luôn vì sao ra kết quả như vậy giúp mình với, nhất là đoạn cuối cùng vì sao số p của A.. hoặc B ra như vậy, lấy mấy nhân mấy hay chia mấy á, cảm ơn nhiều ạ
Đọc tiếp
Cho biết tổng số hạt p, e, n trong 2 nguyên tử của 2 nguyên tố A và B là 78,trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 26 hạt. Số hạt mang điện của nguyên tử nguyên tố A nhiều hơn số hạt mang điện của B là 28 hạt. Xác định số p trong 2 nguyên tố A và B. Giúp mình với ạ, các bn viết luôn vì sao ra kết quả như vậy giúp mình với, nhất là đoạn cuối cùng vì sao số p của A.. hoặc B ra như vậy, lấy mấy nhân mấy hay chia mấy á, cảm ơn nhiều ạ
Đặt tổng số hạt p, n, e của A và B lần lượt là p, n, e
`=>` \(\left\{{}\begin{matrix}p+e+n=78\\p+e-n=26\\p=e\end{matrix}\right.\Leftrightarrow p=e=n=26\)
`=>` \(\left\{{}\begin{matrix}p_A+p_B=26\\2p_A-2p_B=28\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p_A=20\\p_B=6\end{matrix}\right.\)
Vậy A là Canxi (Ca); B là Cacbon (C)
Đúng 1
Bình luận (0)
Tổng số hạt trong nguyên tử của 1 nguyên tố z là 35. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 11 hạt. Tìm số hạt electron?
Nguyên tử nguyên tố X có tổng số hạt proton,nơtron và electron là 52. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 16.Tính số hạt mỗi loại của nguyên tử X
Ta có: p + e + n = 52
Mà p = e, nên: 2p + n = 52 (1)
Theo đề, ta có: 2p - n = 16 (2)
Từ (1) và (2), ta có HPT:
\(\left\{{}\begin{matrix}2p+n=52\\2p-n=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=17\\n=18\end{matrix}\right.\)
Vậy p = e = 17 hạt, n = 18 hạt.
Đúng 3
Bình luận (2)
Vì tổng số hạt proton , nơtron , electron là 52 nên ta có :
\(p+n+e=52\Leftrightarrow2p+n=52\left(1\right)\)
Vì số hạt mang điện nhiều hơn số hạt không mang điện nên ta có :
\(2p-n=16\left(2\right)\)
Từ (1) và (2) ta có hệ phương trình :
\(\left\{{}\begin{matrix}2p+n=52\\2p-n=16\end{matrix}\right.\)
Giải hệ ta được :
\(p=17\Rightarrow e=17\)
\(n=18\)
Đúng 2
Bình luận (2)
Nguyên tử của 1 nguyên tố có tổng các loại hạt là 28 hạt.Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 8 hạt.
a)Hãy tìm số hạt proton ,electron và nơtron của nguyên tử .
b) Tính nguyên tử khối của nguyên tử.
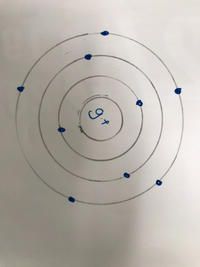
c)Vẽ sơ đồ cấu tạo của nguyên tử.
Tổng các loại hạt là 28 hạt
\(2p+n=28\left(1\right)\)
Số hạt mang điện nhiều hơn số hạt không mang điện là 8 hạt.
\(2p-n=8\left(2\right)\)
\(\left(1\right),\left(2\right):p=e=9.n=10\)
\(M=p+n=9+10=19\left(đvc\right)\)
Đúng 1
Bình luận (0)
a)
Gọi :
Số hạt proton = số hạt electron = p
Số hạt notron = n
Tổng số hạt : 2p + n = 28
Hạt mang điện nhiều hơn không mang điện là 8 : 2p - n = 8
Suy ra : p = 9 ; n = 10
Vậy có 9 hạt proton,9 hạt electron và 10 hạt notron
b)
Nguyên tử khối = p + n = 9 + 10 = 19 đvC
c)
Đúng 0
Bình luận (0)
a) nguyên tử X có tổng số 3 loại hạt p,n và e bằng 52 hạt trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt
b) một nguyên tử của nguyên tố Y có tổng số hạt là 28 (p,n và e) và số hạt không mang điện chiếm xấp xỉ 35,7%
hãy xác định số p,n và e và vẽ sơ đồ đơn giản của nguyên tử X,Y
a. Nguyên tử X:
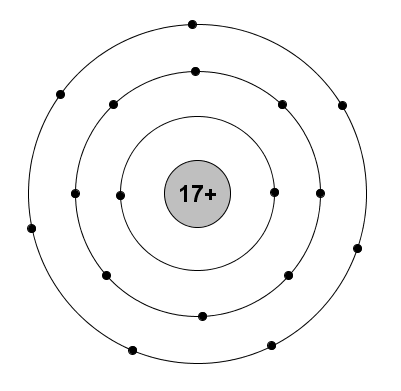
\(\left\{{}\begin{matrix}2P+N=52\\2P-N=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=17=E=Z\\N=18\end{matrix}\right.\)
Sơ đồ đơn giản:
b. * Nguyên tử Y:
\(\left\{{}\begin{matrix}2P+N=28\\N\approx35,7\%.28=10\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=E=Z=9\\N=10\end{matrix}\right.\)
Sơ đồ cấu tạo nguyên tử Y:
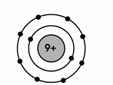
Em tham khảo nha!
Đúng 2
Bình luận (0)
a.
Gọi: pX , eX , nX là các hạt trong X.
Khi đó :
\(2p_X+n_X=52\)
\(2p_X-n_X=16\)
\(\Rightarrow p_X=17,n_X=18\)

b.
Gọi: pY , eY , nY là các hạt trong Y.
Khi đó :
\(2p_Y+n_Y=28\)
\(n_Y=35.7\%\cdot28=10\) \(\Rightarrow p_Y=9\)
Đúng 3
Bình luận (0)
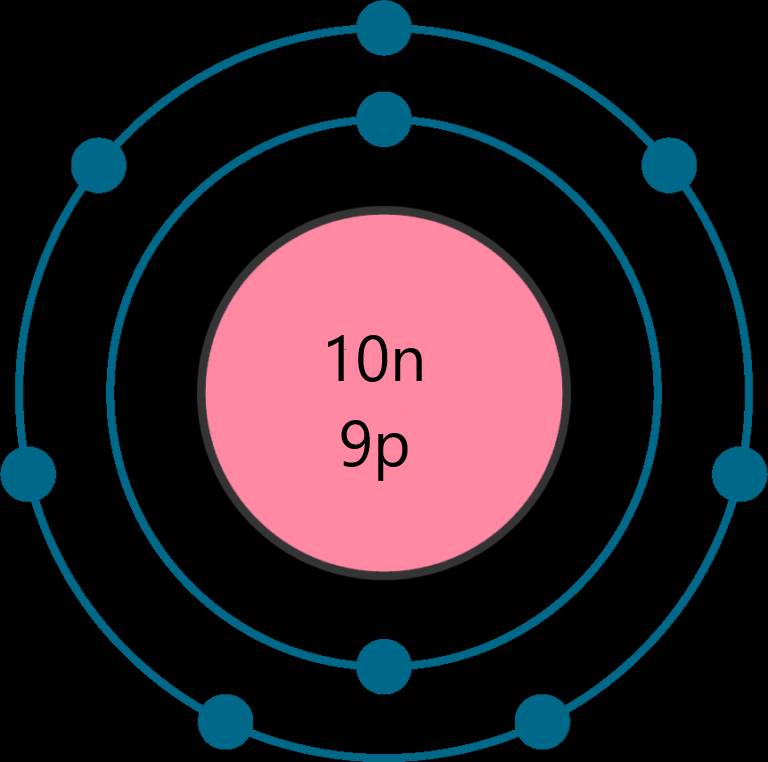
nguyên tử của một nguyên tố có tổng số các loại hạt là 28, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 8. Xác định số p, số n, số e của nguyên tử nguyên tố đó. Vẽ mô hình nguyên tử. Xác định vị trí của nguyên tố đó trong bảng tuần hoàn.
Tổng số các loại hạt là 28, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 8
⇒ Số neutron là 10 hạt
Số proton là 9 hạt
Số electron là 9 hạt
⇒ Nguyên tố Fluorine - ô số 9, chu kì 2, nhóm VIIA trong bảng tuần hoàn
Đúng 1
Bình luận (0)




























