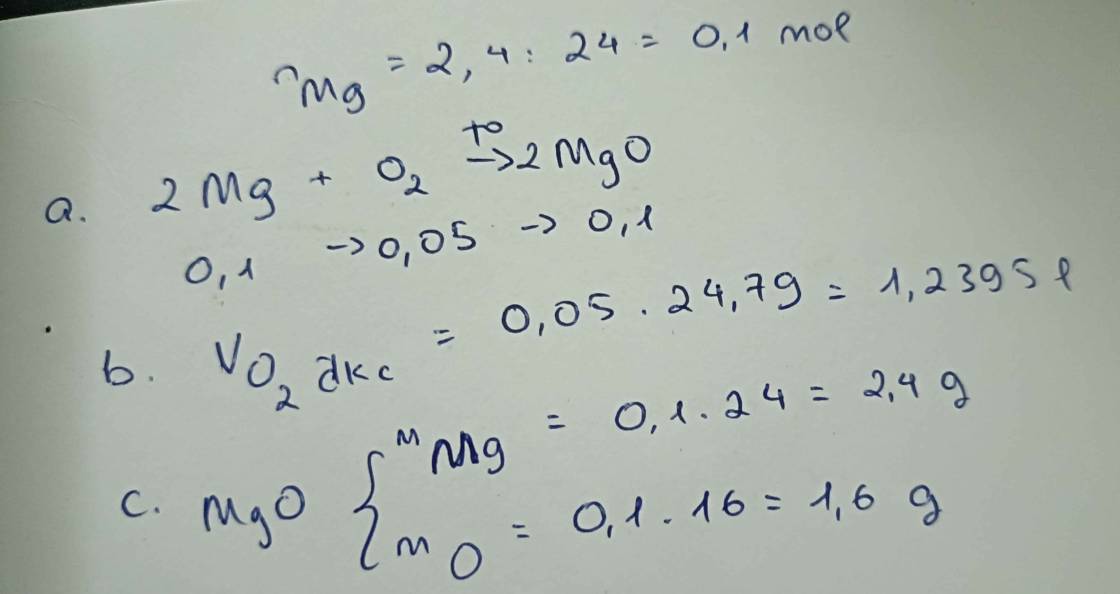đốt cháy hoàn toàn 36g Mg trong không khí thu được m [g] MgO . tính m ?

Những câu hỏi liên quan
BÀI 2: Đốt cháy hoàn toàn 4,8 gam Mg trong khí oxygen (O2) thu được MgO.a. Viết phương trình hóa học.b. Tính thể tích khí O2 cần dùng ở đktc (25oC, 1 bar).c. Tính khối lượng MgO thu đượcBÀI 3: Đốt cháy hoàn toàn 2,4 gam Mg trong 1,6 gam khí oxygen (O2) thu được MgO.a. Viết công thức về khối lượng của phản ứng xảy ra.b. Tính khối lượng MgO thu được.c. Khối lượng khí O2 tham gia ở trên tương đương bao nhiêu phân tử?Cho: Mg 24; O 16; H 1
Đọc tiếp
BÀI 2: Đốt cháy hoàn toàn 4,8 gam Mg trong khí oxygen (O2) thu được MgO.
a. Viết phương trình hóa học.
b. Tính thể tích khí O2 cần dùng ở đktc (25oC, 1 bar).
c. Tính khối lượng MgO thu được
BÀI 3: Đốt cháy hoàn toàn 2,4 gam Mg trong 1,6 gam khí oxygen (O2) thu được MgO.
a. Viết công thức về khối lượng của phản ứng xảy ra.
b. Tính khối lượng MgO thu được.
c. Khối lượng khí O2 tham gia ở trên tương đương bao nhiêu phân tử?
Cho: Mg = 24; O = 16; H = 1
Bài 2:
a) 2Mg + O2 --to--> 2MgO
b) \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: 2Mg + O2 --to--> 2MgO
_______0,2->0,1------>0,2
=> VO2 = \(\dfrac{0,1.0,082.\left(273+25\right)}{0,99}=2,468\left(l\right)\)
c) mMgO = 0,2.40 = 8(g)
Bài 3
a) Theo ĐLBTKL: mMg + mO2 = mMgO (1)
b) (1) => mMgO = 2,4 + 1,6 = 4(g)
c) \(nO_2=\dfrac{1,6}{32}=0,05\left(mol\right)\)
=> Số phân tử O2 = 0,05.6.1023 = 0,3.1023
Đúng 4
Bình luận (0)
Đốt cháy hoàn toàn 2,4 g Mg trong khí Oxy thu được Magnesium Oxide
a) Lập PTHH của phản ứng trên?
b) Tính thể tích Oxy cần dùng ở đkc `(25^0` và `1` bar`)`
c) Tính số g mỗi nguyên tố trong lượng MgO thu được.
Đốt cháy hoàn toàn 8,6g Mg trong ko khí thu đc 20, 4g MgO . Tính khối lượng khí oxi đã dùng
Đốt cháy hoàn toàn 0,48 gam Mg trong không khí thu được Mgo a,phương trình hóa học của phản ứng
b, tính thể tích không khí cần dùng ở điều kiện tự nhiên biết oxi chiếm 20% thể tích không khí
c, tính khối lượng chất tạo thành
a. \(n_{Mg}=\dfrac{0,48}{24}=0,02\left(mol\right)\)
PTHH : 2Mg + O2 -to-> 2MgO
0,02 0,01 0,02
b. \(V_{O_2}=0,01.22,4=0,224\left(l\right)\)
\(\Rightarrow V_{kk}=0,224.5=1,12\left(l\right)\)
c. \(m_{MgO}=0,02.40=0,8\left(g\right)\)
Đúng 2
Bình luận (0)
: Đốt cháy hoàn toàn 24g Magie( Mg) trong không khí. Sau khi phản ứng xảy ra hoàn toàn thu được 40g Magie oxit( MgO). Hãy: a/ Lập phương trình hóa học của phản ứng trênb/ Viết công thức về khối lượng theo ĐLBTKL và tính khối lượng Oxi( O2) tham gia trong phản ứng. Biết rằng Mg cháy trong không khí là phản ứng với Oxi (Al27, C12, O16, H1
Đọc tiếp
: Đốt cháy hoàn toàn 24g Magie( Mg) trong không khí. Sau khi phản ứng xảy ra hoàn toàn thu được 40g Magie oxit( MgO). Hãy:
a/ Lập phương trình hóa học của phản ứng trên
b/ Viết công thức về khối lượng theo ĐLBTKL và tính khối lượng Oxi( O2) tham gia trong phản ứng. Biết rằng Mg cháy trong không khí là phản ứng với Oxi
(Al=27, C=12, O=16, H=1
a, PTHH:
2Mg + O2 \(\underrightarrow{t^o}\) 2 Mg O
b, CT về khối lượng theo ĐLBTKL:
mMg + mO2 = mMgO
24 + mO2 = 40
=> mO2 = 40 - 24 = 16 ( g )
Đúng 0
Bình luận (2)
Đốt cháy m g kim loại magie Mg trong không khí thu được 12g hợp chất magie oxit (MgO). Biết rằng khối lượng magie Mg tham gia bằng 1,5 lần khối lượng oxi (không khí) tham gia phản ứng
nMgO = 12/40 = 0.3 mol
Mg + 1/2O2 -to-> MgO
0.3_____0.15____0.3
mMg = 0.3*24=7.2 g
mO2= 0.15*32=4.8 g
Đúng 0
Bình luận (0)
Đốt cháy m g kim loại magie Mg trong không khí thu được 8g hợp chất magie oxit (MgO). Biết rằng khối lượng magie Mg tham gia bằng 1,5 lần khối lượng oxi (không khí) tham gia phản ứng
nMgO = 8/40= 0.2 (mol)
Mg + 1/2O2 -to-> MgO
nMg = nMgO = 0.2 mol
mMg = 4.8 (g)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 4,8g Mg trong bình đựng khí Oxi và thu được MgO
a) viết PTHH
b) Tính thể tích khí Oxi ở đktc
c) Tính khối lượng MgO thu được
d) Tính thể tích KMnO4 để điều chế lượng Oxi trên
a.b.c.\(n_{Mg}=\dfrac{m_{Mg}}{M_{Mg}}\dfrac{4,8}{24}=0,2mol\)
\(2Mg+O_2\rightarrow\left(t^o\right)2MgO\)
0,2 0,1 0,2 ( mol )
\(V_{O_2}=n_{O_2}.22,4=0,1.22,4=2,24l\)
\(m_{MgO}=n_{MgO}.M_{MgO}=0,2.40=8g\)
d. Sửa đề: tính khối lượng KMnO4
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,2 0,1 ( mol )
\(m_{KMnO_4}=n_{KMnO_4}.M_{KMnO_4}=0,2.158=31,6g\)
Đúng 2
Bình luận (0)
Nhiệt phân hoàn toàn 73,5 gam KClO3 để điều chế khí O2
a) tính thể tích O2 ở điều kiện tiêu chuẩn
b) Lấy toàn bộ lượng O2 thu được trên Để đốt cháy 7,2 g Mg thì thu được bao nhiêu gam MgO
Xem chi tiết
a, PT: \(2KClO_3\xrightarrow[MnO_2]{t^o}2KCl+3O_2\)
Ta có: \(n_{KClO_3}=\dfrac{73,5}{122,5}=0,6\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{3}{2}n_{KClO_3}=0,9\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,9.22,4=20,16\left(l\right)\)
b, PT: \(2Mg+O_2\underrightarrow{t^o}2MgO\)
Ta có: \(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,3}{2}< \dfrac{0,9}{1}\), ta được O2 dư.
Theo PT: \(n_{MgO}=n_{Mg}=0,3\left(mol\right)\)
\(\Rightarrow m_{MgO}=0,3.40=12\left(g\right)\)
Bạn tham khảo nhé!
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 4,8 g magie(Mg) trong không khí thì thu được 8g Magie oxit . Tính khối lượng oxi tham gia phản ứng
\(m_{Mg}+m_{O_2}\rightarrow m_{MgO}\Leftrightarrow4,8g+m_{O_2}\rightarrow8\Leftrightarrow m_{O_2}=3,2g\)
MIK ĐANG CẦN GẤP GIÚP MIK VỚI