Cho một lượng kim loại R có khối lượng 5,4 gam vào dung dịch HCl dư thì thu được 6,72 lít khí Hiđro (ĐTC). Xác định kim loại R Biết R có hóa trị III.

Những câu hỏi liên quan
Cho 5,4 gam kim loại X hóa trị III hòa tan hết vào dung dịch HCl thu được 6,72 lít khí H2 (đktc)
a)Lập PTHH của phản ứng.
b)Xác định kim loại X.
c) Tính khối lượng muối XCl3 tạo thành
\(a,PTHH:2X+6HCl\to 2XCl_3+3H_2\\ b,n_{H_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ \Rightarrow n_{X}=\dfrac{2}{3}n_{H_2}=0,2(mol)\\ \Rightarrow M_{X}=\dfrac{5,4}{0,2}=27(g/mol)\)
Vậy X là nhôm (Al)
\(c,n_{AlCl_3}=n_{Al}=0,2(mol)\\ \Rightarrow m_{AlCl_3}=0,2.133,5=26,7(g)\)
Đúng 0
Bình luận (0)
Cho 16,8 gam một kim loại R hóa trị 2 tan hoàn toàn trong dung dịch H2SO4 loãng thu được 6,72 lít khí (điều kiện tiêu chuẩn).Xác định tên kim loại ( R) và khối lượng muối thu được.
$R + H_2SO_4 \to RSO_4 + H_2$
$n_R = n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)$
$M_R = \dfrac{16,8}{0,3} =56(Fe)$
Vậy R là Sắt
$n_{FeSO_4} = n_{H_2} = 0,3(mol)$
$m_{FeSO_4} = 0,3.152 =45,6(gam)$
Đúng 1
Bình luận (0)
Hòa tan hết 5,4 gam kim loại R (hóa trị III) vào dung dịch H2SO4 loãng thu được 6,72 lít H2 (ở đktc) a/ Xác định tên kim loại b/ Nếu dùng 5,4 gam kim loại trên cho tác dụng hết với H2SO4 đặc nóng thì thể tích khí đo được ở đktc là bao nhiêu
Hòa tan hết 5,4 gam kim loại R (hóa trị III) vào dung dịch H2SO4 loãng thu được 6,72 lít H2 (ở đktc) a/ Xác định tên kim loại b/ Nếu dùng 5,4 gam kim loại trên cho tác dụng hết với H2SO4 đặc nóng thì thể tích khí đo được ở đktc là bao nhiêu
\(n_{H2\left(dktc\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a) Pt : \(2R+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
0,2 0,3
\(n_R=\dfrac{0,3.2}{3}=0,2\left(mol\right)\)
⇒ \(M_R=\dfrac{5,4}{0,2}=27\left(dvc\right)\)
Vậy kim loại R là nhôm
b) \(2Al+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Al_2\left(SO_4\right)_3+3SO_2+6H_2O|\)
2 6 1 3 6
0,2 0,3
\(n_{SO2}=\dfrac{0,3.3}{2}=0,3\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,3.22,4=6,72\left(l\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
a) PTHH: \(2R+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\) \(\Rightarrow n_R=0,2\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{5,4}{0,2}=27\) \(\Rightarrow\) R là Nhôm (Al)
b) PTHH: \(2Al+6H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}Al_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
Theo PTHH: \(n_{SO_2}=0,3\left(mol\right)\) \(\Rightarrow V_{SO_2}=0,3\cdot22,4=6,72\left(l\right)\)
Đúng 2
Bình luận (0)
Hòa tan 16,8g kim loại R hóa trị( ll )vào dung dịch HCl dư, sau phản ứng thu được 6,72 lít khí H₂ (đktc). Xác định R.
\(n_{H2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Pt : \(R+2HCl\rightarrow RCl_2+H_2\)
\(n_R=n_{H2}=0,3\left(mol\right)\Rightarrow M_R=\dfrac{16,8}{0,3}=56\left(Fe\right)\)
Vậy kim loại R là sắt
Đúng 1
Bình luận (0)
Cho khí hiđro dư đi qua 28,8 gam hỗn hợp X gồm R và Oxit kim loại R nung nóng. Sau khi phản ứng xảy ra hoàn toàn thu được 22,4 gam chất rắn. Hòa tan hết lượng chất rắn trên bằng dung dịch HCl thì có 8,96 lít hiđro bay ra ở đktc. a) Xác định kim loại R b) Xác định công thức oxit kim loại R, biết tỉ lệ khối giữa oxit kim loại R và R trong X là 29:7.
Cho 6,06 gam hỗn hợp X gồm một kim loại kiềm M và một kim loại R có hóa trị III vào nước, thấy hỗn hợp X tan hoàn toàn tạo ra dung dịch A và 3,808 lít khí (đktc). Chia dung dịch A làm hai phần bằng nhau: – Cô cạn phần thứ nhất thu được 4,48 gam chất rắn khan. – Thêm V lít dung dịch HCl 1M vào phần thứ hai thấy xuất hiện 0,78 gam kết tủa. a. Xác định tên hai kim loại và tính thành phần % khối lượng mỗi kim loại trong X. b. Tính giá trị V.
Đọc tiếp
Cho 6,06 gam hỗn hợp X gồm một kim loại kiềm M và một kim loại R có hóa trị III vào nước, thấy hỗn hợp X tan hoàn toàn tạo ra dung dịch A và 3,808 lít khí (đktc). Chia dung dịch A làm hai phần bằng nhau:
– Cô cạn phần thứ nhất thu được 4,48 gam chất rắn khan.
– Thêm V lít dung dịch HCl 1M vào phần thứ hai thấy xuất hiện 0,78 gam kết tủa.
a. Xác định tên hai kim loại và tính thành phần % khối lượng mỗi kim loại trong X.
b. Tính giá trị V.
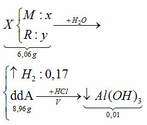
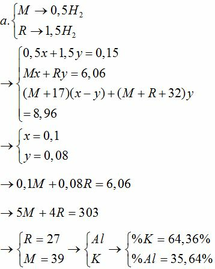
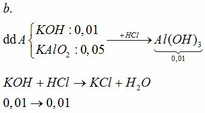
TH1: kết tủa Al(OH)3 chưa bị hòa tan
KAlO2 + HCl +H2O → KCl + Al(OH)3↓
0,01 ←0,01
→ nHCl = 0,02
→ V = 0,02 (lít) = 20 (ml)
TH2: kết tủa Al(OH)3 bị hòa tan một phần
KAlO2 + HCl +H2O → KCl + Al(OH)3↓
0,05 → 0,05 0,05
Al(OH)3 + 3HCl → AlCl3 + 3H2O
0,04` → 0,12
→ nHCl = 0,18 → V = 0,18 (l) = 180 (ml)
Vậy có 2 giá trị của V thỏa mãn là: 20 ml và 180 ml
Đúng 0
Bình luận (0)
Hòa tan 5,4g một kim loại hóa trị III vào dung dịch H2SO4 lượng dư. Sau p/ứ thu được 6,72 lít khí H2 (đktc). Xác định tên kim loại.
nH2 = 6.72/22.4 = 0.3 (mol)
2A + 3H2SO4 => A2(SO4)3 + 3H2
0.2______________________0.3
MA = 5.4/0.2 = 27
=> A là : Al
Đúng 3
Bình luận (0)
Cho 4,8 gam kim loại magie tác dụng hoàn toàn với dung dịch axit HCl. Tính: a. Thể tích hiđro thu được ở đktc? c. Nếu dùng lượng khí Hiđro trên để khử vừa đủ một lượng oxit kim loại R hóa trị II thì thu được 12,8gam kim loại. Tìm kim loại R.
Mg+2HCl->MgCl2+H2
0,2-----------------------0,2
RO+H2-to>R+H2O
0,2-------------0,2
n Mg=\(\dfrac{4,8}{24}\)=0,2 mol
=>VH2=0,2.22,4=4,48l
->0,2=\(\dfrac{12,8}{R}\)
=>R=64 g\mol
=>R là Cu(đồng)
Đúng 2
Bình luận (0)
Cho 2,16 gam một kim loại R hóa trị (III) tác dụng hết với lượng khí oxi dư, thu được 4,08 gam một oxit có dạng R 2 O 3 . Xác định tên và kí hiệu hóa học của kim loại R.






















