Methane là một nguyên liệu sạch , thân thiện với môi trường.Xét phản ứng đốt cháy methane trong buồng đốt động cơ xe buýt sử dụng nguyên liệu CNG Tính thể tích khí co2 (điều kiện chuẩn) ở 25°C, 1bar từ 24,79 lít khí CH4

Những câu hỏi liên quan
Đốt cháy hoàn toàn 0,1 mol khí methane tính thể tích khí carbon dioxde (điều kiện chuẩn) và khối lượng nước sinh ra khi đốt cháy.
Đọc tiếp
Đốt cháy hoàn toàn 0,1 mol khí methane tính thể tích khí carbon dioxde (điều kiện chuẩn) và khối lượng nước sinh ra khi đốt cháy.
\(PTHH:CH_4+2O_2-^{t^o}>CO_2+2H_2O\)
tỉ lệ 1 ; 2 : 1 ; 2
n(mol) 0,1------->0,2------>0,1------->0,2
\(V_{CO_2\left(dkc\right)}=n\cdot24,79=0,1\cdot24,79=2,479\left(l\right)\\ m_{H_2O}=n\cdot M=0,2\cdot18=3,6\left(g\right)\)
Đúng 3
Bình luận (0)
đốt cháy hoàn toàn 11,2 lit khí methane hãy tính khí oxygen cần dùng và thể tích khí carbonic tạo thành ( ở đkc 25°C , 1bar ) xin có giải thích , vì sao luôn ạ
\(n_{CH_4}=\dfrac{V}{22,4}=\dfrac{11,2}{22,4}=0,5mol\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
0,5 1 0,5 ( mol )
\(V_{O_2}=n.24,79=1.24,79=24,79l\)
\(V_{CO_2}=n.24,79=0,5.24,79=12,395l\)
Đúng 6
Bình luận (0)
nCH4 = 11,2/22,4 = 0,5 (mol)
PTHH: CH4 + 2O2 -> (t°) CO2 + 2H2O
Mol: 0,5 ---> 1
VO2 = 1 . 24,79 = 24,79 (l)
Đúng 4
Bình luận (0)
nCH4 = 11,2/22,4 = 0,5 (mol)
PTHH: CH4 + 2O2 -> (t°) CO2 + 2H2O
Mol: 0,5 ---> 1
VO2 = 1 . 24,79 = 24,79 (l)
Đúng 1
Bình luận (0)
Một nhà máy phát điện vận hành bằng các đốt cháy nhiên liệu phức hợp có công thức trung bình là C11H7S. Giả sử nguồn không khí cung cấp chỉ chứa N2 và O2 có tỷ lệ mol 3,76:1,00 và N2 không cho phản ứng. Ngoài nước tạo thành, lượng cacbon trong nhiên liệu được chuyển hóa hoàn toàn thành CO2 và lưu huỳnh chuyển hóa thành SO2. (a) Viết phương trình phản ứng cháy của C11H7S. (b) Để phản ứng cháy xảy ra hoàn toàn, thực tế cần dùng dư 20% lượng oxy so với tỷ lượng lý thuyết. Tính khối lượng (kg) và t...
Đọc tiếp
Một nhà máy phát điện vận hành bằng các đốt cháy nhiên liệu phức hợp có công thức trung bình là C11H7S. Giả sử nguồn không khí cung cấp chỉ chứa N2 và O2 có tỷ lệ mol 3,76:1,00 và N2 không cho phản ứng. Ngoài nước tạo thành, lượng cacbon trong nhiên liệu được chuyển hóa hoàn toàn thành CO2 và lưu huỳnh chuyển hóa thành SO2.
(a) Viết phương trình phản ứng cháy của C11H7S.
(b) Để phản ứng cháy xảy ra hoàn toàn, thực tế cần dùng dư 20% lượng oxy so với tỷ lượng lý thuyết. Tính khối lượng (kg) và thể tích (ở đktc, m3) không khí cần sử dụng để đốt cháy hoàn toàn 1 tấn C11H7S.
(c) Tính tổng khối lượng CO2 và SO2 tạo thành trong điều kiện của câu (b) trên

Do lấy dư 20% oxi so với lượng cần đốt cháy nên lượng oxi đã lấy là:


Tổng khối lượng CO2 và SO2 :
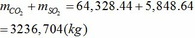
Chú ý:
Lượng O2 lấy dư 20% so với với lượng cần thiết => tính mol O2 chính xác
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 4,48 lít khí Methane (CH4) không khí.
a. Tính khối lượng CO2 tạo thành.
b. Tính thể tích oxi và thể tích không khí cần cho phản ứng (biết oxi chiếm 20% thể tích không khí; các thể tích khí đo ở đktc).
các bạn giúp mình :>
CH4+2O2-to>CO2+2H2O
0,2-----0,4------0,2
n CH4=0,2 mol
=>mCO2=0,2.44=8,8g
=>VO2=0,4.22,4=8,96l
=>Vkk=8,96.5=44,8l
Đúng 3
Bình luận (1)
nCH4 = 4,48:22,4 = 0,2 (mol)
pthh : CH4 + 2O2 -t-> CO2 + 2H2O
0,2 0,4 0,2
mCO2 = 0,2 . 44 = 8,8 (G)
VO2 = 0,4 . 22,4 = 8,96 (L)
=> Vkk = VO2 : 20% = 8,96 : 20% = 44,8 (L)
Đúng 1
Bình luận (1)
Đốt cháy khí methane (CH4) trong không khí thu được carbon dioxide (CO2) và nước (H2O) theo sơ đồ sau:Quan sát sơ đồ hình 2.3 và cho biết:a) Trước phản ứng có các chất nào, những nguyên tử nào liên kết với nhau?b) Sau phản ứng, có các chất nào được tạo thành, những nguyên tử nào liên kết với nhau?c) So sánh số nguyên tử C, H, O trước và sau phản ứng.
Đọc tiếp
Đốt cháy khí methane (CH4) trong không khí thu được carbon dioxide (CO2) và nước (H2O) theo sơ đồ sau:
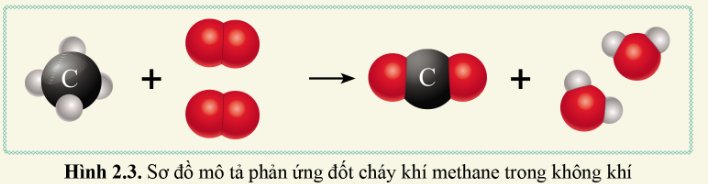
Quan sát sơ đồ hình 2.3 và cho biết:
a) Trước phản ứng có các chất nào, những nguyên tử nào liên kết với nhau?
b) Sau phản ứng, có các chất nào được tạo thành, những nguyên tử nào liên kết với nhau?
c) So sánh số nguyên tử C, H, O trước và sau phản ứng.
a. Trước phản ứng, có các chất là C, H, O.
- Những nguyên tử H đã liên kết với nguyên tử C, nguyên tử O liên kết với nguyên tử O.
b. Sau phản ứng, có các chất được tào thành là CO2, H2O.
- Những nguyên tử O đã liên kết với nguyên tử C, những nguyên tử H đã liên kết với những nguyên tử O.
c. Số nguyên tử C, H, O trước phản ứng và sau phản ứng đều bằng nhau
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn 1,2 lít khí axetilen trong không khí
a, tính thể tíc khí co2 sinh ra ở điều kiện tiêu chuẩn
b, tính thể tích không khí (ở điều kiện chuẩn) cần dùng cho phản ứng trên biết oxi chiếm 20% thể tích của không khí biết
Methane là thành phần chính của khí thiên nhiên. Xét phản ứng đốt cháy methane:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ΔrH298
o = -890,3 kJ
Biết nhiệt tạo thành chuẩn của CO2(g) và H2O(l) tương ứng là –393,5 và –285,8 kJ/mol. Hãy tính
nhiệt tạo thành chuẩn của khí methane.
\(\Delta_fH^{^{ }o}_{298}\left[CH_4\right]=-\left(-890,3-\left(-393,5\right)-\left(-285,8\right)\right)\\ \Delta_fH^{^{ }o}_{298}\left[CH_4\right]=211kJ\cdot mol^{-1}\)
Đúng 1
Bình luận (0)
Khí thiên nhiên được sử dụng làm nhiên liệu và nguyên liệu đầu vào cho ngành chế biến hóa chất, đốt trong các bếp, lò ga để nấu nướng, sấy khô, nung gạch, lò cao sản xuất xi măng, nấu thủy tinh, luyện kim, … Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lit khí CO2 (ở đktc) và 9,90 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là: A. 84,...
Đọc tiếp
Khí thiên nhiên được sử dụng làm nhiên liệu và nguyên liệu đầu vào cho ngành chế biến hóa chất, đốt trong các bếp, lò ga để nấu nướng, sấy khô, nung gạch, lò cao sản xuất xi măng, nấu thủy tinh, luyện kim, … Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lit khí CO2 (ở đktc) và 9,90 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là:
A. 84,00 lít
B. 78,40 lít
C. 70,00 lít
D. 56,00 lít
Chọn C
Bảo toàn O : 2nO2 = 2nCO2 + nH2O => nO2 = 0,625 mol
=> nkk = 5nO2 = = 3,125 mol => Vkk = 70 lit
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 9,2 gam rượu etylic.
a) Tính thể tích khí CO2 tạo ra ở điều kiện tiêu chuẩn.
b) Tính thể tích không khí (ở điều kiện tiêu chuẩn) cần dùng cho phản ứng trên. Biết oxi chiếm 20% thể tích không khí


























