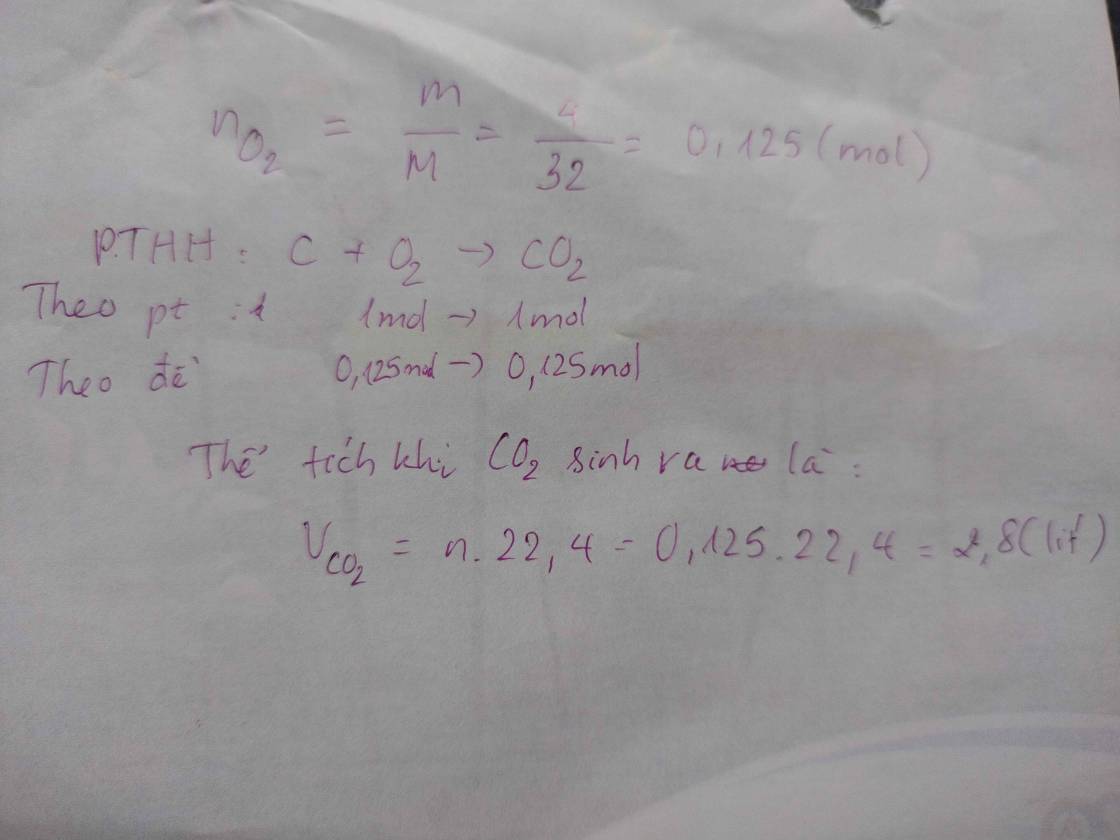Đốt 12g carbon trong oxygen dư thu được 39.6 g carbon dioxide CO2 theo pthh C + O2 suy ra CO2 Tính hiệu suất của phản ứng trên

Những câu hỏi liên quan
Tính hiệu suất phản ứng khi đốt 12 gam carbon trong khí oxygen thu được 39,6 gam, CO2 biết phản ứng xảy ra theo phương trình: C + O2 = CO2
\(n_C=\dfrac{12}{12}=1mol\\ C+O_2\underrightarrow{t^0}CO_2\\ n_{CO_2,lt}=n_C=1mol\\ m_{CO_2,lt}=1.44=44g\\ H=\dfrac{39,6}{44}\cdot100\%=90\%\)
Đúng 0
Bình luận (0)
Carbon cháy trong khí oxygen hoặc trong không khí sinh ra khí carbon dioxxide: C + O2 → CO2 Hãy tìm thể tích khí carbon dioxide (đktc) sinh ra nếu có 4 gam khí oxi tham gia phản ứng
Đốt cháy 1 tấn than trong khí oxygen, biết trong than có chứa 90% Carbon, biết hiệu suất đạt 80%
a. Lập PTHH của phản ứng
b. Tính khối lượng CO2 sinh ra
\(m_C=1000\cdot90\%=900\left(kg\right)\)
\(n_C=\dfrac{900}{12}=75\left(kmol\right)\)
\(C+O_2\underrightarrow{^{^{t^o}}}CO_2\)
\(75............75\)
\(m_{CO_2}=75\cdot44=3300\left(kg\right)\)
\(m_{CO_2\left(tt\right)}=3300\cdot80\%=2640\left(kg\right)=2.64\left(\text{tấn}\right)\)
Đúng 2
Bình luận (0)
Đốt cháy carbon C cần dùng 16 g khí oxygen O2, thu được 22 g khí carbonic CO2
a) Viết công thức về khối lượng của phản ứng xảy ra.
b) Tính khối lượng carbon đã phản ứng.
a) C+O2→CO2(đk nhiệt độ)
b)Áp dụng định luật bảo toàn khối lượng,có:
mC+mO2=mCO2
=>mC=22-16=6 g
Đúng 1
Bình luận (1)
Nung 16,8 gam magnesium carbonate (MgCO3), thu được khí carbon dioxide (CO2) và 6 gam magnesium oxide (MgO). Tính hiệu suất phản ứng ?
`#3107.101107`
Khối lượng mol của \(\text{MgCO}_3\) là:
\(\text{M}_{\text{MgCO}_3}=24+12+16\cdot3=84\left(\text{mol}\right)\)
Số mol của \(\text{MgCO}_3\) là:
\(\text{n}_{\text{MgCO}_3}=\dfrac{\text{m}_{\text{MgCO}_3}}{\text{M}_{\text{MgCO}_3}}=\dfrac{16,8}{84}=0,2\left(\text{mol}\right)\)
PTHH: \(\text{MgCO}_3\text{ }\underrightarrow{t^0}\text{ CO}_2+\text{MgO}\)
Theo PT: 1 : 1 : 1 (mol)
`=>` n của MgO là `0,2` mol
Khối lượng của MgO thu được là:
\(\text{m}_{\text{MgO}}=\text{n}_{\text{MgO}}\cdot\text{ M}_{\text{MgO}_2}=0,2\cdot\left(24+16\right)=0,2\cdot40=8\left(\text{g}\right)\)
Hiệu suất của pứ trên là:
\(\text{H = }\dfrac{\text{m'}}{\text{m}}\cdot100=\dfrac{6}{8}\cdot100=75\%\)
Vậy, hiệu suất của phản ứng trên là `75%.`
Đúng 1
Bình luận (0)
4. Carbon cháy trong khí oxygen hoặc trong không khí sinh ra khí carbon dioxxide: C + O2 → CO2 Hãy tính thể tích khí oxygen O2 (đktc) cần dùng để đốt cháy hoàn toàn 24 gam carbon C
gài 7: Dẫn 6,72 lit khí Carbon dioxide CO2 (đkc) vào 200ml dung dịch nước vôi trong dư. a) Tính khối lượng kết tủa CaCO3 thu được b) Tính CM của dung dịch nước vôi trong đã phản ứng. Bài 8: Hấp thụ V(lít) khí Carbon dioxide CO2 vào 200ml dung dịch Barium hydroxide Ba(OH)2 1M dư. a) Tính thể tích khí Carbon dioxide CO2 đã dùng (ở đkc) b) Tỉnh khối lượng kết tủa BaCO3 thu được
Bài 8 :
\(n_{Ba\left(OH\right)2}=1.0,2=0,2\left(mol\right)\)
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3\downarrow+H_2O\)
Theo Pt : \(n_{Ba\left(OH\right)2}=n_{CO2}=n_{BaCO3}=0,2\left(mol\right)\)
a) \(V_{CO2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
b) \(m_{BaCO3}=0,2.197=39,4\left(g\right)\)
Đúng 2
Bình luận (0)
Điều kiện tiêu chuẩn chứ bạn nhỉ? Đkc sao lại 6,72l đc?
Bài 7 :
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH :
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,3 0,3 0,3 0,3
\(a,m_{CaCO_3}=0,3.100=30\left(g\right)\)
\(b,C_{M\left(Ca\left(OH\right)_2\right)}=\dfrac{0,3}{0,2}=1,5M\)
Bài 8 :
\(n_{Ba\left(OH\right)_2}=1.0,2=0,2\left(mol\right)\)
PTHH :
\(CO_2+Ba\left(OH\right)_2\rightarrow BaCO_3+H_2O\)
0,2 0,2 0,2 0,2
\(a,V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
\(b,m_{BaCO_3}=0,2.197=39,4\left(g\right)\)
Đúng 2
Bình luận (0)
\(n_{CO2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
Theo Pt : \(n_{CO2}=n_{Ca\left(OH\right)2}=n_{CaCO3}=0,3\left(mol\right)\)
\(m_{CaCO3}=0,2.100=20\left(g\right)\)
b) \(C_{MddCa\left(OH\right)2}=\dfrac{0,3}{0,2}=1,5M\)
Đúng 0
Bình luận (2)
cho 6 kg carbon tác dụng với 16 kg oxygen. Tính khối lượng khí carbon dioxide thu được. Cho biết phản ứng xả ra hoàn toàn
PTHH : $C + O_2 \xrightarrow{t^o} CO_2$
Ta có :
$m_C + m_{O_2} = m_{CO_2}$
$\Rightarrow m_{CO_2} = 6 + 16 = 22(kg)$
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn lượng bột nhôm (Al) cần dùng 7,437L khí oxygen (O2) ở điều kiện chuẩn
a) Lập PTHH của phản ứng trên
b) tính khối lượng chất sản phẩm thu được
c) nếu giả sử trong phản ứng chỉ thu được 18,36 g sản phẩm thì hiệu suất phản ứng trên là bao nhiêu
a, \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
b, \(n_{O_2}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
Theo PT: \(n_{Al_2O_3}=\dfrac{2}{3}n_{O_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3}=0,2.102=20,4\left(g\right)\)
c, \(H=\dfrac{18,36}{20,4}.100\%=90\%\)
Đúng 2
Bình luận (0)