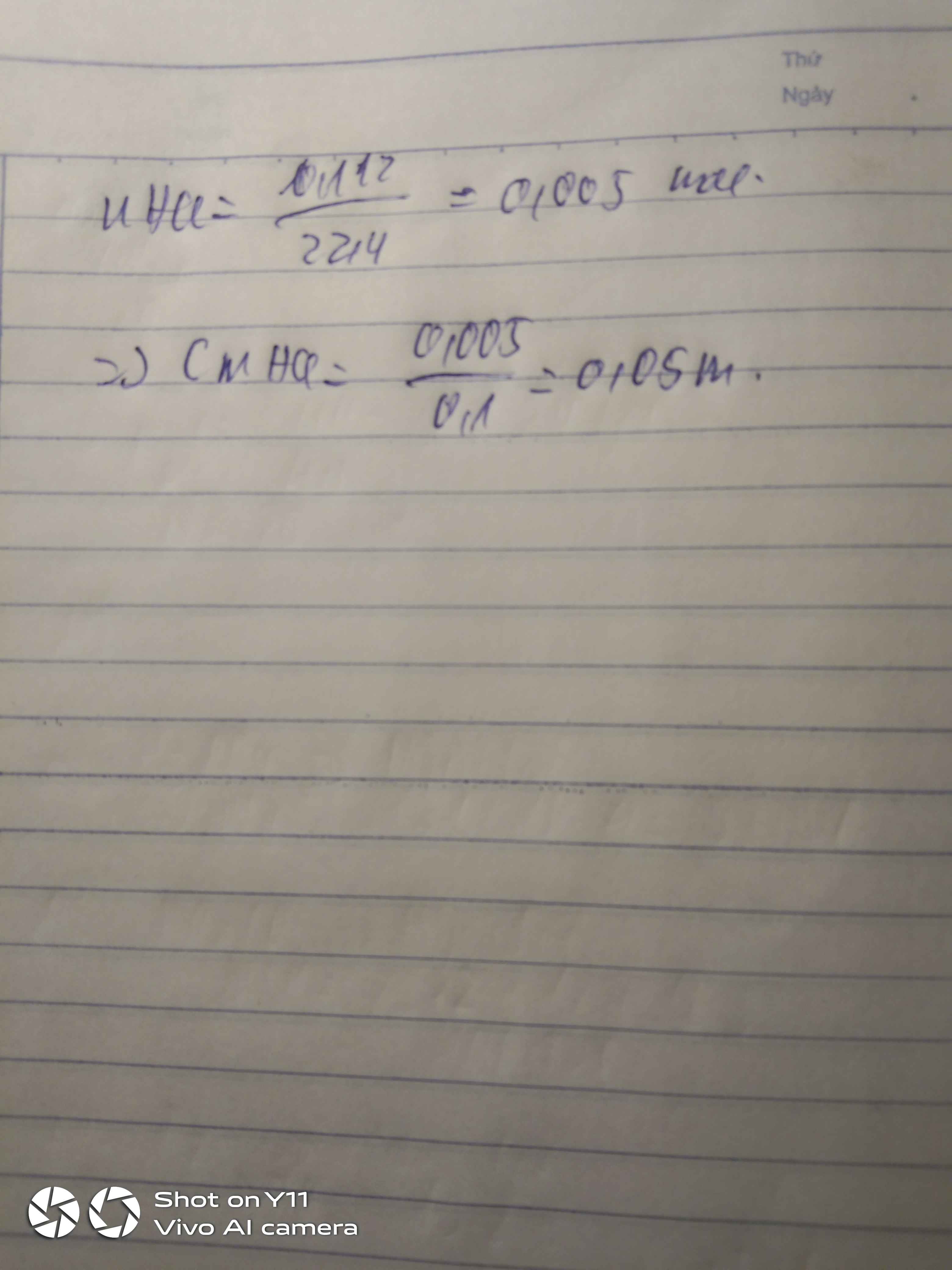hòa tan 1,2g Magie bằng 50 ml dd HCl 3M A) Viết PTHH B) tính thể tích thoát ra (Đktc) C) tính nồng độ mol/L của dd thu đc ( với thể tích k đổi)

Những câu hỏi liên quan
Hòa tan hoàn toàn 16.25 gam bột kẽm vào 500ml dd HCl a) Viết PTHH xảy ra? b) Tính thể tích khí hiđro thoát ra ở đktc? c) Tính nồng độ mol/l của axit trong dd lúc đầu? d) Cho toàn bộ lượn muối sinh ra vào 400ml dd nạo nồng độ 1M. Tính khối lượng chất rắn thu được trong dd sau PƯ?
a) $Zn + 2HCl \to ZnCl_2 + H_2$
b) Theo PTHH : $n_{H_2} = n_{Zn} = \dfrac{16,25}{65} = 0,25(mol)$
$\Rightarrow V_{H_2} = 0,25.22,4 = 5,6(lít)$
c) $n_{HCl} = 2n_{Zn} = 0,5(mol)$
$\Rightarrow C_{M_{HCl}} = \dfrac{0,5}{0,5} = 1M$
Đúng 1
Bình luận (0)
Cho 4.8 gam kim loại magie vào 200ml dd axit clohiric (hcl) sau phản ứng thu được magie clorua(MgCl2) và khí hidro a) tính thể tích khí video thu được ở đktc b) tính nồng độ mol dd HCL? c) nếu trung hòa dd HCL trên bằng dd KOH 5.6% (D= 1.045g/ml).Tính thể tích dd KOH cần dùng
Ta có: \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
a, \(n_{H_2}=n_{Mg}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, \(n_{HCl}=2n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,4}{0,2}=2\left(M\right)\)
c, PT: \(HCl+KOH\rightarrow KCl+H_2O\)
Theo PT: \(n_{KOH}=n_{HCl}=0,4\left(mol\right)\)
\(\Rightarrow m_{ddKOH}=\dfrac{0,4.56}{5,6\%}=400\left(g\right)\)
\(\Rightarrow V_{ddKOH}=\dfrac{400}{1,045}\approx382,78\left(ml\right)\)
Đúng 2
Bình luận (0)
Hòa tan 32,5 gam Zn bằng 250 ml dd HCl, sau phản ứng tạo ra kẽm clorua ZnCl2 và khí H2 a/ tính khối lượng muối ZnCl2 b/ tính thể tích H2 tạo thành sau phản ứng (đktc) c/ tính nồng độ mol dd HCl đã dùng d/ tính nồng độ mol dd sau phản ứng ( thể tích dd không đổi) Lập tóm tắt
Zn + 2HCl --> ZnCl2 + H2
0,5 1 0,5 0,5
nZn=\(\dfrac{32,5}{65}\)=0,5(mol)
mZnCl2=0,5.136=68(g)
VH2=0,5.22,4=11,2(l)
c) CM HCl=\(\dfrac{1}{0,25}=4M\)
Đúng 8
Bình luận (3)
cho 16,8g sắt tác dụng hết với 500ml dd HCL
a/ viết pthh
b/ tính thể tích khí H2 thu đc ở đktc
c/ tính KL muối tạo thành sau phản ứng
d/ tính nồng độ mol của các chất tan trong dd sau phản ứng biết ban đầu dd HCL có nồng độ là 0,6M (coi thể tích đ thay đổi k đg kể )
giúp mk vs mk đg cần gấp
Hòa tan 7.8 g kim loại K vào 200g H2O ( D=1g/ml ) thu được V (l) khí ở đktc và dung dịch A.
a, tính thể tích khí thu được (đktc)
b, tính nồng độ mol/l của dd A
c, tính thể tích dung dịch HCl cần dùng để trung hòa hết dd A và tính nông độ mol/l của dd thu được sau phản ứng
K + H2O = KOH + 1/2H2
0,2 mol 0,1 mol
a) V = 0,1.22,4 = 2,24 lit
b) CM = n/V = 0,2/0,2 = 1 M (thể tích dd A đổi ra là 200 ml = 0.2 lit).
c) HCl + KOH = KCl + H2O
V = 0,2.22,4 = 4,48 lit; CM = 0,2/(0,2+4,48) = 0,0427 M (câu này đúng ra phải cho nồng độ của HCl, bạn kiểm tra lại xem đề bài có thiếu không). Nếu cho nồng độ của HCl thì thể tích của HCl = 0,2.CM(HCl); và CM = 0,2/(V(HCl) + 0,2).
Đúng 0
Bình luận (0)
sao Vdd = 0,2. thế k cộng K vào vs nước à bạn
Đúng 0
Bình luận (0)
Chú ý là khối lượng chất tan khi cho vào dd thì không làm thay đổi đáng kể Vdd, do đó Vdd vẫn là 0,2.
Đúng 0
Bình luận (0)
Cho kẽm tác dụng với 300ml dd hcl thu dd A và 2,24l khí B (đktc) A) viết PTHH B) tính nồng độ mol dd hcl C) tính nồng độ mol dd A. Thể tích dd B D) tính khối lượng kẽm
A) Viết phương trình hoá học:
Khi kẽm (Zn) tác dụng với axit clohidric (HCl), sẽ tạo ra khí hidro (H2) và muối kẽm clorua (ZnCl2).
Phương trình hoá học cho phản ứng này là:
Zn + 2HCl -> ZnCl2 + H2
B) Tính nồng độ mol của dung dịch HCl:
Dựa vào phương trình hoá học, 1 mol kẽm (Zn) reaguje với 2 mol axit clohidric (HCl) để tạo ra 1 mol khí hidro (H2) và 1 mol muối kẽm clorua (ZnCl2).
Dựa vào thông tin bạn đã cung cấp, chúng ta có 2,24 lít khí H2 (đktc), tức là chúng ta có 2,24 mol khí H2 (vì 1 mol khí ở điều kiện tiêu chuẩn có thể có thể thể tích 22,4 lít).
Vì mỗi mol khí H2 tạo ra tương ứng với 2 mol HCl, nên nồng độ mol của dung dịch HCl là:
Nồng độ mol HCl = 2 x 2,24 mol = 4,48 mol/L
C) Tính nồng độ mol của dung dịch A:
Theo phương trình hoá học, mỗi mol kẽm (Zn) tạo ra 1 mol muối kẽm clorua (ZnCl2). Vì vậy, nồng độ mol của dung dịch A cũng là 4,48 mol/L, giống như nồng độ mol của dung dịch HCl.
D) Tính khối lượng của kẽm:
Theo phương trình hoá học, 1 mol kẽm (Zn) tạo ra 1 mol muối kẽm clorua (ZnCl2). Vì vậy, khối lượng của kẽm (Zn) bằng khối lượng muối kẽm clorua (ZnCl2).
Để tính khối lượng muối ZnCl2, bạn cần biết khối lượng mol của nó. Để làm điều này, bạn cần biết trọng lượng nguyên tử của mỗi nguyên tố trong muối ZnCl2:
Khối lượng nguyên tử của Zn (kẽm) = 65,38 g/molKhối lượng nguyên tử của Cl (clor) = 35,45 g/mol (x 2 vì có 2 nguyên tử clor)Khối lượng mol của ZnCl2 = (65,38 g/mol + 2 x 35,45 g/mol) = 136,28 g/mol
Bây giờ chúng ta có thể tính khối lượng muối kẽm clorua (ZnCl2):
Khối lượng muối ZnCl2 = Nồng độ mol x Thể tích = 4,48 mol/L x 0,3 L = 1,344 mol
Khối lượng muối ZnCl2 = 1,344 mol x 136,28 g/mol = 183,13 g
Vậy khối lượng của kẽm (Zn) là 183,13 g.
Đúng 0
Bình luận (0)
\(n_{H2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
a) Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
0,1 0,2 0,1 0,1
b)\(C_{MddHCl}=\dfrac{0,2}{0,3}=0,67\left(M\right)\)
c) \(C_{MZnCl2}=\dfrac{0,1}{0,3}=0,33\left(M\right)\)
d) \(m_{Zn}=0,1.65=6,5\left(g\right)\)
Chúc bạn học tôt
Đúng 1
Bình luận (1)
Để hòa tan hoàn toàn 10,8 gam nhôm cần dùng 150 ml dung dịch H2 SO4
a, Tính nồng độ mol/lit của dd H2SO4 đã dùng
b, Tính thể tích khí Hiđro thoát ra ở đktc
c, Tính nồng độ mol/lít của dung dịch thu được sau phản ứng(coi như thể tích là không đổi)
Đọc tiếp
Để hòa tan hoàn toàn 10,8 gam nhôm cần dùng 150 ml dung dịch H2 SO4
a, Tính nồng độ mol/lit của dd H2SO4 đã dùng
b, Tính thể tích khí Hiđro thoát ra ở đktc
c, Tính nồng độ mol/lít của dung dịch thu được sau phản ứng(coi như thể tích là không đổi)
a) \(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
0,4-->0,6---------->0,2------->0,6
=> \(C_{M\left(dd.H_2SO_4\right)}=\dfrac{0,6}{0,15}=4M\)
b) VH2 = 0,6.22,4 = 13,44 (l)
c) \(C_{M\left(Al_2\left(SO_4\right)_3\right)}=\dfrac{0,2}{0,15}=\dfrac{4}{3}M\)
Đúng 2
Bình luận (0)
\(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\\
pthh:2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,4 0,6 0,2 0,6
\(C_M_{H_2SO_4}=\dfrac{0,6}{0,15}=4M\\ V_{H_2}=0,622,4=13,44L\)
\(C_M=\dfrac{0,2}{0,15}=1,3M\)
Đúng 0
Bình luận (0)
hòa tan 112 ml khí HCl(đktc) vào trong 100ml nước biết thể tích dd thay đổi không đang kể tính nồng độ mol của dd HCl
Hòa tan 6 g Magie trong dung dịch axit clohiđric nồng độ 2M
a. Viết PTHH
b. tính thể tích khí thoát ra (đktc)
c. cần dùng bao nhiêu ml dung dịch axit clohiđric để hòa tan hết lượng magie trên.
\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\)
a) Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,25 0,5 0,25
b) \(n_{H2}=\dfrac{0,25.1}{1}=0,25\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,25.22,4=5,6\left(l\right)\)
c) \(n_{HCl}=\dfrac{0,25.2}{1}=0,5\left(mol\right)\)
\(V_{ddHCl}=\dfrac{0,5}{2}=0,25\left(l\right)=250\left(ml\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
\(a,PTHH:Mg+2HCl\rightarrow MgCl_2+H_2\\ b,n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\\ \Rightarrow n_{H_2}=0,25\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=0,25\cdot22,4=5,6\left(l\right)\\ c,n_{HCl}=2n_{Mg}=0,5\left(mol\right)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,5}{2}=0,25\left(l\right)\)
Đúng 1
Bình luận (0)
nMg=6/24=0,25 mol
Mg+HCl→MgCl2+ H2
0,25 0,25 0,25 mol
VH2=0,25.22,4=5,6 l
VHCl=0,25/2=0,125l =125ml
Đúng 0
Bình luận (0)