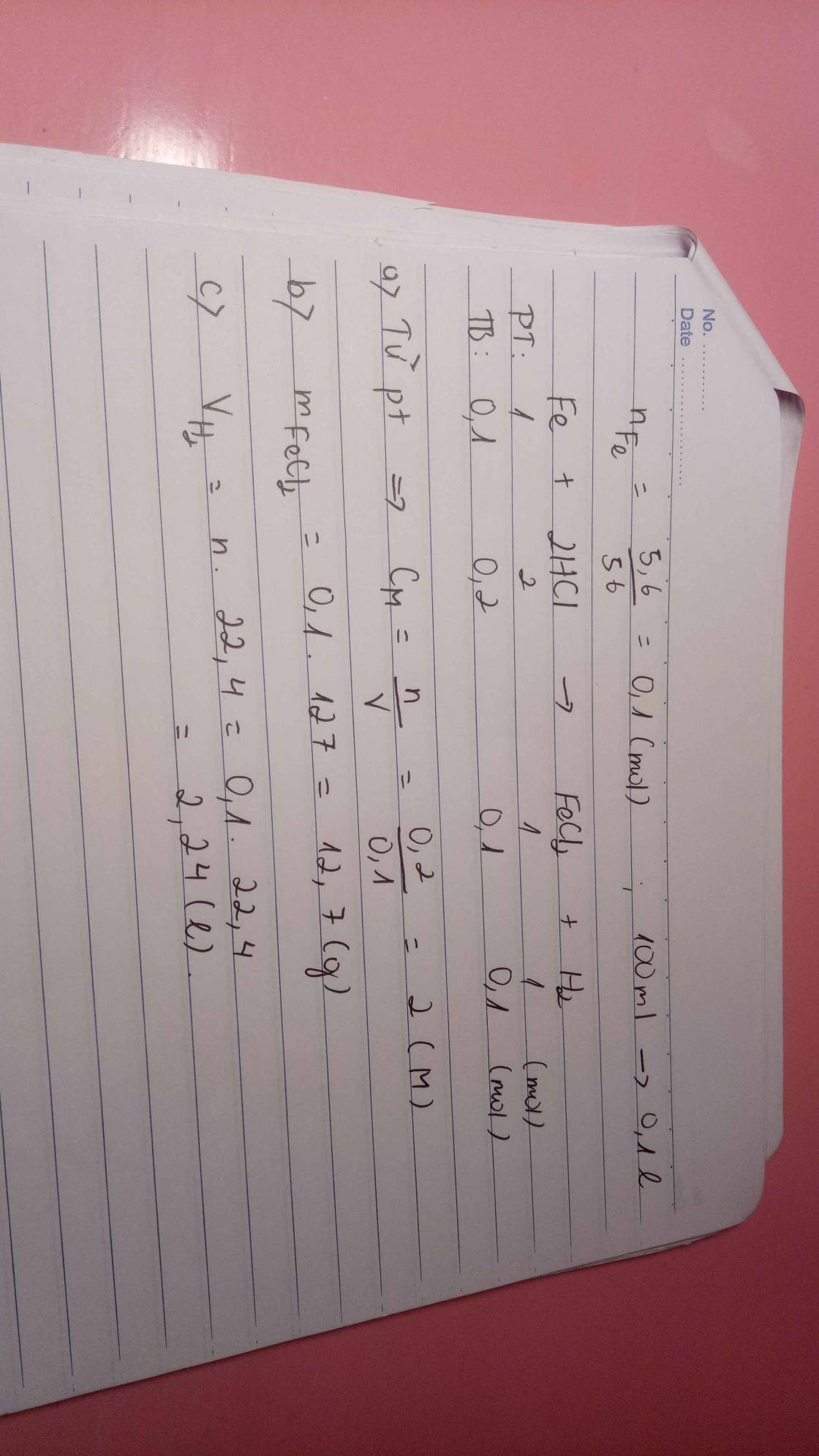cho 2,8g sắt Fe phản ứng hoàn toàn với dung dịch axit clohdric HCl phản ứng hóa học xảy ra theo PTHH sau . tính khối lượng dung dịch axit HCl sau phản ứng , Biết Fe bằng 56; Zn bằng 65; Cl bằng 35,5 ; H bằng 1

Những câu hỏi liên quan
cho 2,8g sắt Fe phản ứng hoàn toàn với dung dịch axit clohdric HCl phản ứng hóa học xảy ra theo PTHH sau . tính khối lượng dung dịch axit HCl sau phản ứng ;
Fe + HCl → FeCl2 + H2
tính khối lượng dung dịch axit HCl sau phản ứng
(Biết: Fe = 56; Zn = 65; Cl = 35,5; H = 1
\(n_{Fe}=\dfrac{2.8}{56}=0.05\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.05......0.1\)
\(m_{HCl}=0.1\cdot36.5=3.65\left(g\right)\)
Chỉ tìm được khối lượng HCl thoi em nhé !
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 1 lượng Fe bằng dung dịch HCL 0,3M ,thu được 6,72 L khí (đktc) : viết PTHH a,Tính khối lượng Fe tham gia phản ứng b,Tính thể tích dung dịch axit tham gia c,Tính nồng độ dung dịch sau phản ứng [biết Fe:56/Cl:35,5/H:1) Giúp mình plsssss :>>
a) \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
nFe = nH2 = 0,3 (mol)
\(\Rightarrow m_{Fe}=0,3.56=16,8\left(g\right)\)
b) nHCl = 2.nH2 = 0,6 (mol)
\(\Rightarrow V_{ddHCl}=\dfrac{0,6}{0,3}=2\left(l\right)\)
c) \(n_{FeCl_2}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow C_{M\left(FeCl_2\right)}=\dfrac{0,3}{2}=0,15M\)
Đúng 4
Bình luận (0)
\(Fe+2HCl\rightarrow FeCl_2+H_2\\ a,n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\\ n_{Fe}=n_{FeCl_2}=n_{H_2}=0,3mol\\ m_{Fe}=0,3.56=16,8g\\ b,n_{HCl}=2n_{H_2}=0,3.2=0,6mol\\ V_{ddHCl}=\dfrac{0,6}{0,3}=2l\\ c,C_{M_{FeCl_2}}=\dfrac{0,3}{2}=0,15M\)
Đúng 2
Bình luận (1)
Cho 28g sắt(Fe) phản ứng hoàn toàn với dung dịch axit clohidric(HCl), phản ứng hóa học xảy ra như sau:
Fe + HCl -> FeCl2 + H2
a) Viết phương trình phản ứng hóa học.
b) Tính thể tích khí H2 thu được ở đktc
c) Tính khối lượng FeCl2 thu được bằng 2 cách.
M.n giúp mìh với, mìh cần gấp ạ, thanks
a) Theo đề bài , ta có:
nFe= \(\frac{m_{Fe}}{M_{Fe}}=\frac{28}{56}=0,5\left(mol\right)\)
PTHH: Fe + 2HCl -> FeCl2 + H2
Theo PTHH: 1:2:1:1 (mol)
Theo đề bài: 0,5:1:0,5:0,5 (mol)
b) Theo PTHH và đề bài, ta có:
\(n_{H_2}=n_{Fe}=0,5\left(mol\right)\)
Thể tích khí H2 thu được (đktc) :
\(V_{H_2\left(đktc\right)}=n_{H_2}.22,4=0,5.22,4=11,2\left(g\right)\)
c) Theo PTHH và đề bài, ta có:
\(n_{FeCl_2}=n_{Fe}=0,5\left(mol\right)\)
Khối lượng FeCl2 thu được:
\(m_{FeCl_2}=n_{FeCl_2}.M_{FeCl_2}=0,5.127=63,5\left(g\right)\)
Đúng 2
Bình luận (0)
Cho khối lượng của Fe là 5,6 gam phản ứng với dung dịch HCl theo sơ đồ phản ứng sau:
Fe + HCl -> FeCl2 + H2
a) Lập phương trình hóa học của phản ứng
b) Tính khối lượng FeCl2 và thể tích của H2
Biết Fe bằng 56, H bằng 1, Cl bằng 17
a, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b, Ta có: \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Theo PT: \(n_{FeCl_2}=n_{H_2}=n_{Fe}=0,1\left(mol\right)\)
\(\Rightarrow m_{FeCl_2}=0,1.127=12,7\left(g\right)\)
\(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 2
Bình luận (0)
cho 2,8g sắt Fe phản ứng hoàn toàn với dung dịch axit clohdric, thu được sắt II clorua FeCl2 và khí Hidro thoát ra
a, Viết PTHH
b, tính Vhidro thoát ra
giúp tuii zớiii
\(n_{Fe}=\dfrac{2,8}{56}=0,05mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,05 0,05
\(V_{H_2}=0,05\cdot22,4=1,12l\)
Đúng 5
Bình luận (0)
hòa tan hoàn toàn 11,2 gam kim loại sắt (Fe) cần vừa đủ 200 gam dung dịch axit axetic CH3COOH
Viết phương trình hóa học của phản ứng xảy ra
tính khối lượng muối sinh ra
tính nồng độ phần trăm của muối có trong dung dịch sau phản ứng
\(Fe+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Fe+H_2\)
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Theo PT: \(n_{\left(CH_3COO\right)_2Fe}=n_{Fe}=0,2\left(mol\right)\Rightarrow m_{\left(CH_3COO\right)_2Fe}=0,2.174=34,8\left(g\right)\)
Ta có: \(n_{H_2}=n_{Fe}=0,2\left(mol\right)\)
m dd sau pư = 11,2 + 200 - 0,2.2 = 210,8 (g)
\(\Rightarrow C\%_{\left(CH_3COO\right)_2Fe}=\dfrac{34,8}{210,8}.100\%\approx16,51\%\)
Đúng 3
Bình luận (0)
1. Cho 200g dung dịch NaOH 20% tác dụng vừa hết với 100g dung dịch HCl. Tính:
a) Nồng độ muối thu được sau phản ứng?
b) Tính nồng độ axit HCl. Biết phản ứng xảy ra hoàn toàn?
2. Hòa tan hoàn toàn 11,2g sắt cần vừa đủ V(l) dung dịch HCl 0,2M sau phản ứng thu được dung dịch A và X (lít) H2(đktc).
a) Tìm V?
b) Tìm X?
c) Tính CM của muối thu được trong dung dịch A?
1. Cho 200g dung dịch NaOH 20% tác dụng vừa hết với 100g dung dịch HCl. Tính:
a) Nồng độ muối thu được sau phản ứng?
b) Tính nồng độ axit HCl. Biết phản ứng xảy ra hoàn toàn?
---
a) mNaOH=20%.200=40(g) -> nNaOH=40/40=0,1(mol)
PTHH: NaOH + HCl -> NaCl + H2O
Ta có: nNaCl=nHCl=nNaOH=1(mol)
=> mNaCl=1.58,5=58,5(g)
mddNaCl=mddNaOH + mddHCl= 200+100=300(g)
=>C%ddNaCl= (58,5/300).100=19,5%
b) mHCl=0,1. 36,5=36,5(g)
=> C%ddHCl=(36,5/100).100=36,5%
Đúng 1
Bình luận (0)
2. Hòa tan hoàn toàn 11,2g sắt cần vừa đủ V(l) dung dịch HCl 0,2M sau phản ứng thu được dung dịch A và X (lít) H2(đktc).
a) Tìm V?
b) Tìm X?
c) Tính CM của muối thu được trong dung dịch A?
---
a) nFe=0,2(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
0,2_____0,4______0,2___0,2(mol)
a) V=VddHCl= nHCl/CMddHCl= 0,4/0,2=2(l)
b) V(H2,đktc)=0,2.22,4=4,48(l)
c) Vddmuoi=VddHCl=2(l)
CMddFeCl2= (0,2/2)=0,1(M)
Chúc em học tốt!
Đúng 1
Bình luận (0)
Cho 5,6g Fe phản ứng hoàn toàn với 100ml dung dịch HCl phản ứng xảy ra hoàn toàn a. Xác định nồng độ dung dịch HCl cần dùng b. Xác định khối lượng muối thu được sau phản ứng c. Xác định thể tích Hidro thu được sau phản ứng
Để giải bài toán này, ta cần biết phương trình phản ứng giữa Fe và HCl: Fe + 2HCl -> FeCl2 + H2 a. Để xác định nồng độ dung dịch HCl cần dùng, ta cần tính số mol của Fe. Đầu tiên, ta cần chuyển khối lượng Fe thành số mol bằng cách sử dụng khối lượng mol của Fe (56g/mol): Số mol Fe = khối lượng Fe / khối lượng mol Fe = 5,6g / 56g/mol = 0,1 mol Vì theo phương trình phản ứng, 1 mol Fe tương ứng với 2 mol HCl, nên số mol HCl cần dùng là gấp đôi số mol Fe: Số mol HCl = 2 x số mol Fe = 2 x 0,1 mol = 0,2 mol Để tính nồng độ dung dịch HCl, ta chia số mol HCl cho thể tích dung dịch HCl: Nồng độ HCl = số mol HCl / thể tích dung dịch HCl = 0,2 mol / 0,1 L = 2 mol/L Vậy, nồng độ dung dịch HCl cần dùng là 2 mol/L. b. Để xác định khối lượng muối thu được sau phản ứng, ta cần tính số mol muối FeCl2. Theo phương trình phản ứng, 1 mol Fe tương ứng với 1 mol FeCl2, nên số mol muối FeCl2 cũng là 0,1 mol. Khối lượng muối FeCl2 = số mol muối FeCl2 x khối lượng mol muối FeCl2 = 0,1 mol x (56g/mol + 2 x 35,5g/mol) = 0,1 mol x 127g/mol = 12,7g Vậy, khối lượng muối thu được sau phản ứng là 12,7g. c. Để xác định thể tích Hidro thu được sau phản ứng, ta cần tính số mol H2. Theo phương trình phản ứng, 1 mol Fe tương ứng với 1 mol H2, nên số mol H2 cũng là 0,1 mol. Thể tích H2 = số mol H2 x thể tích mol của H2 = 0,1 mol x 22,4 L/mol = 2,24 L Vậy, thể tích Hidro thu được sau phản ứng là 2,24 L.
Đúng 1
Bình luận (0)
a, \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{HCl}=2n_{Fe}=0,2\left(mol\right)\Rightarrow C_{M_{HCl}}=\dfrac{0,2}{0,1}=2\left(M\right)\)
b, \(n_{FeCl_2}=n_{H_2}=n_{Fe}=0,1\left(mol\right)\)
\(\Rightarrow m_{FeCl_2}=0,1.127=12,7\left(g\right)\)
c, \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 2,8g Fe bằng dung dịch HCl 10%.a. Tính V khí thoát ra (đkc)b. Tính khối lượng dung dịch acid HCl đã dùngc. Tính nồng độ phần trăm của dung dịch sau phản ứng
Đọc tiếp
Hòa tan hoàn toàn 2,8g Fe bằng dung dịch HCl 10%.
a. Tính V khí thoát ra (đkc)
b. Tính khối lượng dung dịch acid HCl đã dùng
c. Tính nồng độ phần trăm của dung dịch sau phản ứng
\(a)n_{Fe}=\dfrac{2,8}{56}=0,05mol\\ Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
0,05 0,1 0,05 0,05
\(V_{H_2\left(đktc\right)}=0,05.22,4=1,12l\\ b)m_{ddHCl}=\dfrac{0,1.36,5}{10}\cdot100=36,5g\\ c)C_{\%FeCl_2}=\dfrac{0,05.127}{2,8+36,5-0,05.2}\cdot100=16,2\%\)
Đúng 2
Bình luận (0)