cho 32g oxit sắt FexOy tác dụng đủ với 100ml dung dịch H2SO4 loãng ,sau phản ứng cô cạn dung dịch thu được 80g muối khan.Nồng độ mol/l của dung dịch H2so4 (giải bằng cách nhanh nhất vì đây là câu hỏi trắc nghiệm)

Những câu hỏi liên quan
cho 32g oxit sắt Fe\(_x\)O\(_y\) tác dụng đủ với 100ml dung dịch H\(_2\)SO\(_4\) loãng sau phản ứng cô cạn dung dịch thu đc 80g muối khan. Nồng độ mol/l của dd H2SO4 là:
A. 2M
B. 3M
C. 4M
D. 6M
Cho kim loại X (hóa trị III) tác dụng với dung dịch HCl vừa đủ rồi cô cạn dung dịch sau phản ứng, thu được a gam muối khan. Nếu lấy cùng lượng X như trên cho tác dụng với dd H2SO4 loãng vừa đủ rồi cô cạn dung dịch, thì thu được b gam muối khan. Lập biểu thức tính số mol X theo a, b.
\(n_{XCl_3}=\dfrac{a}{M_X+106,5}\left(mol\right)\)
PTHH: 2X + 6HCl --> 2XCl3 + 3H2
=> \(n_X=\dfrac{a}{M_X+106,5}\left(mol\right)\)
\(n_{X_2\left(SO_4\right)_3}=\dfrac{b}{2.M_X+288}\left(mol\right)\)
PTHH: 2X + 3H2SO4 --> X2(SO4)3 + 3H2
=> \(n_X=\dfrac{b}{M_X+144}\left(mol\right)\)
Câu 4: Cho 22,4g Fe tác dụng vừa đủ với 200g dung dịch H2SO4 loãng. Nồng độ % của dung dịch axít đã phản ứng là: Câu 5: Hoà tan một lượng sắt vào 400ml dung dịch HCl vừa đủ. Sau phản ứng thu được 3,36 lít khí hidrô (đktc). Nồng độ M của dung dịch HCl là: Câu 6: Cho 9,6 gam kim loại Magie vào 120 gam dung dịch HCl (vừa đủ). Nồng độ phần trăm của dung dịch sau phản ứng là :Help pls !!!!!!!!!!!!
Đọc tiếp
Câu 4: Cho 22,4g Fe tác dụng vừa đủ với 200g dung dịch H2SO4 loãng. Nồng độ % của dung dịch axít đã phản ứng là:
Câu 5: Hoà tan một lượng sắt vào 400ml dung dịch HCl vừa đủ. Sau phản ứng thu được 3,36 lít khí hidrô (đktc). Nồng độ M của dung dịch HCl là:
Câu 6: Cho 9,6 gam kim loại Magie vào 120 gam dung dịch HCl (vừa đủ). Nồng độ phần trăm của dung dịch sau phản ứng là :
Help pls !!!!!!!!!!!!
Câu 4:
Tính khối lượng của H2SO4 có trong dung dịch:
m = n x M x V
Trong đó:
n = 0,4 mol (số mol của H2SO4)
M = 98g/mol (khối lượng mol của H2SO4)
V = 200g (thể tích của dung dịch)
m = 0,4 mol x 98g/mol x 200g / 1000g = 7,84g
% = (khối lượng H2SO4 / khối lượng dung dịch) x 100 % = (7,84g / 200g) x 100 = 3,92% Vậy nồng độ % của dung dịch axít đã phản ứng là 3,92%.
Đúng 1
Bình luận (1)
C6
Mg + 2HCl -> MgCl2 + H2
m = n x M
n = m / M
Trong đó:
m = 9,6g (khối lượng của Mg)
M = 24,31g/mol (khối lượng mol của Mg)
n = 9,6g / 24,31g/mol = 0,395 mol
Mg + 2HCl -> MgCl2 + H2
Tỷ lệ phản ứng của Mg và HCl là 1:2, vì vậy số mol của HCl là 2 x 0,395 mol = 0,79 mol.
Để tính khối lượng của dung dịch sau phản ứng, ta cần biết khối lượng riêng của dung dịch HCl. Với dung dịch HCl có nồng độ 36,5%, khối lượng riêng xấp xỉ là 1,18 g/mL.
V = m / rho
V = 120g / 1,18 g/mL = 101,69 mL (thể tích của dung dịch)
m (HCl) = 0,79 mol x 36,5g/mol = 28,835 g (khối lượng của HCl sau phản ứng)
M (dung dịch sau phản ứng) = m + M(H2O) = 28,835g + 72g = 100,835g
% = (khối lượng chất tan / khối lượng dung dịch) x 100
% = (28,835g / 100,835g) x 100 = 28,62%
Vậy nồng độ phần trăm của dung dịch sau phản ứng là 28,62%.
Đúng 1
Bình luận (1)
`C4:`
`n_[Fe]=[22,4]/56=0,4(mol)`
`Fe+H_2 SO_4 ->FeSO_4 +H_2 \uparrow`
`0,4` `0,4` `(mol)`
`C%_[H_2 SO_4]=[0,4.98]/200 .100=19,6%`
`C5:`
`n_[H_2]=[3,36]/[22,4]=0,15(mol)`
`Fe+2HCl->FeCl_2 +H_2 \uparrow`
`0,3` `0,15` `(mol)`
`C_[M_[HCl]]=[0,3]/[0,4]=0,75(M)`
`C6:`
`n_[Mg]=[9,6]/24=0,4(mol)`
`Mg+2HCl->MgCl_2 +H_2 \uparrow`
`0,4` `0,8` `(mol)`
`C%_[HCl]=[0,8.36,5]/120 .100=24,3%`
Đúng 3
Bình luận (1)
Xem thêm câu trả lời
Bài 1. Cho 200ml dd KOH 0,5M tác dụng với 100ml dung dịch H2SO4 (x)M.
a. Viết PTHH của phản ứng hóa học xảy ra.
b. Tính nồng độ mol của dung dịch H2SO4 đã dùng.
c. Tính nồng độ mol của dung dịch muối thu được sau phản ứng.
PTHH: \(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
Ta có: \(n_{KOH}=0,2\cdot0,5=0,1\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4}=n_{K_2SO_4}=0,05\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{H_2SO_4}}=\dfrac{0,05}{0,1}=0,5\left(M\right)\\C_{M_{K_2SO_4}}=\dfrac{0,05}{0,2+0,1}\approx0,17\left(M\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Bài 1 :
200ml = 0,2l
100ml = 0,1l
\(n_{KOH}=0,5.0,2=0,1\left(mol\right)\)
a) Pt : \(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O|\)
2 1 1 2
0,1 0,05 0,05
b) \(n_{H2SO4}=\dfrac{0,1.1}{2}=0,05\left(mol\right)\)
\(C_{M_{ddH2SO4}}=\dfrac{0,05}{0,1}=0,5\left(M\right)\)
c) \(n_{K2SO4}=\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
\(V_{ddspu}=0,2+0,1=0,3\left(l\right)\)
\(C_{M_{K2SO4}}=\dfrac{0,05}{0,3}=\dfrac{1}{6}\left(M\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Cho 7.2g kim loại X có hóa trị 2 tác dụng vừa đủ với dung dịch H2SO4 loãng . Cô cạn dung dịch sau phản ứng thu được 36g muối . Hãy cho biết tên và kí hiệu hóa học
\(n_X=\dfrac{7,2}{M_X}\left(mol\right)\)
PTHH: X + H2SO4 --> XSO4 + H2
____\(\dfrac{7,2}{M_X}\)------------->\(\dfrac{7,2}{M_X}\)
\(\dfrac{7,2}{M_X}\left(M_X+96\right)=36=>M_X=24\left(Mg\right)\)
Đúng 1
Bình luận (0)
Cho 7,2 gam kim loại X có hóa trị II tác dụng vừa đủ với dung dịch H2SO4 loãng. Cô cạn dung dịch sau phản ứng thu được 36 gam muối. Hãy cho biết tên và kí hiệu hóa học của X.
\(X+H_2SO_4\rightarrow XSO_4+H_2\\Tacó: n_X=n_{XSO_4}\\ \Rightarrow\dfrac{7,2}{X}=\dfrac{36}{X+96}\\ \Rightarrow X=24\left(Magie-Mg\right)\)
Đúng 2
Bình luận (0)
\(n_X=\dfrac{7,2}{M_X}\left(mol\right)\)
PTHH: X + H2SO4 --> XSO4 + H2
____\(\dfrac{7,2}{M_X}\)----------->\(\dfrac{7,2}{M_X}\)
=> \(\dfrac{7,2}{M_X}\left(M_X+96\right)=36=>M_X=24\left(g/mol\right)\)
=> X là Mg (Magie)
Đúng 0
Bình luận (0)
Gọi x là số mol của kim loại X
PTHH: X + H2SO4 XSO4 + H2
Theo định luật bảo toàn khối lượng ta có:
mX + mH2SO4 = m muối + mH2
7,2 + 98x = 36 + 2x
x = 0,3 (mol)
MX = 7,2 : 0,3 = 24 (g/mol)
X là magie (Mg)
Đúng 0
Bình luận (0)
Cho một mẩu sắt tác dụng vủa đủ 200ml dung dịch axit H2SO4, sau khi phản ứng xảy ra hoàn toàn thu được 6,72 lít khí H2 ở đktc.a/ Tính khối lượng sắt đã dùng.b/ Tính nồng độ mol của dung dịch H2SO4 đã dùng.c/ Tính nồng độ mol của dung dịch muối thu được. Biết thể tích dung dịch thay đổi không đáng kể.
Đọc tiếp
Cho một mẩu sắt tác dụng vủa đủ 200ml dung dịch axit H2SO4, sau khi phản ứng xảy ra hoàn toàn thu được 6,72 lít khí H2 ở đktc.
a/ Tính khối lượng sắt đã dùng.
b/ Tính nồng độ mol của dung dịch H2SO4 đã dùng.
c/ Tính nồng độ mol của dung dịch muối thu được. Biết thể tích dung dịch thay đổi không đáng kể.
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
0,3 0,3 0,3 0,3
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(m_{Fe}=0,3.56=16,8\left(g\right)\)
\(C_{M_{H_2SO_4}}=\dfrac{n}{V}=\dfrac{0,3}{0,2}=1,5M\)
\(C_{M_{FeSO_4}}=\dfrac{n}{V}=\dfrac{0,3}{0,2}=1,5M\)
Đúng 2
Bình luận (0)
PTHH: Fe + H₂SO₄ --> FeSO₄ + H₂
200ml = 0,2 lít.
a) Số mol H₂: nH₂ = 6,72 ÷ 22,4 = 0,3 mol
Theo PTHH => Số mol Fe: nFe = 0,3 mol
=> Khối lượng Fe: mFe = 16,8g
b) Số mol H₂SO₄: nH₂SO₄ = 0,3 mol
Nồng độ mol dd: CM = 0,3 ÷ 0,2 = 1,5M
Đúng 0
Bình luận (0)
Cho một lượng sắt tác dụng vừa đủ với 300ml dung dịch H2SO4 1M
a. Tính khối lượng Fe đã tham gia phản ứng
b. Tính V khí thoát ra ở đktc
c. Tính nồng độ mol/l của dung dịch muối thu được sau phản ứng
\(n_{H_2SO_4}=0.3\cdot1=0.3\left(mol\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(0.3.....0.3..............0.3...........0.3\)
\(m_{Fe}=0.3\cdot56=16.8\left(g\right)\)
\(V_{H_2}=0.3\cdot22.4=6.72\left(l\right)\)
\(C_{M_{FeSO_4}}=\dfrac{0.3}{0.3}=1\left(M\right)\)
Đúng 0
Bình luận (0)
Cho 10,2 gam hỗn hợp X gồm Al và Mg tác dụng với dung dịch H2SO4 loãng, dư thu được 11,2 lít khí hiđro (đktc). Cô cạn dung dịch sau phản ứng, khối lượng muối khan thu được là A. 43,6 gam. B. 81,7 gam. C. 85,4 gam. D. 58,2 gam.
Đọc tiếp
Cho 10,2 gam hỗn hợp X gồm Al và Mg tác dụng với dung dịch H2SO4 loãng, dư thu được 11,2 lít khí hiđro (đktc). Cô cạn dung dịch sau phản ứng, khối lượng muối khan thu được là
A. 43,6 gam.
B. 81,7 gam.
C. 85,4 gam.
D. 58,2 gam.
Đáp án D
Số mol H2 thu được là : n H 2 = 11 , 2 22 , 4 = 0 , 5 mol
Gọi M là kim loại chung cho Al và Mg với hóa trị n
Sơ dồ phản ứng :
M ⏟ 10 , 2 gam + H 2 S O 4 ( l o ã n g , d ư ) → M 2 ( S O 4 ) n ⏟ m u ố i + H 2 ↑ ⏟ 0 , 5 m o l
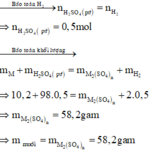
Đúng 0
Bình luận (0)































