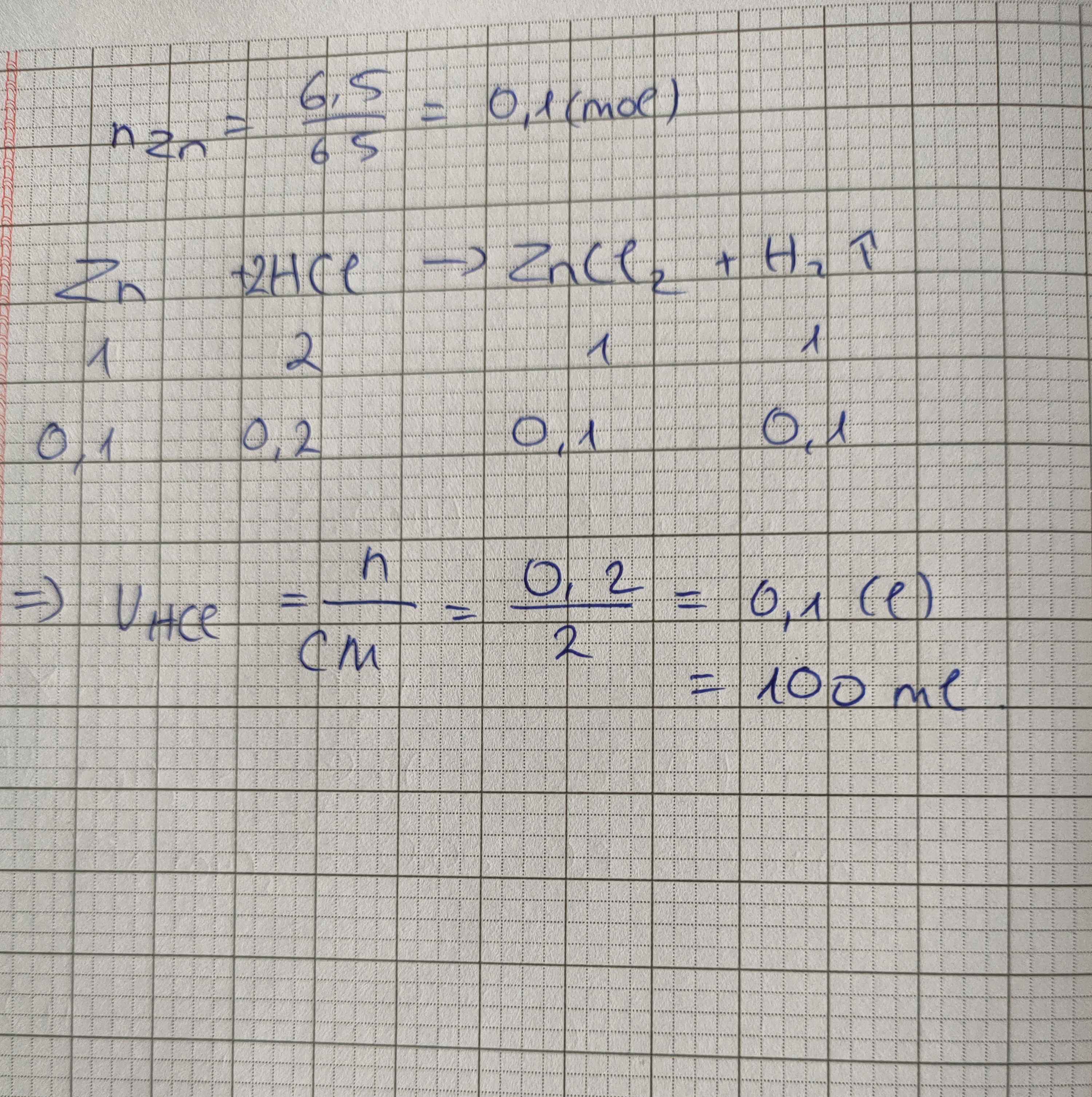Để hoà tan 6,5 g kẽm cần dùng bao nhiêu ml dung dịch HCl 2M ? tính C(M) của dd thu được

Những câu hỏi liên quan
a. Biết gam. Hãy tính nồng độ phần trăm của dung dịch NaCl bão hòa ở nhiệt độ này.b.Để hoà tan 6,5 g kẽm cần dùng bao nhiêu ml dung dịch HCl 2M ?
Đọc tiếp
a. Biết ![]() gam. Hãy tính nồng độ phần trăm của dung dịch NaCl bão hòa ở nhiệt độ này.
gam. Hãy tính nồng độ phần trăm của dung dịch NaCl bão hòa ở nhiệt độ này.
b.Để hoà tan 6,5 g kẽm cần dùng bao nhiêu ml dung dịch HCl 2M ?
để hòa tan 6,5 g kẽm cần dùng bao nhiêu ml dung dịch hcl 2m
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 ( mol )
\(V_{HCl}=\dfrac{0,2}{2}=0,1l\)
Đúng 3
Bình luận (0)
Xem thêm câu trả lời
cho 6,5 g hỗn hợp kẽm vào 200 ml dd hcl 2m thu được bao nhiêu lít khí ở đktc ? Gấp ạ
\(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(n_{HCl}=0.2\cdot2=0.4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Ta có :
\(\dfrac{0.1}{1}< \dfrac{0.4}{2}\rightarrow HCldư\)
\(n_{H_2}=0.1\left(mol\right)\)
\(V=0.1\cdot22.4=2.24\left(l\right)\)
Đúng 1
Bình luận (1)
Bài 1: Hoà tan 21,7 gam Na2O vào nước thu được 400 ml dung dịch A.
a. Nêu hiện tượng xảy ra khi nhúng quì tím vào dd A? Giải thích?
b. Tính nồng độ mol của A?
Bài 2: Người ta dung dung dịch HCl 1,5M để hòa tan hoàn toàn a (g) kẽm, sau phản ứng thu được 3,36 lit khí H2 (đktc)
a.Tính a?
b.Tính thể tích dung dịch HCl cần dùng?
Bài1:
a,Vì dd A là dd bazo nên làm cho quỳ tím đổi thành màu xanh
b,\(n_{Na_2O}=\dfrac{21,7}{62}=0,35\left(mol\right)\)
PTHH: Na2O + H2O → 2NaOH
Mol: 0,35 0,7
\(\Rightarrow C_{M_{ddNaOH}}=\dfrac{0,7}{0,4}=1,75M\)
Đúng 3
Bình luận (1)
Bài 2:
a,\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,15 0,3 0,15
⇒ a=mZn = 0,15.65 = 9,75 (g)
b,\(V_{HCl}=\dfrac{0,3}{1,5}=0,2\left(l\right)=200\left(ml\right)\)
Đúng 3
Bình luận (1)
Để hoà tan hoàn toàn 6,5 g Zn cần vừa đủ 200g dung dịch HCl x%: Tính thể tích khí thu được Tính C% dung dịch thu được sau phản ứng
\(n\) \(Zn\) \(=\frac{6,5}{65}=0,1\left(mol\right)\)
Ta có:
\(Zn+2HCL\rightarrow ZnCL2+H2\)
\(0,1\rightarrow0,1\rightarrow0,1\)
a) \(V\) \(H2\)\(=22,4.0,1=2,24\left(g\right)\))
b) Ta có :
m dd s.p.ư = m Zn + m dd HCl - m H2
= 6,5 + 200 - 22,4 * 0,1
= 204,26 (g)
m ZnCl2 = 136 * 0,1 = 13,6 (g)
=> C% ZnCl2 = 13,6 / 204,26 * 100 = ~6,66%
Đúng 0
Bình luận (0)
n Zn = 6,5 / 65 = 0,1 (mol)
Ta có:
Zn + 2HCl -> ZnCl2 + H2
0,1 -> 0,1 -> 0,1
a) V H2 = 22,4 * 0,1 = 2,24 (g)
b) Ta có :
m dd s.p.ư = m Zn + m dd HCl - m H2
= 6,5 + 200 - 22,4 * 0,1
= 204,26 (g)
m ZnCl2 = 136 * 0,1 = 13,6 (g)
=> C% ZnCl2 = 13,6 / 204,26 * 100 = ~6,66%
Đúng 0
Bình luận (1)
Để hoà tan hoàn toàn hỗn hợp X gồm 11,2g Fe và 4,8g Fe2O3 cần dùng tối thiểu V ml dung dịch HCl 2M, thu được dung dịch Y. Cho dung dịch AgNO3 dư vào Y, thu được m gam kết tủA. Giá trị của V và m lần lượt là A. 290 và 83,23 B. 260 và 102,7 C. 290 và 104,83 D. 260 và 74,62
Đọc tiếp
Để hoà tan hoàn toàn hỗn hợp X gồm 11,2g Fe và 4,8g Fe2O3 cần dùng tối thiểu V ml dung dịch HCl 2M, thu được dung dịch Y. Cho dung dịch AgNO3 dư vào Y, thu được m gam kết tủA. Giá trị của V và m lần lượt là
A. 290 và 83,23
B. 260 và 102,7
C. 290 và 104,83
D. 260 và 74,62
Đáp án B
nFe2O3 = 0,03; nFe = 0,2
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
0,03 → 0,18 → 0,06
Fe + 2FeCl3 → 3FeCl2
0,03 ← 0,06 → 0,09
Fe + 2HCl → FeCl2 + H2
0,17 → 0,34 → 0,17
=> nHCl = 0,18 + 0,34 = 0,52 => V = 0,26 lít
nAg = nFe2+ = nFe + 2nFe2O3 = 0,26; nAgCl = nHCl = 0,52
=> m = 0,26.108 + 0,52.143,5 = 102,7
Đúng 0
Bình luận (0)
Hoà tan 6,5 gam kẽm cần vừa đủ 200ml dd HCl 2M Tính số mol HCl tham gia phản ứng ?
Đọc tiếp
Hoà tan 6,5 gam kẽm cần vừa đủ 200ml dd HCl 2M
Tính số mol HCl tham gia phản ứng ?
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ n_{HCl}=0,2.2=0,4\left(mol\right)\\ Zn+2HCl\xrightarrow[]{}ZnCl_2+H_2\\ \Rightarrow\dfrac{0,1}{1}< \dfrac{0,4}{2}\Rightarrow HCl.dư\\ n_{HCl\left(pư\right)}=0,1.2=0,2\left(mol\right)\)
Đúng 2
Bình luận (0)
Hoà tan 13 g kẽm bằng 250 g dung dịch axit HCl vừa đủ.
a. Tính thể tích hiđro thoát ra ở đktc.
b. Tính khối lượng muối thu được sau phản ứng.
c. Tính nồng độ phần trăm của dung dịch axit HCl cần dùng.
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,2 0,4 0,2 0,2
a) \(n_{H2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
b) \(n_{ZnCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{ZnCl2}=0,2.136=27,2\left(g\right)\)
c) \(n_{HCl}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
⇒ \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(C_{ddHCl}=\dfrac{14,6.100}{250}=5,84\)0/0
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Giúp em với ạ b) Tính khối lượng CuO cần lấy để phản ứng vừa đủ 200 ml dung dịch HCl 2M. c) Tính thể tích dung dịch H2SO4 2M cần lấy để hoà tan hết 16,2 gam ZnO. d) Để trung hòa hết 100 ml H2SO4 2M cần dùng V ml dung dịch KOH 1M. Tính V.
b,\(n_{HCl}=0,2.2=0,4\left(mol\right)\)
PTHH: CuO + 2HCl → CuCl2 + H2
Mol: 0,2 0,4
\(\Rightarrow m_{CuO}=0,2.80=16\left(g\right)\)
c,\(n_{ZnO}=\dfrac{16,2}{81}=0,2\left(mol\right)\)
PTHH: ZnO + H2SO4 → ZnSO4 + H2
Mol: 0,2 0,2
\(\Rightarrow V_{ddH_2SO_4}=\dfrac{0,2}{2}=0,1\left(l\right)\)
d,\(n_{H_2SO_4}=2.0,1=0,2\left(mol\right)\)
PTHH: H2SO4 + 2KOH → K2SO4 + 2H2O
Mol: 0,2 0,4
\(\Rightarrow V_{ddKOH}=\dfrac{0,4}{1}=0,4\left(l\right)\)
Đúng 1
Bình luận (0)