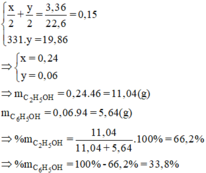8/ Hỗn hợp A gồm phenol C6H5OH và etanol. Cho mg A tác dụng với Na dư, thu đc 25,2g muối và khí hidro( đktc). Mặt khác, mg A tác dụng vừa đủ với 100ml dd KOH 1M. Tính V ?

Những câu hỏi liên quan
4/ Hỗn hợp A gồm phenol C6H5OH và etanol. Cho mg A tác dụng với Na dư, thu được 12,6g muối và V lít khí H2 ( đktc). Mặt khác, m gam A tác dụng vừa đủ với 50ml dd KOH 1M. Tính V ?
Gọi số mol của C6H5OH và C2H5OH trong m gam A lần lượt là x và y.
Khi cho m gam A tác dụng vừa đủ với KOH thì chỉ phenol phản ứng
C6H5OH + KOH → C6H5OK + H2O
=> nC6H5OH = nKOH = 0,05.1 = 0,05 mol
Khi m gam A phản ứng với Na dư:
C6H5OH + Na → C6H5ONa + 1/2H2
C2H5OH + Na → C2H5ONa + 1/2H2
mMuối = mC6H5ONa + mC2H5ONa = 0,05.116 + 68y = 12,6
=> y = 0,1 mol
=> nH2 = (0,05 + 0,1):2 = 0,075 mol
<=> V H2 = 0,075.22,4 = 1,68 lít
Đúng 0
Bình luận (0)
nung 10,2g hỗn hợp Al, Mg, Na trong khí õi dư. sau Phản ứng kết thúc thu được 17g hỗn hợp chất rắn. mặt khác cho hỗn hợp kim loại trên tác dụng với đ HCl dư thì thấy thoát ra V lít khí và dd A. cô cạn A thì thu đc m gam muối Clorua khan. tính V và m
Coi hỗn hợp kim loại trên là R có hóa trị n
\(4R + nO_2 \xrightarrow{t^o} 2R_2O_n\\ m_{O_2} = 17-10,2 = 6,8(gam) \Rightarrow n_{O_2} = \dfrac{6,8}{32} = 0,2125(mol)\\ n_R = \dfrac{4}{n}n_{O_2} = \dfrac{0,85}{n}(mol)\\ 2R + 2nHCl \to 2RCl_n + nH_2\\ n_{H_2} = \dfrac{n}{2}n_R = 0,425(mol)\\ \Rightarrow V = 0,425.22,4 = 9,52(lít)\\ n_{HCl} = 2n_{H_2} = 0,85(mol)\\ \text{Bảo toàn khối lượng : }\\ m_{muối} = m_{kim\ loại} + m_{HCl} - m_{H_2} = 10,2 + 0,85.36,5 - 0,425.2 = 40,375(gam)\)
Đúng 1
Bình luận (0)
Cho hỗn hợp X gồm etanol và phenol tác dụng với natri (dư) thu được 3,36 lít khí hidro (đktc). Nếu cho hỗn hợp X trên tác dụng với dung dịch nước brom vừa đủ thu được 19,86 gam kết tủa trắng. Phần trăm khối lượng của etanol trong X là: A. 66,19%. B. 20%. C. 80%. D. 33,81%.
Đọc tiếp
Cho hỗn hợp X gồm etanol và phenol tác dụng với natri (dư) thu được 3,36 lít khí hidro (đktc). Nếu cho hỗn hợp X trên tác dụng với dung dịch nước brom vừa đủ thu được 19,86 gam kết tủa trắng. Phần trăm khối lượng của etanol trong X là:
A. 66,19%.
B. 20%.
C. 80%.
D. 33,81%.
Cho m gam hỗn hợp Al và Fe tác dụng vừa đủ với dd HCl 2M, thu đc dd muối A và 1,456lits H2 ở đktc. Mặt khác cho lượng hỗn hợp trên tác dụng với dd NaOH dư, thu đc 1,12 g chất rắn không tan.
a) tính khối lượng và% khối lượng mỗi chất trong hỗn hợp nói trên
b) tính khối lượng muối thu đc trong ddA
a) \(2Al+6HCl\rightarrow2AlCl_3+3H_2\left(1\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\\ 2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
Cho hỗn hợp tác dụng với NaOH, chất rắn không tan là Fe
=> mFe= 1,12 (g) \(\Rightarrow n_{Fe}=0,02\left(mol\right)\)
Ta có: \(n_{H_2\left(2\right)}=n_{Fe}=0,02\left(mol\right)\)
=> \(n_{H_2\left(1\right)}=\Sigma n_{H_2}-n_{H_2\left(2\right)}=0,065-0,02=0,045\left(mol\right)\)
\(\Rightarrow n_{Al}=\dfrac{2}{3}n_{H_2\left(1\right)}=0,03\left(mol\right)\)
\(\Rightarrow m_{Al}=0,03.27=0,81\left(g\right)\)
\(\Rightarrow\%m_{Al}=41,97\%,\%m_{Fe}=58,03\%\)
b) \(m_{FeCl_2}=0,02.127=2,54\left(g\right)\\ m_{AlCl_3}=0,03.133,5=4,005\left(g\right)\)
Đúng 0
Bình luận (0)
Tính khối lượng dd sau phản ứng. a, cho 12.3 g hỗn hợp al mg zn tác dụng với vừa đủ dd h2so4 9% thu được 7.84 lít khí h2 đktc B, cho 16.2 g hỗn hợp gồm mg al fe tác dụng với vừa đủ dd h2so4 25% thu được 12.32 lít khí h2 đktc
a) Sửa đề: dd H2SO4 9,8%
Ta có: \(n_{H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\) \(\Rightarrow m_{H_2}=0,35\cdot2=0,7\left(g\right)\)
Bảo toàn nguyên tố: \(n_{H_2SO_4}=n_{H_2}=0,35\left(mol\right)\) \(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,35\cdot98}{9,8\%}=350\left(g\right)\)
\(\Rightarrow m_{dd}=m_{KL}+m_{H_2SO_4}-m_{H_2}=361,6\left(g\right)\)
b) Tương tự câu a
Đúng 1
Bình luận (0)
Cho hỗn hợp gồm etanol và phenol tác dụng với natri (dư) thu được 3,36 lít khí hidro ở đktc. Nếu cho hỗn hợp trên tác dụng với dung dịch nước brom vừa đủ thu được 19,86 gam kết tủa trắng của 2,4,6-tribromphenol
Tính thành phần phần trăm khối lượng của mỗi chất trong hỗn hợp đã dùng.
cho 70,2 g hỗn hợp gồm etanol và phenol tác dụng với Na (dư) thu được 10,08 lít khí H2 (đktc) .Cũng hỗn hợp trên tác dụng vừa đủ V (ml) dung dịch NaOH 0,5 M
a) viết phương trình của những phản ứng xay ra
b) tính khối lượng cua mỗi chất trong hỗn hơp đã dùng
c)tính thể tích dung dich NaOH đã phản ứng
(Cho biết NTK:Br=80; Ag= 108; Na=23 ;Ca=40; C=12; O=16;H=1;Cu=64;N=14
`a)PTHH:`
`C_2 H_5 OH+Na->C_2 H_5 ONa+1/2H_2 \uparrow`
`C_6 H_5 OH+Na->C_6 H_5 ONa+1/2H_2 \uparrow`
`C_6 H_5 OH+NaOH->C_6 H_5 ONa+H_2 O`
`b)n_[H_2]=[10,08]/[22,4]=0,45(mol)`
Gọi `n_[C_2 H_5 OH]=x;n_[C_6 H_5 OH]=y`
`=>` $\begin{cases} 46x+94y=70,2\\\dfrac{1}{2}x+\dfrac{1}{2}=0,45 \end{cases}$
`<=>` $\begin{cases} x=0,3\\y=0,6 \end{cases}$
`@m_[C_2 H_5 OH]=0,3.46=13,8(g)`
`@m_[C_6 H_5 OH]=70,2-13,8=56,4(g)`
`c)V_[dd NaOH]=[0,6]/[0,5]=1,2(M)`
Đúng 1
Bình luận (0)
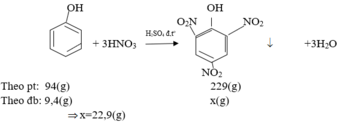
Cho 14,0 gam hỗn hợp A gồm phenol và etanol tác dụng với natri dư thu được 2,24 lít khí hidro (đktc)
Cho 14,0 gam hỗn hợp A tác dụng với HNO3 thì thu được bao nhiêu gam axit picric (2,4,6- trinitrophenol)?
Cho 14 gam hỗn hợp A gồm etanol và phenol tác dụng với Na dư thu được 2,24 lít khí H2 (đktc). Phần trăm khối lượng của etanol và phenol trong hỗn hợp lần lượt là A. 32,85% và 67,15%. B. 39,00% và 61,00%. C. 40,53% và 59,47%. D. 60,24% và 39,76%.
Đọc tiếp
Cho 14 gam hỗn hợp A gồm etanol và phenol tác dụng với Na dư thu được 2,24 lít khí H2 (đktc). Phần trăm khối lượng của etanol và phenol trong hỗn hợp lần lượt là
A. 32,85% và 67,15%.
B. 39,00% và 61,00%.
C. 40,53% và 59,47%.
D. 60,24% và 39,76%.
Chọn đáp án A
Đặt nC2H5OH = x; nC6H5OH = y ⇒ mA = 14(g) = 46x + 94y.
nH2 = 0,5x + 0,5y = 0,1 mol ||⇒ giải hệ có: x = y = 0,1 mol.
► %metanol = 0,1 × 46 ÷ 14 × 100% = 32,86% ⇒ %mphenol = 67,14%.
Đúng 0
Bình luận (0)