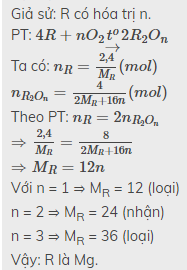Đốt cháy hoàn toàn 2,4g kim loại M thu đc 4g oxit.Xác định tên kim loại M và công thức của oxit

Những câu hỏi liên quan
Đốt cháy hết 2,4g một kim loại R(II) thu đc 4g oxit của nó.
xác định kim loại.
Áp dụng ĐLBTKL:
\(m_{O_2}=4-2,4=1,6\left(g\right)\\ \rightarrow n_{O_2}=\dfrac{1,6}{32}=0,05\left(mol\right)\)
PTHH: \(2R+O_2\xrightarrow[]{t^o}2RO\)
0,1<-0,05
\(\rightarrow M_R=\dfrac{2,4}{0,1}=24\left(g\text{/}mol\right)\)
=> R là Mg
Đúng 1
Bình luận (0)
Đốt cháy một kim loại R hóa trị (||) trong bình chứa 4,48 lit khí oxi (đktc) thu đc 16g oxit.Xác định R và công thức hóa học của oxit đos?
2R + O2 -to-> 2RO
.........0.2...........0.4
M = 16/0.4 = 40 (đvc)
=> R + 16 = 40
=> R = 24
CT : MgO
Đúng 1
Bình luận (1)
Đốt cháy hoàn toàn 2,4 gam một kim loại đơn hóa trị ta thu được 4g oxit .Xác định tên kim loại đó
Gọi kim loại cần tìm là R
$4R + nO_2 \xrightarrow{t^o} 2R_2O_n$
Theo PTHH :
$n_R = 2n_{R_2O_n}$
$\dfrac{2,4}{R} = \dfrac{4}{2R + 16n}.2$
$\Rightarrow R = 12n$
Với n = 2 thì R = 24(Magie)
Đúng 3
Bình luận (1)
KL A hóa trị x (x: nguyên, dương)
PTHH: 4 A + x O2 -to-> 2 A2Ox
mO2=4-2,4=1,6(g)
=> nO2= 0,05(mol)
=> nA= (0,05.4)/x= 0,2/x(mol)
=>M(A)= 2,4: (0,2/x)= 12x
Với x=1 =>M(A)=12 (loại)
Với x=2 =>M(A)=24(A là Mg)
Với x=3 =>M(A)=36 (loại)
Với x=8/3 =>M(A)=32 (loại)
=> Kim loại cần tìm là magie. (Mg=24)
Đúng 2
Bình luận (1)
Khử hoàn toàn 24 gam oxit kim loại M bằng khí Z dư, thu được 16,8 gam kim loại M. Xác định tên kim loại M và công thức của oxit kim loại M.
Giả sử Z là H2
\(n_{M_2O_n}=\dfrac{24}{2.M_M+16n}\left(mol\right)\)
PTHH: M2On + nH2 --to--> 2M + nH2O
\(\dfrac{24}{2.M_M+16n}\)------>\(\dfrac{24}{M_M+8n}\)
=> \(\dfrac{24}{M_M+8n}.M_M=16,8\)
=> \(M_M=\dfrac{56}{3}n\left(g/mol\right)\)
Xét n = 3 thỏa mãn => MM = 56 (g/mol)
=> M là Fe (Sắt)
CTHH của oxit là Fe2O3
Đúng 5
Bình luận (0)
\(n_{M_2O_n}=\dfrac{24}{2.M_M+16n}\left(mol\right)\)
PTHH: M2On + nH2 --to--> 2M + nH2O
\(\dfrac{24}{2.M_M+16n}\)------>\(\dfrac{24}{M_M+8n}\)
=> \(\dfrac{24}{M_M+8n}.M_M=16,8\)
=> \(M_M=\dfrac{56}{3}n\left(g/mol\right)\)
Xét n = 3 thỏa mãn => MM = 56 (g/mol)
=> M là Fe (Sắt)
CTHH của oxit là Fe2O3
1.Đốt cháy hoàn toàn 10,8g môt kim loại chưa rõ hóa trị, sau phản ứng thu đươhc 20,4g một oxit. Hãy xác định công thức hóa học của kim loại.2.Đốt cháy hoàn toàn 8,4g môt kim loại chưa rõ hóa trị, sau phản ứng thu được 16,6 g một oxit. Hãy xác định công thức hóa học của kim loại3.Cho 2,7g Al vào đung dịch có chứa 16,1g HCla.Viết PTHH của phản ứngb.Chất nào dư? Tính khối lượng dư.c.Nếu dùng toàn bộ thể tích khí H2 trên để khử 30g Đồng(II) oxit, hãy tính khối lượng chất rắn thu được sau phản ứng.gi...
Đọc tiếp
1.Đốt cháy hoàn toàn 10,8g môt kim loại chưa rõ hóa trị, sau phản ứng thu đươhc 20,4g một oxit. Hãy xác định công thức hóa học của kim loại.
2.Đốt cháy hoàn toàn 8,4g môt kim loại chưa rõ hóa trị, sau phản ứng thu được 16,6 g một oxit. Hãy xác định công thức hóa học của kim loại
3.Cho 2,7g Al vào đung dịch có chứa 16,1g HCl
a.Viết PTHH của phản ứng
b.Chất nào dư? Tính khối lượng dư.
c.Nếu dùng toàn bộ thể tích khí H2 trên để khử 30g Đồng(II) oxit, hãy tính khối lượng chất rắn thu được sau phản ứng.
giúp em sáng 6h nộp rồi ạ
Câu 1:
Giả sử KL là A có hóa trị n.
PT: \(4A+nO_2\underrightarrow{t^o}2A_2O_n\)
Ta có: \(n_A=\dfrac{10,8}{M_A}\left(mol\right)\), \(n_{A_2O_n}=\dfrac{20,4}{2M_A+16n}\left(mol\right)\)
Theo PT: \(n_A=2n_{A_2O_3}\Rightarrow\dfrac{10,8}{M_A}=\dfrac{2.20,4}{2M_A+16n}\Rightarrow M_A=9n\left(g/mol\right)\)
Với = 3 thì MA = 27 (g/mol) là thỏa mãn.
Vậy: A là Al.
Câu 2:
Giả sử KL cần tìm là A có hóa trị n.
PT: \(4A+nO_2\underrightarrow{t^o}2A_2O_n\)
Ta có: \(n_A=\dfrac{8,4}{M_A}\left(mol\right)\), \(n_{A_2O_n}=\dfrac{16,6}{2M_A+16n}\left(mol\right)\)
Theo PT: \(n_A=2n_{A_2O_n}\Rightarrow\dfrac{8,4}{M_A}=\dfrac{2.16,6}{2M_A+16n}\Rightarrow M_A=\dfrac{336}{41}n\)
→ vô lý
Bạn xem lại đề câu này nhé.
Câu 3:
a, \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
b, \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
\(n_{HCl}=\dfrac{16,1}{36,5}=\dfrac{161}{365}\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1}{2}< \dfrac{\dfrac{161}{365}}{6}\), ta được HCl dư.
THeo PT: \(n_{HCl\left(pư\right)}=3n_{Al}=0,3\left(mol\right)\)
\(\Rightarrow n_{HCl\left(dư\right)}=\dfrac{161}{365}-0,3=\dfrac{103}{730}\left(mol\right)\Rightarrow m_{HCl\left(dư\right)}=\dfrac{103}{365}.36,5=5,15\left(g\right)\)
c, \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,15\left(mol\right)\), \(n_{CuO}=\dfrac{30}{80}=0,375\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,375}{1}>\dfrac{0,15}{1}\), ta được CuO dư.
Theo PT: \(n_{CuO\left(pư\right)}=n_{Cu}=n_{H_2}=0,15\left(mol\right)\Rightarrow n_{CuO\left(dư\right)}=0,375-0,15=0,225\left(mol\right)\)
⇒ m chất rắn = mCu + mCuO (dư) = 0,15.64 + 0,225.80 = 27,6 (g)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 9,2 g một mẩu kim loại M hóa trị 1 trong khí Oxi thì thu được 12,4 g một oxit của kim loại M. tìm tên nguyên tố M và CTHH của oxit
\(n_M=\dfrac{9,2}{M_M}\left(mol\right)\)
PTHH: 4M + O2 --to--> 2M2O
\(\dfrac{9,2}{M_M}\)---------->\(\dfrac{4,6}{M_M}\)
=> \(\dfrac{4,6}{M_M}\left(2.M_M+16\right)=12,4\)
=> MM = 23 (g/mol)
=> M là Na (Natri)
CTHH của oxit là Na2O
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 3,9 gam một kim loại M hóa trị I thu được 4,7 gam một oxit A.
a) Cho biết A thuộc loại oxit nào?
b) Tìm tên kim loại M và cho biết bazơ tương ứng của oxit A
Cậu tham khảo:
a) A là oxit bazơ vì M là kim loại
b)
4M+O2--->2M2O
mO2=mM2O-mM=4,7-3,9=0,8(g)
=>nO2=0,8/32=0,025(mol)
Theo pt: nM=4nO2=4.0,025=0,1(mol)
=>MM=3,9/0,1=39
=>M là K
=>Bazơ tương ứng của A KOH
Đúng 2
Bình luận (1)
Đốt cháy hoàn toàn 15,68g kim loại M trong bình đựng khí clo dư thu được 45,5g muối cloruaa) Xác định tên kim loại Mb) Để hòa tan hoàn toàn 9,2g hỗn hợp X gồm kim loại M và một oxit của kim loại M cần dùng vừa hết 160ml dung dịch HCl 2M,còn neeusndaax luồng H2 dư đi qua 9,2g hỗn hợp X nung nóng,sau khi phản ứng xảy ra hoàn toàn thu được 7,28g chắt răn.Tìm CT của oxit kim loại trong hỗn hợp
Đọc tiếp
Đốt cháy hoàn toàn 15,68g kim loại M trong bình đựng khí clo dư thu được 45,5g muối clorua
a) Xác định tên kim loại M
b) Để hòa tan hoàn toàn 9,2g hỗn hợp X gồm kim loại M và một oxit của kim loại M cần dùng vừa hết 160ml dung dịch HCl 2M,còn neeusndaax luồng H2 dư đi qua 9,2g hỗn hợp X nung nóng,sau khi phản ứng xảy ra hoàn toàn thu được 7,28g chắt răn.Tìm CT của oxit kim loại trong hỗn hợp
Đốt cháy 2,4g một kim loại đơn hóa trị thu đc 4g oxit. Xác định tên kim loại đó.?
Pt : M + O2 -> M2On (với n là hóa trị của kim loại M )
Ta có : mO2= mOxit - mkl=4- 2,4=1,6 (g)
=> NO2=0,1 mol
Từ pt =>NM=NO2=0,1 mol
=>M=m/N=2,4/0,1=24 -> M là Mg
Đúng 1
Bình luận (0)
Gọi kim loại cần tìm là M. Đặt MM = M (g/mol).
PTHH: \(4M+xO_2\underrightarrow{t^o}2M_2O_x\)
Theo ĐLBTKL :
\(m_{O_2}=4-2,4=1,6\left(g\right)\)
=> \(n_{O_2}=\frac{1,6}{32}=0,05\left(mol\right)\)
Theo PT : nM =\(\frac{4}{x}.n_{O_2}=\frac{4}{x}.0,05=\frac{0,2}{x}\left(mol\right)\)
=> M = \(\frac{2,4}{\frac{0,2}{x}}=12x\)(g/mol)
Chỉ có cặp nghiệm x = 2 , M =24 là thỏa mãn.
=> M là Magie (Mg)
Đúng 0
Bình luận (0)
Gọi kim loại là M ,có hóa trị x,ta có PTHH
4M +xO2->2M2Ox
Theo PTHH:2.nM2Ox=>2,4/M=2.4/2M +16x =>4,8M+38,4x=8M
3,2M=38,4x=>M=12x
+, Nếu x=1 => M=12 ( loại)
+, Nếu x =2 =>M=24
+, Nếu x=3 =>M=36 ( loại)
Vậy M=24 ( đvC) là Magie ( Mg)
Đúng 0
Bình luận (0)