
Những câu hỏi liên quan
Viết CTT hóa học của những chất sau:
Kali hiđro cacbonat, canxi sunfat, axit nitric, đồng (II) hyđroxit, kẽm nitrat, sắt
(III) oxit, axit brom hiđric, chì (II) clorua, nhôm sunfat, kali hyđroxit, bari photphat, nhôm cacbonat, cacbon đioxit, crôm trioxit, nhôm clorua, canxi đihiđro photphat, đinitơtrioxit, axit sunfuhiđric, magie oxit, axit sunfurơ, sắt (III) hiđroxit, mangan (VII) oxit,kali bromua.
KHCO3, CaSO4, HNO3, Cu(OH)2, Zn(NO3)2, Fe2O3, HBr, PbCl2, Al2(SO4)3, KOH, Ba3(PO4)2, Al2(CO3)3, CO2, CrO3, AlCl3, Ca(H2PO4)2, N2O3, H2SO4, MgO, H2SO3, Fe(OH)3, MnO2, KBr
Đúng 2
Bình luận (0)
Viết các phương trình hóa học biểu diễn sự cháy trong oxi của các đơn chất: cacbon, photpho, hidro, nhôm biết rằng sản phẩm lần lượt là những hợp chất có công thức hóa học: CO2, P2O5, H2O, Al2O3. Hãy gọi tên các sản phẩm.
\(C+O_2\underrightarrow{t^0}CO_2\) ( Cacbon dioxit)
\(4P+5O_2\underrightarrow{t^0}2P_2O_5\)( Diphotpho pentaoxit)
\(H_2+\dfrac{1}{2}O_2\underrightarrow{t^0}H_2O\) ( Nước hay dihidro monooxit)
\(4Al+3O_2\underrightarrow{t^0}2Al_2O_3\) ( Nhôm oxit)
Đúng 1
Bình luận (1)
C + O2 --to--> CO2 (Khí cacbonic)
4P + 5O2 --tO--> 2P2O5 (đi photpho pentaoxit)
H + O2 --to--> H2O (Nước)
4Al + 3O2 --to--> 2Al2O3 (Nhôm oxit)
Đúng 1
Bình luận (0)
Viết các phương trình hóa học biểu diễn sự cháy trong oxi của các đơn chất: cacbon, photpho, hiđro, nhôm biết rằng sản phẩm là những hợp chất lần lượt có công thức hóa học là CO2, P2O5, H2O, Al2O3. Hãy gọi tên các chất tạo thành.
C + O2 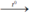 CO2. Cacbon đioxit.
CO2. Cacbon đioxit.
4P + 5O2 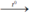 2P2O5. Điphotpho pentaoxit.
2P2O5. Điphotpho pentaoxit.
2H2 + O2 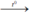 2H2O. Nước.
2H2O. Nước.
4Al + 3O2 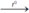 2Al2O3. Nhôm oxit.
2Al2O3. Nhôm oxit.
Đúng 1
Bình luận (0)
Bài 1: Viết các phương trình hóa học biểu diễn sự cháy trong oxi của các đơn chất: cacbon, photpho, hiđro, nhôm biết rằng sản phẩm là những hợp chất lần lượt có công thức hóa học là CO2, P2O5, H2O, Al2O3. Hãy gọi tên các chất tạo thành. Bài 8: Để chuẩn bị cho buổi thí nghiệm thực hành của lớp cần thu 20 lọ khí oxi, mỗi lọ có dung tích 100ml. a) Tính khối lượng kali pemanganat phải dùng, giả sử khí oxi thu được ở điều kiện tiêu chuẩn và hao hụt 10%?b) Nếu dùng kali clorat có thêm một lượng nhỏ Mn...
Đọc tiếp
Bài 1: Viết các phương trình hóa học biểu diễn sự cháy trong oxi của các đơn chất: cacbon, photpho, hiđro, nhôm biết rằng sản phẩm là những hợp chất lần lượt có công thức hóa học là CO2, P2O5, H2O, Al2O3. Hãy gọi tên các chất tạo thành.
Bài 8: Để chuẩn bị cho buổi thí nghiệm thực hành của lớp cần thu 20 lọ khí oxi, mỗi lọ có dung tích 100ml.
a) Tính khối lượng kali pemanganat phải dùng, giả sử khí oxi thu được ở điều kiện tiêu chuẩn và hao hụt 10%?
b) Nếu dùng kali clorat có thêm một lượng nhỏ MnO2 thì lượng kali clorat cần dùng là bao nhiêu? Viết phương trình phản ứng và chỉ rõ điều kiện phản ứng.
Bài 8:
\(V_{O_2}=20.100=2000\left(ml\right)=2\left(l\right)\\ a,PTHH:2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\\ n_{O_2}=\dfrac{2}{22,4}=\dfrac{5}{56}\left(mol\right)\\ n_{O_2\left(p.ứ\right)}=\dfrac{5}{56}.90\%=\dfrac{9}{112}\left(mol\right)\\ n_{KMnO_4\left(dùng\right)}=\dfrac{9}{112}.2=\dfrac{9}{56}\left(mol\right)\\ \Rightarrow m_{KMnO_4}=\dfrac{9}{56}.158=\dfrac{711}{28}\left(g\right)\\ b,2KClO_3\rightarrow\left(t^o,xt\right)2KCl+3O_2\\ n_{KClO_3}=\dfrac{2}{56}.\dfrac{2}{3}=\dfrac{1}{42}\left(mol\right)\\ m_{KClO_3}=122,5.\dfrac{1}{42}=\dfrac{35}{12}\left(g\right)\)
Đúng 2
Bình luận (0)
Bài 1:
\(C+O_2\rightarrow\left(t^o\right)CO_2\)
Tên sản phẩm: Cacbon dioxit/ Khí cacbonic
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
Tên sản phẩm: Điphotpho pentaoxit
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
Tên sản phẩm: Nước
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
Tên sản phẩm: Nhôm oxit
Đúng 1
Bình luận (0)
Viết phương trình hóa học biểu diễn sự cháy của sắt, phôtpho, lưu huỳnh, nhôm trong khí oxi
3Fe + 2O2 -> (t°) Fe3O4
4P + 5O2 -> (t°) 2P2O5
S + O2 -> (t°) SO2
4Al + 3O2 -> (t°) 2Al2O3
Đúng 2
Bình luận (1)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
\(S+O_2\rightarrow\left(t^o\right)SO_2\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
Đúng 0
Bình luận (0)
Câu 1: (2đ) Viết phương trình hóa học của oxi với những chất sau:
a. Đồng
d. Sắt e. Nhôm g. Cacbon
i. Nhôm
c. Khí axetilen C,H, , khí etanC2Ho, propanol (C3H3O).
h. Kẽm
b. Khí hiđro
k. Cacbon 1. Khí etan (C,H6) m. Kẽm
a, 2Cu + O2 --to--> 2CuO
d, 3Fe + 2O2 --to--> Fe3O4
e, 4Al + 3O2 --to--> 2Al2O3
g, C + O2 --to--> CO2
i, 4Al + 3O2 --to--> 2Al2O3
c, 2C2H2 + 5O2 --to--> 4CO2 + 2H2O
2C2H6 + 7O2 --to--> 4CO2 + 6H2O
2C3H3O + 8O2 --to--> 6CO2 + 6H2O
h, 2Zn + O2 --to--> 2ZnO
Đúng 2
Bình luận (0)
help me plss
Viết phương trình hóa học biểu diễn sự cháy trong oxi của các chất sau: a) Sắt, cacbon, magie, lưu huỳnh; b) Axetilen C2H2, hiđrosunfua H2S, sắt(II) sunfua FeS.
a)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(C+O_2\underrightarrow{t^o}CO_2\)
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
\(S+O_2\underrightarrow{t^o}SO_2\)
b)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
\(H_2S+\dfrac{3}{2}O_2\underrightarrow{t^o}SO_2+H_2O\)
\(2FeS+\dfrac{7}{2}O_2\underrightarrow{t^o}Fe_2O_3+2SO_2\)
Đúng 6
Bình luận (0)
\(a,3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\\ C+O_2\rightarrow\left(t^o\right)CO_2\\ 2Mg+O_2\rightarrow\left(t^o\right)2MgO\\ S+O_2\rightarrow\left(t^o\right)SO_2\\ b,2C_2H_2+5O_2\rightarrow\left(t^o\right)4CO_2+2H_2O\\ 2H_2S+3O_2\rightarrow\left(t^o\right)2SO_2+2H_2O\\ 4FeS+7O_2\rightarrow\left(t^o\right)2Fe_2O_3+4SO_2\)
Đúng 5
Bình luận (0)
a.
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
\(C+O_2\rightarrow\left(t^o\right)CO_2\)
\(Mg+\dfrac{1}{2}O_2\rightarrow\left(t^o\right)MgO\)
\(S+O_2\rightarrow\left(t^o\right)SO_2\)
b.
\(C_2H_2+\dfrac{5}{2}O_2\rightarrow\left(t^o\right)2CO_2+H_2O\)
\(2H_2S+3O_2\rightarrow\left(t^o\right)2SO_2+2H_2O\)
\(4FeS+7O_2\rightarrow\left(t^o\right)2Fe_2O_3+4SO_2\)
Đúng 1
Bình luận (0)
Câu 9: (3,0 điểm)
a. Viết phương trình hóa học biểu diễn sự cháy của các chất sau trong khí oxi: đồng,
nhôm, lưu huỳnh, butan (C4H10)
b. Một oxit được tạo bởi 2 nguyên tố sắt và oxi trong đó tỉ lệ khối lượng giữa sắt và
oxi là 7:3. Tìm công thức phân tử của oxit đó.
a)\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(S+O_2\underrightarrow{t^o}SO_2\)
\(C_4H_{10}+\dfrac{13}{2}O_2\underrightarrow{t^o}4CO_2+5H_2O\)
b)Gọi CTHH là \(Fe_xO_y\)
\(x:y=\dfrac{m_{Fe}}{56}:\dfrac{m_O}{16}=\dfrac{7}{56}:\dfrac{3}{16}=0,125:0,1875=2:3\)
\(\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\Rightarrow Fe_2O_3\)
Đúng 2
Bình luận (0)
Bài 1: Hãy lập pthh biểu diễn các phản ứng hóa học sau:
a) Sắt + clo -> Sắt (III) clorua.
b) Nhôm + oxi -> Nhôm oxit.
c) Hiđro + oxi -> Nước.
d) Đồng oxit + cacbon oxit -> Đồng + Cacbon dioxit.
e) Natri + Nước -> Natri hiđroxit + khí hiđro.
Cho biết tỉ lệ số nguyên tử, phân tử của các chất trong mỗi phản ứng.
\(a,2Fe+3Cl_2\buildrel{{t^o}}\over\to 2FeCl_3\\ 2:3:2\\ b,4Al+3O_2\buildrel{{t^o}}\over\to 2Al_2O_3\\ 4:3:2\\ c,2H_2+O_2\buildrel{{t^o}}\over\to 2H_2O\\ 2:1:2\\ d,CuO+CO\buildrel{{t^o}}\over\to Cu+CO_2\\ 1:1:1:1\\ e,2Na+2H_2O\to 2NaOH+H_2\\ 2:2:2:1 \)
Đúng 2
Bình luận (0)

























