
Những câu hỏi liên quan
Khử 48 gam đồng(II) oxit bằng khí hiđro. Hãy:
a) Tính số gam đồng kim loại thu được.
b) Tính thể tích khí hiđro (đktc) cần dùng.
nCuO = 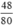 = 0,6 mol.
= 0,6 mol.
Phương trình hóa học của phản ứng khử CuO:
CuO + H2 → Cu + H2O.
nCu = 0,6mol.
mCu = 0,6 .64 = 38,4g.
Theo phương trình phản ứng trên:
nH2 = 0,6 mol
VH2 = 0,6 .22,4 = 13,44 lít.
Đúng 0
Bình luận (0)
Khử hoàn toàn 8 gam đồng (II) oxit bằng khí hiđro ở nhiệt độ cao. Hãy tính thể tích khí hiđro (đktc) cần dùng.(Cho Cu = 64; O = 16)
\(n_{CuO}=\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{8}{80}=0,1\left(mol\right)\)
PTHH: \(CuO+H_2\rightarrow Cu+H_2O\)
.............1.............1...............................
.............0,1...........0,1...........................
\(V_{H_2\left(ĐKTC\right)}=n_{H_2}\cdot22,4=0,1\cdot22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
nCuO=8/80=0,1(mol)
CuO+H2->Cu+H2O
1 : 1 : 1 : 1 (mol)
0,1: 0,1 : 0,1: 0,1 (mol)
VH2=0,1x22,4=2,24(lít)
Đúng 1
Bình luận (0)
Bài 6: Khử 48 gam đồng (II) oxit bằng khí hidro. Hãy:
a) Tính số gam đồng kim loại thu được
Tính thể tích khí hiđro (đktc) cần dùng
nCuO = 48 : 80 = 0,6 (Mol)
pthh : CuO + H2 -t--> Cu + H2O
0,6---->06------>0,6
=> mCu= 0,6 . 64 = 38,4 (G)
=> VH2 = 0,6 .22,4 = 13,44 (L)
Đúng 1
Bình luận (0)
a, \(n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
0,6 0,6 0,6
\(\rightarrow\left\{{}\begin{matrix}m_{Cu}=0,6.64=38,4\left(g\right)\\V_{H_2}=0,6.22,4=13,44\left(l\right)\end{matrix}\right.\)
Đúng 0
Bình luận (0)
PTHH : \(CuO+H_2\left(t^o\right)->Cu+H_2O\) (1)
a) \(n_{CuO}=\dfrac{m}{M}=\dfrac{48}{64+16}=0,6\left(mol\right)\)
Từ (1) -> \(n_{Cu}=n_{CuO}=n_{H_2}=0,6\left(mol\right)\)
-> \(m_{Cu}=n.M=0,6.64=38,4\left(g\right)\)
\(V_{H_2}=n.22,4=0,6.22,4=13,44\left(l\right)\)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Khử 48 gam đồng(II) oxit bằng khí hiđro. Hãy:
a) Tính khối lượng đồng thu được.
b) Tính thể tích khí hiđro (đktc) cần dùng.
khử 9,6 gam đồng (ll) oxit bằng khí hiđro. hãy:
a)tính số gam đồng kim loại thu được;
b)tính thể tích khí hiđro (đktc)cần dùng.
\(n_{CuO}=\dfrac{9,6}{80}=0,12mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,12 0,12 0,12
a)\(m_{Cu}=0,12\cdot64=7,68g\)
b)\(V=0,12\cdot22,4=2,688l\)
Đúng 2
Bình luận (0)
\(n_{CuO}=\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{9,6}{80}=0,12mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,12 0,12 0,12 ( mol )
\(m_{Cu}=n_{Cu}.M_{Cu}=0,12.56=6,72g\)
\(V_{H_2}=n_{H_2}.22,4=0,12.22,4=2,688l\)
Đúng 1
Bình luận (0)
1/ khử 48 gam đồng (II) Oxit bằng khí hiđro.hãy
tính số gam đồng kim loại thu được
tính thể tích khí hiđro (đktc) cần dùng
2/ tính số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít khí oxi (các thể tích khí đo ở đktc)
1/ \(CuO+H_2-^{t^o}\rightarrow Cu+H_2O\)
\(n_{Cu}=n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\)
=> \(m_{Cu}=0,6.64=38,4\left(g\right)\)
\(n_{H_2}=n_{CuO}=0,6\left(mol\right)\)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
Đúng 3
Bình luận (0)
2. \(2H_2+O_2-^{t^o}\rightarrow2H_2O\)
\(n_{H_2}=0,375;n_{O_2}=0,125\)
Lập tỉ lệ \(\dfrac{0,375}{2}>\dfrac{0,125}{1}\)
=> Sau phản ứng H2 dư, tính theo số mol O2
\(n_{H_2O}=2n_{O_2}=0,25\left(mol\right)\)
=> \(m_{H_2O}=0,25.18=4,5\left(g\right)\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 12,8 gam đồng trong lọ chứa khí oxi
a) Viết PTHH xảy ra.
b) Tính khối lượng đồng(II)oxit thu được.
c) Tính thể tích khí Hidro (đktc) cần dùng để khử hoàn toàn lượng đồng (II)oxit trên ở nhiệt độ cao.
khử hoàn toàn 16 gam đồng(II) oxit( CuO) bằng khí hidro. tính
a) số gam đồng thu được sau phản ứng
b) thể tích khí hidro ở( đktc)
a, Ta có: \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(n_{Cu}=n_{CuO}=0,2\left(mol\right)\Rightarrow m_{Cu}=0,2.64=12,8\left(g\right)\)
b, \(n_{H_2}=n_{CuO}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
Đúng 2
Bình luận (0)
\(n_{CuO}=\dfrac{m}{M}=\dfrac{16}{64+16}=0,2\left(mol\right)\)
\(PTHH:Cu+H_2O\rightarrow CuO+H_2\)
1 1 1 1
0,2 0,2 0,2 0,2
a) \(m_{Cu}=n.M=0,2.64=12,8\left(g\right)\)
b) \(V_{H_2}=n.24,79=4,958\left(l\right).\)
Đúng 1
Bình luận (0)
n\(_{CuO}\)=\(\dfrac{16}{80}\)=0,2(m)
PTHH:CuO+H\(_2\)->Cu+H\(_2\)O
tỉ lệ :1 1 1 1
số mol:0,2 0,2 0,2 0,2
a)m\(_{Cu}\)=0,2.64=12,8(g)
b)V\(_{H_2}\)=0,2.22,4=44,8(l)
Đúng 1
Bình luận (0)
khử hoàn toàn 48g đồng (II) oxit bằng khí hidro ở nhiệt độ cao thu dc kim loại đồng và nc
tính gam đồng kim loại thu dc
tính thể tích khí h2 (đctc) cần dùng
PTHH: CuO+H2→H2O+Cu nCuO=4880=0,6 mol.
Bảo toàn nguyên tố: Số mol đồng kim loại thu được là: nCu=0,6 mol. \
Số gam đồng thu được là: mCu=0,6×64=38,4g
Số mol khí Hidro cần dùng là: nH2=nCuO=0,6 mol
Thể tích khí Hidro cần dùng là: V=0,6×22,4=13,44l
Đúng 2
Bình luận (0)
\(n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\\
pthh:CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,6 0,6 0,6
=> \(m_{Cu}=0,6.64=38,4\left(g\right)\\
V_{H_2}=0,6.22,4=13,44\left(l\right)\)
Đúng 0
Bình luận (0)





























