Cân bằng ptrinh oxi hóa khử

Những câu hỏi liên quan
Câu 2
A,Có 3 lo mất nhãn đựng 3 chất lỏng gồm: H2O, dụng dịch HCL, dung dịch NaOH, bằng phương trình hóa học hãy nhận bt từng chất trong mỗi lo
B, hòa tan 3,6 gam bột kim loại A hóa trị 2 bằng một lượng dư như axit HCL thu được 3,36 l khí H2 điều kiện tiêu chuẩn xác định kim loại A
Câu 3 cho 13 gam Zn phản ứng hoàn toàn với dung dịch HCl dư A, viết phương trình hóa học xảy ra B, tính Tính thể tích H2 ở điều...
Đọc tiếp
Câu 2
A,Có 3 lo mất nhãn đựng 3 chất lỏng gồm: H2O, dụng dịch HCL, dung dịch NaOH, bằng phương trình hóa học hãy nhận bt từng chất trong mỗi lo
B, hòa tan 3,6 gam bột kim loại A hóa trị 2 bằng một lượng dư như axit HCL thu được 3,36 l khí H2 điều kiện tiêu chuẩn xác định kim loại A
Câu 3 cho 13 gam Zn phản ứng hoàn toàn với dung dịch HCl dư A, viết phương trình hóa học xảy ra B, tính Tính thể tích H2 ở điều kiện tiêu chuẩn C, Nếu dung hoàn toàn lượng H2 bay ra ở trên nên đem khử 12 gam bột CuO ở nhiệt độ cao sao còn dư bao nhiêu gam
B, hòa tan 3,6 gam bột kim loại A hóa trị 2 bằng một lượng dư như axit HCL thu được 3,36 l khí H2 điều kiện tiêu chuẩn xác định kim loại A
--
PTHH: A+ 2 HCl -> ACl2 + H2
nH2= 0,15(mol)
=> nA= 0,15(mol)
=> M(A)=3,6/0,15=24(g/mol)
=> A(II) cần tìm là Magie (Mg(II)=24)
Câu 3 cho 13 gam Zn phản ứng hoàn toàn với dung dịch HCl dư A, viết phương trình hóa học xảy ra B, tính Tính thể tích H2 ở điều kiện tiêu chuẩn C, Nếu dung hoàn toàn lượng H2 bay ra ở trên nên đem khử 12 gam bột CuO ở nhiệt độ cao sao còn dư bao nhiêu gam
----
nZn= 0,2(mol); nCuO= 0,15(mol)
a) PTHH: Zn + 2 HCl -> ZnCl2 + H2
b)nH2 = nZn=0,2(mol) =>V(H2,đktc)=0,2.22,4=4,48(l)
c) PTHH: H2 + CuO -to-> Cu + H2O
Ta có: 0,2/1 < 0,15/1
=> CuO hết, Zn dư, tính theo nCuO.
=> nZn(p.ứ)=nCuO=0,15(mol)
=>nZn(dư)=nZn(ban đầu)-nZn(p.ứ)=0,2-0,15=0,05(mol)
=> mZn(dư)=0,05.65= 3,25(g)
Đúng 0
Bình luận (0)
Khử hoàn toàn 0,8gam CuO bằng khí H2. Em hãy tính a. Số gam đồng thu được b. Thể tích khí H2 cần dùng ở (đktc)
\(n_{CuO}=\dfrac{0,8}{80}=0,01mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,01 0,01 0,01 ( mol )
\(m_{Cu}=0,01.64=0,64g\)
\(V_{H_2}=0,01.22,4=0,224l\)
Đúng 1
Bình luận (0)
Phú Ông có 10 túi đựng tiền vàng giống in hệt nhau. Trong đó có một túi đựng tiền giả. Biết rằng đồng tiền giả nặng 9g, trong khi đồng tiền thật nặng 10g. Phú Ông ra lệnh cho Cuội phải tìm ra túi đựng tiền giả đó bằng một chiếc cân đồng hồ và chỉ một lần cân.
Khử hoàn toàn 10,23g hỗn hợp Cu và PbO bằng khí CO ở nhiệt độ cao. Khí sinh ra sau phản ứng được dẫn vào bình đựng dd Ca(OH)2 thu được 11g kết tủa. a. Viết pthh b. Tính thành phần 5% theo khối lượng của mỗi oxit trong hỗn hợp
Sửa đề: 10,23g CuO và PbO
Bảo toàn Cacbon: \(n_{CO_2}=n_{CaCO_3}=\dfrac{11}{100}=0,11\left(mol\right)\)
PTHH: \(CuO+CO\xrightarrow[]{t^o}Cu+CO_2\)
a_________________a (mol)
\(PbO+CO\xrightarrow[]{t^o}Pb+CO_2\)
b_________________b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}80a+223b=10,23\\a+b=0,11\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,01\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CuO}=\dfrac{0,1\cdot80}{10,23}\cdot100\%\approx78,2\%\\\%m_{PbO}=21,8\%\end{matrix}\right.\)
Đúng 2
Bình luận (1)
a) \(PbO+CO-^{t^o}\rightarrow Pb+CO_2\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
b) \(n_{kt}=n_{CO_2}=0,11\left(mol\right)\)
\(n_{PbO}=n_{CO_2}=0,11\left(mol\right)\)
=> \(\%m_{PbO}=\dfrac{0,11.223}{10,23}.100=239,78\)%
Đề sai :D
Đúng 0
Bình luận (1)
Khử 8g đồng 2 oxit bằng khí hidro nung nóng a.Viết phương trình hóa học b.Tính khối lượng kim loại thu được c.Tính thể tích hidro (đktc) cần dùng
câu 1) trình bày các tính chất của hóa học của oxi và mổi tính chất háo học viết 2 phương trính hóa học minh họa ?
câu 2) khí oxi là chất ở đơn chất của nguyên tố gì?
khí oxi có nhiều ở đâu ?
ở dạng hợp chất nguyên tố oxi có nhiều ở đâu ?
câu 3) định nghỉa sự oxi hóa là gì ? viết 3 phương trình hóa học minh họa cho sự oxi hóa?
câu 4) định nghĩa phản ứng hóa hợp là gì ? viết 3 phương trình hóa học minh họa cho phản ứn...
Đọc tiếp
câu 1) trình bày các tính chất của hóa học của oxi và mổi tính chất háo học viết 2 phương trính hóa học minh họa ?
câu 2) khí oxi là chất ở đơn chất của nguyên tố gì?
khí oxi có nhiều ở đâu ?
ở dạng hợp chất nguyên tố oxi có nhiều ở đâu ?
câu 3) định nghỉa sự oxi hóa là gì ? viết 3 phương trình hóa học minh họa cho sự oxi hóa?
câu 4) định nghĩa phản ứng hóa hợp là gì ? viết 3 phương trình hóa học minh họa cho phản ứng hóa hợp?
Oxi hóa 6 gam ancol đơn chức A bằng oxi không khí (có xúc tác và đun nóng) thu được 8,4 gam hỗn hợp anđehit, ancol dư và nước. Phần trăm A bị oxi hóa là: A. 60%. B. 75%. C. 80%. D. 53,33%.
Đọc tiếp
Oxi hóa 6 gam ancol đơn chức A bằng oxi không khí (có xúc tác và đun nóng) thu được 8,4 gam hỗn hợp anđehit, ancol dư và nước. Phần trăm A bị oxi hóa là:
A. 60%.
B. 75%.
C. 80%.
D. 53,33%.
Đáp án C
Hướng dẫn
Đặt công thức của ancol là RCH2OH.
Số mol O2 đã tham gia phản ứng là:
![]()
Phương trình phản ứng :
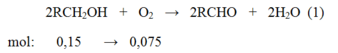
Theo (1) ta thấy số mol RCH2OH đã phản ứng là 0,15 mol, theo giả thiết sau phản ứng ancol còn dư nên ta suy ra số mol ancol ban đầu phải lớn hơn 0,15 mol. Do đó:
![]()
Hiệu suất phản ứng oxi hóa ancol là:
![]()
Đúng 0
Bình luận (0)
Oxi hóa 9,2 gam ancol đơn chức X bằng oxi không khí (có xúc tác và đun nóng) thu được 12,4 gam hỗn hợp anđehit, ancol dư và nước. Phần trăm X bị oxi hóa có giá trị gần nhất với A. 60%. B. 80%. C. 90%. D. 70%.
Đọc tiếp
Oxi hóa 9,2 gam ancol đơn chức X bằng oxi không khí (có xúc tác và đun nóng) thu được 12,4 gam hỗn hợp anđehit, ancol dư và nước. Phần trăm X bị oxi hóa có giá trị gần nhất với
A. 60%.
B. 80%.
C. 90%.
D. 70%.
Khí oxi trữ trong các bệnh viện được hóa lỏng và đựng trong bình thép. Người ta đã hóa lỏng oxi bằng cách nào ?
Oxi lỏng (1877)
Năm 1877, L.-P. Cailletet (1832-1913), chủ một xưởng thợ rèn của Côte-d’Or (Bourgogne) đã phát minh ra một chiếc bơm cho phép tạo ra và duy trì được áp suất cỡ vài trăm atmotphe.
Ông đã hóa lỏng được oxi bằng cách gây ra sự giãn nở đột ngột của chất khí chứa trong một mao quản mà ở đó ông đã giảm áp suất từ 300 tới 1 atmotphe, điều đó khiến cho nhiệt độ hạ xuống tới -118,9oC.
Vài ngày sau khi thí nghiệm thành công đó, R.-P. Pictet (1848-1929), giáo sư vạt lý ở Đại học Giơnevơ đã công bố kết quả của các nghiên cứu tương tự.
Không khí lỏng (1895)
Năm 1895, nhà phát minh và nhà công nghiệp K. von Linde (1842-1934) đã hóa lỏng được không khí bằng cách nén và cho giãn nở với sự làm lạnh trung gian. Như vậy là ông đã điều chế được oxi lỏng gần như tinh khiết. năm 1902, nhà bác học G. Claude (1870-1960) đã phát minh ra một phương pháp khác để hóa lỏng không khí, bằng cách cho giãn nở chất khí với việc sản công bên ngoài. Xuất phát tự không khí khóa lỏng, ông đã tách được oxi, nitơ và agon lỏng bằng cách phân đoạn. Như vậy, ông đã tìm ra phương pháp công nghiệp đầu tiên để hóa lỏng chất khí.
Đúng 0
Bình luận (0)