Agon tách từ không khí là một hỗn hợp của 3 đồng vị sau :
![]()
Tính thể tích của 20 gam agon ở điều kiện tiêu chuẩn.
Agon tách ra từ không khí là hỗn hợp ba đồng vị: 99,6% 40Ar; 0,063% 38Ar; 0,337% 36Ar. Tính thể tích của 10g Ar ở điều kiện tiêu chuẩn
agon tách ra từ không khí là hỗn hợp của 3 đồng vị : 99,6% 40Ar ; 0,063% 38Ar ; 0,337% 36Ar Tính thể tích của 10g Ar ở điều kiện tiêu chuẩn
HD:
Nguyên tử khối trung bình của Ar = 0,996.40 + 0,063.38 + 0,337.36 = 54,366 đvC.
Số mol của Ar = 10/54,366 = 0,184 mol. Thể tích V = 0,184.22,4 = 4.1216 lít.
Đốt cháy hoàn toàn m gam hỗn hợp X gồm 3 amin đồng đẳng bằng một lượng không khí vừa đủ, thu được 5,376 lít CO 2 , 7,56 gam H 2 O và 41,664 lít N 2 (các thể tích khí đo được ở điều kiện tiêu chuẩn, O 2 chiếm 20% thể tích không khí, N 2 chiếm 80% thể tích không khí). Giá trị của m là:
A. 10,80 gam
B. 4,05 gam
C. 5,40 gam
D. 8,10gam
Ta có: \(\left\{{}\begin{matrix}n_{O_2}=\dfrac{5,6.20\%}{22,4}=0,05\left(mol\right)\\n_{N_2}=\dfrac{5,6.80\%}{22,4}=0,2\left(mol\right)\end{matrix}\right.\)
- Hỗn hợp 3 khí gồm: CO2, O2 dư và N2.
\(C+O_2\underrightarrow{t^o}CO_2\)
Gọi: nCO2 = x (mol) ⇒ nO2 (pư) = x (mol) ⇒ nO2 (dư) = 0,05 - x (mol)
Mà: hh khí có tỉ khối so với H2 là 14,88.
\(\Rightarrow\dfrac{44x+32.\left(0,05-x\right)+28n_{N_2}}{x+0,05-x+n_{N_2}}=14,88.2\)
⇒ x = 0,02 (mol)
BTNT C, có: nC = nCO2 = 0,02 (mol)
⇒ m = mC = 0,02.12 = 0,24 (g)
Trong tự nhiên Agon có 3 loại đồng vị bền với tỉ lệ % nguyên tử là:
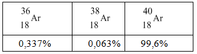
Cho rằng nguyên tử khối của các đồng vị trùng với số khối của chúng. Thể tích của 20gam Agon (đo ở đktc) bằng
A. 1,121 dm3
B. 11,204 dm3
C. 11,214 dm3
D. 1,120 dm3
ĐÁP ÁN B
nAr = x mol gồm có : 0,996x mol 40Ar ; 0,00337x mol 36Ar và 0,00063x mol 38Ar
=> mAr = 20g = 0,996x.40 + 0,00337x.36 + 0,00063x.38 = 20g
=> x = 0,5002 mol
=> VAr = 11,204 lit = 11,204 dm3
Đối cháy 24,8 gam phốt pho bằng 67,2 lít không khí ở điều kiện tiêu chuẩn (không khí có chứa 20% khí oxy và 80% khí nitơ về thể tích). a) Tính khối lượng sản phẩm tạo thành? b) Tính thành phần phần trăm về khối lượng các chất có trong hỗn hợp sau phản ứng? Biết rằng khí nitơ không cháy.
$\rm a)n_{kk} = \dfrac{67,2}{22,4} = 3 (mol)$
$\rm \Rightarrow n_{O_2} = 20\%.3 = 0,6 (mol)$
$\rm n_P = \dfrac{24,8}{31} = 0,8 (mol)$
PTHH: \(\rm 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5 \)
Ban đầu: 0,8 0,6
Pư: 0,48<--0,6
Sau pư: 0,32 0 0,24
$\rm \Rightarrow m_{\text{sản phẩm tạo thành}} = m_{P_2O_5(sinh.ra)} = 0,24.142 = 34,08 (g)$
$\m b) m_{hh} = m_{P(dư)} + m_{P_2O_5} = 0,32.31 + 34,08 = 44 (g)$
$\rm \Rightarrow \%m_P = \dfrac{0,32.31}{44} .100\% = 22,545\%$
$\rm \Rightarrow \%m_{P_2O_5} = 100\% - 22,545\% = 77,455\%$
\(n_P=\dfrac{24,8}{31}=0,8\left(mol\right)\)
Thể tích Oxi trong 67,2 lít không khí :
67,2 x 20% = 13,44(l)
\(n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH :
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
Trc p/ư: 0,8 0,6 (mol)
p/ư 0,48 0,6 0,24
Sau p/ư: 0,32 0 0,24
=> Sau p/ư P dư
Khối lượng sản phẩm tạo thành :
\(m_{P_2O_5}=0,24.142=34,08\left(g\right)\)
Khối lượng P trong hỗn hợp :
\(m_{P\left(P_2O_5\right)}=0,48.31=14,88\left(g\right)\)
Thành phần % của P :
\(14,88:34,08=43,66\%\)
Đốt cháy hoàn toàn 9,2 gam rượu etylic.
a) Tính thể tích khí CO2 tạo ra ở điều kiện tiêu chuẩn.
b) Tính thể tích không khí (ở điều kiện tiêu chuẩn) cần dùng cho phản ứng trên. Biết oxi chiếm 20% thể tích không khí
dẫn hỗn hợp 20 lít khí ch4 và c2h4 qua dung dịch br2 sau khi phản ứng kết thúc thấy có 8 gam br2 tham gia phản ứng .tính thành phần % các khí trong hỗn hợp ban đầu( các thể tích đo ở điều kiện tiêu chuẩn)
\(n_{Br_2}=\dfrac{8}{160}=0.05\left(mol\right)\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(0.05......0.05\)
\(V_{C_2H_4}=0.05\cdot22.4=1.12\left(l\right)\)
\(V_{CH_4}=20-1.12=18.88\left(l\right)\left(mol\right)\)
\(\%V_{C_2H_4}=\dfrac{1.12}{20}\cdot100\%=5.6\%\)
\(\%V_{CH_4}=100-5.6=94.4\%\)