Cho 250ml dung dịch Ba(OH)2 0,4M vào 250ml dung dịch H2SO4 0,3M. Nồng độ mol của chất trong dung dịch sau phản ứng
A. 0,05M B.0,15M C.0,2M D.0,025M
1.Cho dung dịch chứa 0,9 mol NaOH vào dung dịch có chứa a mol H3PO4. Sau phản ứng chỉ thu được muối Na3PO4 và H2O. Giá trị của a là:
A. 0,3 mol B. 0,4 mol C. 0,6 mol D. 0,9 mol 2. Cho 200ml dung dịch Ba(OH)2 0,4M vào 250ml dung dịch H2SO4 0,3M. Khối lượng kết tủa thu được là:
A. 17,645 g B. 16,475 g C. 17,475 g D. 18,645 g 3.Cho 200ml dung dịch KOH 1M tác dụng với 200ml dung dịch H2SO4 1M, sau phản ứng cho thêm một mảnh Mg dư vào sản phẩm thấy thoát ra một thể tích khí H2 (đktc) là:
A. 2,479 lít B. 4,958 lít C. 3,719 lít D. 7,437 lít
\(1.3NaOH+H_3PO_4\rightarrow Na_3PO_4+3H_2O\\ a=n_{H_3PO_4}=\dfrac{1}{3}n_{NaOH}=\dfrac{1}{3}\cdot0,9=0,3mol\\ \Rightarrow A\\ 2.n_{Ba\left(OH\right)_2}=0,2.0,4=0,08mol\\ n_{H_2SO_4}=0,25.0,3=0,075mol\\ Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4+2H_2O\\ \Rightarrow\dfrac{0,08}{1}>\dfrac{0,075}{1}\Rightarrow Ba\left(OH\right)_2.dư\\ n_{BaSO_4}=n_{H_2SO_4}=0,075mol\\ m_{\uparrow}=m_{BaSO_4}=0,075.233=16,725g\\ \Rightarrow?:))\\ 3.n_{KOH}=0,2.1=0,2mol\\ n_{H_2SO_4}=0,2.1=0,2mol\\ 2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\\ \Rightarrow\dfrac{0,2}{2}< \dfrac{0,2}{1}\Rightarrow H_2SO_4.dư\\ n_{H_2SO_4.pư}=\dfrac{1}{2}n_{KOH}=\dfrac{1}{2}\cdot0,2=0,1mol\\ n_{H_2SO_4_4.dư}=0,2-0,1mol\\ H_2SO_4+Mg\rightarrow MgSO_4+H_2\\ n_{H_2}=n_{H_2SO_4.dư}=0,1mol\\ V_{H_2}=0,1.24,79=2,479l\\ \Rightarrow A\)
Câu 32: Trộn 250ml dung dịch A gồm Ba(OH)2 0,2M và NaOH 0,3M với 250ml dung dịch H_{2}*S*O_{4} có pH = 1 Sau khi trộn thu được dung dịch B và m (g) kết tủa. a) Tính pH của dung dịch A. b) Tính nồng độ các ion trong dung dịch thu được. c) Tính pH của dung dịch thu được d) Tính m Giúp em với ạ
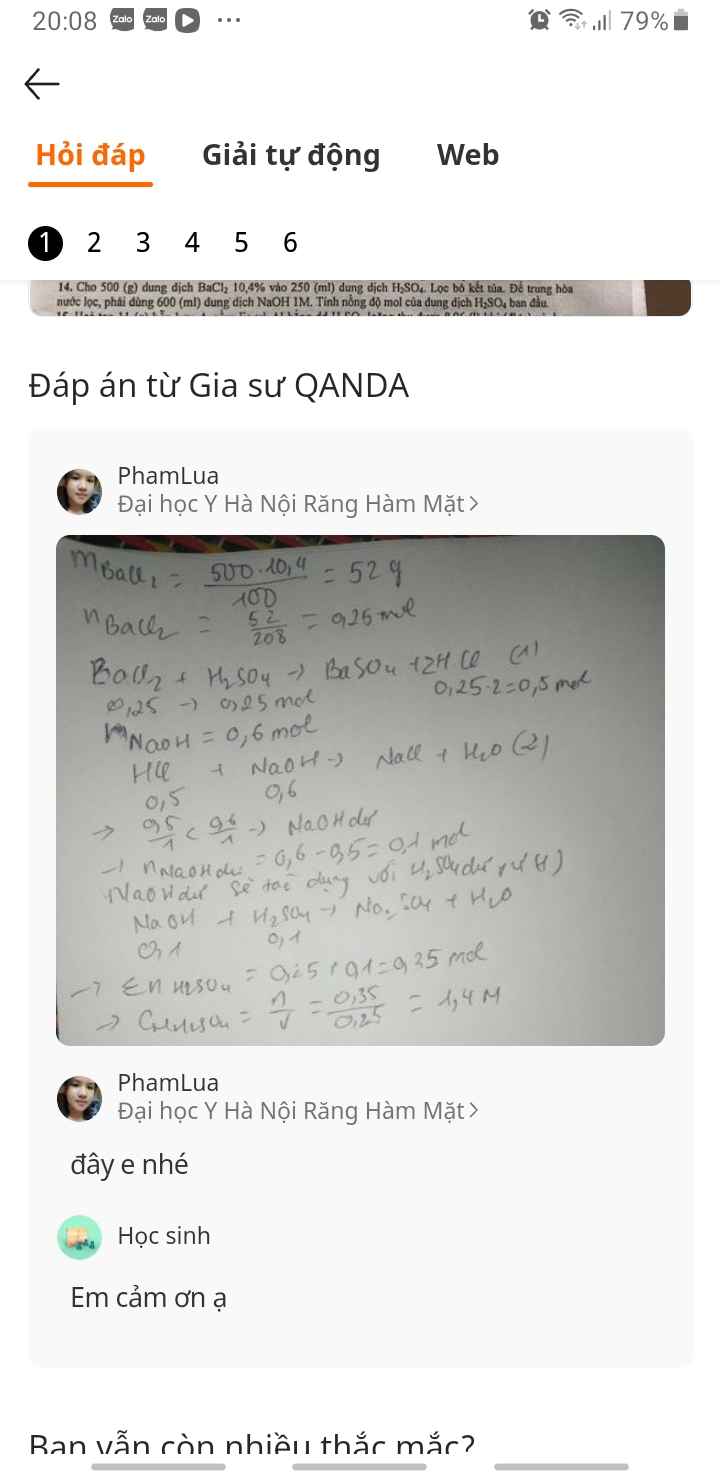
Cho 200g dung dịch Ba(OH)2 10o/o vào 200g dung dịch H2SO4. lọc bỏ kết tủa, trung hòa nước lọc cần dùng 250ml NaOH 25 o/o d = 1,28. Tính nồng độ o/o của dung dịch H2SO4 ban đầu và nồng độ o/o của dung dịch sau phản ứng?
Em ko có tiền nên mong a , cj tham khảo(đây là 500 g dung dịch nên mong a, cj sửa 1 chút ạ)
Giải giúp mình 2 câu nhé:
1) Tính nồng độ mol/lit của các ion trong dung dịch
a)Ion K+ và SO4 2- trong dung dịch K2SO4 0,05M
b)Ion Ba 2+ và OH- trong dung dịch Ba(OH)2 0,02M
c)Ion H+ và NO3 - trong 100ml dung dịch HNO3 nồng độ 10% (D=1,054g/ml)
2) Cho 150 ml dung dịch KOH 2M vào 250ml dung dịch HCl 3M. Tính nông độ mol/lit của các ion trong dung dịch sau phản ứng
2)
nKOH = 0.15*2=0.3 mol
nHCl = 0.25*3=0.75 mol
KOH + HCl --> KCl + H2O
Bđ: 0.3____0.45
Pư : 0.3____0.3____0.3
Kt: 0______0.15___0.3
DD sau phản ứng : 0.15 mol HCl dư , 0.3 mol KCl
CM H+= 0.15/0.25=0.6M
CM Cl- = 0.15/0.25=0.6 M
CM K+= 0.3/(0.15+0.25)=0.75M
CM Cl-= 0.3/(0.15+0.25)= 0.75M
Cho 200ml dung dịch Ba(O H ) 2 0,4M vào 250ml dung dịch H 2 S O 4 0,3M. Khối lượng kết tủa thu được là:
A. 17,645 gam
B. 16,475 gam
C. 17,475 gam
D. 18,645 gam
Chọn C

K ế t t ủ a l à B a S O 4 → n ↓ = n H 2 S O 4 = 0 , 075 m o l m ↓ = 0 , 075 . 233 = 17 , 475 g a m .
Dung dịch A gồm HCl 0,2M ; HNO3 0,3M; H2SO4 0,1M; HClO4 0,3M, dung dịch B gồm KOH 0,3M; NaOH 0,4M, Ba(OH)2 0,15M. Cần trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch có pH=13?
A. 11:9
B. 9:11
C. 101:99
D. 99:101
Đáp án A
Gọi thể tích dung dịch A là V1 lít. Có nH+ = ( 0,2+0,3+0,1.2+0,3).V1 = V1 mol
Gọi thể tích dung dịch B là V2 lít. Có nOH- = ( 0,3+ 0,4+ 0,15.2).V2 = V2 mol
H+ + OH- → H2O
V1 V2
Dung dịch thu được có pH = 13 nên OH- dư
nOHdư = V2- V1 mol
[OH-]dư = (V2-V1)/(V2+ V1) = 10-1 suy ra V1: V2 = 11:9
Dung dịch A gồm HCl 0,2M; HNO3 0,3M; H2SO4 0,1M; HClO4 0,3M, dung dịch B gồm KOH 0,3M; NaOH 0,4M; Ba(OH)2 0,15M. Cần trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch có pH = 13?
A. 11 : 9.
B. 9 : 11.
C. 101 : 99.
D. 99 : 101.
Chọn B.
Nồng độ H+ ban đầu là: (0,2 + 0,3 + 0,1.2 + 0,3) = 1M.
Nồng độ OH- ban đầu là: (0,3 + 0,4 + 0,15.2) = 1M.
Dung dịch sau phản ứng có pH = 13, suy ra OH- dư, pOH = 1.
Nồng độ OH- dư là: 10-1 = 0,1M.
Áp dụng sơ đồ đường chéo cho trường hợp OH- dư, ta được:
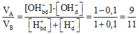
Dung dịch A gồm HCl 0,2M; HNO3 0,3M; H2SO4 0,1M; HClO4 0,3M, dung dịch B gồm KOH 0,3M; NaOH 0,4M; Ba(OH)2 0,15M. Cần trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch có pH = 13?
A. 11 : 9
B. 9 : 11
C. 101 : 99
D. 99 : 101
Đáp án B.
Nồng độ H+ ban đầu là: (0,2 + 0,3 + 0,1.2 + 0,3) = 1M.
Nồng độ OH- ban đầu là: (0,3 + 0,4 + 0,15.2) = 1M.
Dung dịch sau phản ứng có pH = 13, suy ra OH- dư, pOH = 1.
Nồng độ OH- dư là: 10-1 = 0,1M.
Áp dụng sơ đồ đường chéo cho trường hợp OH- dư, ta được:
VA/VB = (1-0,1)/(1+0,1) = 9/11
Cho 250ml dung dịch H2SO4 1M với 250ml dung dịch NaOH, tính nồng độ mol của dung dịch NaOH và nồng độ mol của chất tan có trong dung dịch sau.
PTHH: H2SO4+2NaOH→Na2SO4+2H2O
nH2SO4=0,25×1=0,25 mol.
Theo pt: nNaOH=2nH2SO4=0,5 mol.
Theo pt: nNa2SO4=nH2SO4=0,25 mol.
Vdd spư=250+250=500 ml=0,5 lít.
⇒CM NaOH=0,5/0,25=2 M.
CM Na2SO4=0,25/0,5=0,5 M.