Khối lượng P2O5 có trong 5 tấn quặng photphat chứa 35% Ca3(PO4)2 là
A. 0,5 tấn B. 0,8 tấn C. 0,7 tấn D. 0,85 tấn
1 loại quặng photphat chứa 60% là tạp chất, còn lại là ca3(po4)2. Nếu dùng 20 tấn quặng này thì lượng p2o5 điều chế được là bao nhiêu
\(m_{Ca_3\left(PO_4\right)_2}=20\cdot40\%=8\left(tấn\right)=8000\left(kg\right)\)
\(n_{Ca_3\left(PO_4\right)_2}=\dfrac{8000}{310}=\dfrac{800}{31}\left(kmol\right)\)
Bảo toàn nguyên tố P :
\(n_{P_2O_5}=n_{Ca_3\left(PO_4\right)_2}=\dfrac{800}{31}\left(kmol\right)\)
\(m_{P_2O_5}=\dfrac{800}{31}\cdot142=3664.5\left(kg\right)\)
$m_{Ca_3(PO_4)_2} = 20.(100\%-60\%) = 8(tấn) = 8000(kg)$
Bảo toàn P
$n_{P_2O_5} = n_{Ca_3(PO_4)_2} = \dfrac{8000}{310}(kmol)$
$m_{P_2O_5} = \dfrac{8000}{310}.142 = 3664,5(kg)$
Từ quặng photphorit, có thể điều chế axit photphoric theo sơ đồ sau:
![]()
Biết hiệu suất chung của cả quá trình là 90%. Để điều chế được 1 tấn dung dịch H3PO4 49%, cần bao nhiêu tấn quặng photphorit chứa 73% Ca3(PO4)2 về khối lượng?
A. 1,32tấn
B. 1,23tấn
C. 1,81tấn
D. 1,18tấn
Một loại quặng photphat có chứa 35% Ca3(PO4)2. Hãy tính hàm lượng phần trăm P2O5 có trong quặng trên.
Trong 1000g quặng có: 1000. 35% = 350g Ca3(PO4)2
Bảo toàn nguyên tố P ⇒ trong 1 mol Ca3(PO4)2 có 1mol P2O5 nghĩa là trong 310g Ca3(PO4)2 tương ứng có 142g P2O5.
⇒350g Ca3(PO4)2 có lượng P2O5 là:
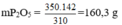
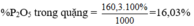
Cho 10 tấn quặng hemantit chứa 60 % Fe2O3.Khối lượng Fe có thể điều chế được là :
(Biết : Fe=56, O=16)
A. 60 tấn
B. 42 tấn
C. 6 tấn
D. 4,2 tấn
\(m_{Fe}=70\%.60\%.10=4,2\left(tấn\right)\)
Khử một lượng quặng hemantit chứa 82% (Fe,O,) thu được 2,52 tấn sắt, khối lượng quặng cần lấy là bao nhiêu? Biết H = 80% A. 5,487 tán B. 5,488 tấn C. 5,489 tấn D. 5,486 tấn
Quặng hemantit chứa thành phần chính là : Fe2O3
Bảo toàn nguyên tố Fe: \(n_{Fe_2O_3}.2=n_{Fe}\\ \Rightarrow n_{Fe_2O_3}=0,0225\left(mol\right)\\ VìH=80\%\Rightarrow m_{Fe_2O_3}=\dfrac{0,0225}{80\%}.160=4,5\left(tấn\right)\\ m_{quặng}=\dfrac{4,5}{82\%}=5,488\left(tấn\right)\)
Từ quặng photphorit, có thể điều chế axit photphoric theo sơ đồ sau:
Quặng photphorit → lò điện SiO 2 , C P → O 2 , t 0 P 2 O 5 → H 2 O H 3 P O 4
Biết hiệu suất chung của quá trình là 90%. Để điều chế được 1 tấn dung dịch H3PO4 49%, cần khối lượng quặng photphorit chứa 73% Ca3(PO4)2 là
A. 1,18 tấn
B. 1,81 tấn
C. 1,23 tấn
D. 1,32 tấn
Có hai loại quặng sắt: quặng loại I và quặng loại II. Khối lượng tổng cộng của hai loại quặng là 10 tấn. Khối lượng sắt nguyên chất trong quặng loại I là 0,8 tấn, trong quặng loại II là 0,6 tấn. Biết tỉ lệ sắt nguyên chất trong quặng loại I nhiều hơn tỉ lệ sắt nguyên chất trong quặng loại II là 10%. Tính khối lượng của mỗi loại quặng
Gọi khối lượng của quặng loại I là x(tấn)
(Điều kiện: 0<x<=10)
Khối lượng của quặng loại II là 10-x(tấn)
Tỉ lệ sắt nguyên chất trong quặng loại I là \(\dfrac{0.8}{x}\left(tấn\right)\)
Tỉ lệ sắt nguyên chất trong quặng loại II là \(\dfrac{0.6}{10-x}\left(tấn\right)\)
Tỉ lệ sắt nguyên chất trong quặng loại I nhiều hơn tỉ lệ sắt nguyên chất trong quặng loại II là 10%=0,1 nên ta có;
\(\dfrac{0.8}{x}-\dfrac{0.6}{10-x}=0.1\)
=>\(\dfrac{8}{x}-\dfrac{6}{10-x}=1\)
=>\(\dfrac{8}{x}+\dfrac{6}{x-10}=1\)
=>\(\dfrac{8x-80+6x}{x\left(x-10\right)}=1\)
=>\(x\left(x-10\right)=14x-80\)
=>\(x^2-24x+80=0\)
=>(x-20)(x-4)=0
=>\(\left[{}\begin{matrix}x-20=0\\x-4=0\end{matrix}\right.\)
=>\(\left[{}\begin{matrix}x=20\left(loại\right)\\x=4\left(nhận\right)\end{matrix}\right.\)
Vậy: Khối lượng quặng loại I là 4 tấn
Khối lượng quặng loại II là 10-4=6 tấn
Có hai quặng sắt: quặng loại I và quặng loại II, khối lượng tổng cộng là 10 tấn. Khối lượng sắt nguyên chất trong quặng I là 0,8 tấn, trong quặng loại II là 0,6 tấn. Biết tỉ số sắt nguyên chất trong quặng loại I nhiều hơn tỉ lệ sắt nguyên chất trong quặng loại II là 10%. Tính khối lượng của mỗi quặng.
Giải thích rõ ràng. Cấm gian lận :)
Gọi khối lượng quặng loại 1 là x ( \(x\ne0\) )
Khối lượng quặng 2 là : \(10-x\left(tấn\right)\)
Tỉ lệ sắt nguyên chất trong quặng loại I là: \(\dfrac{0,8}{x}\)
Tỉ lệ sắt nguyên chất trong quặng loại II là: \(\dfrac{0,6}{10-x}\)
Do tỉ lệ sắt nguyên chất trong quặng loại I nhiều hơn tỉ lệ sắt nguyên chất trong quặng loại II là 10%
Nên ta có phương trình:
\(\dfrac{0,8}{x}-\dfrac{0,6}{10-x}=\dfrac{10}{100}\)
\(\Leftrightarrow0,8\left(10-x\right)-0,6x=0,1x\left(10-x\right)\)
\(\Leftrightarrow8\left(10-x\right)-6x=x\left(10-x\right)\)
\(\Leftrightarrow80-8x-6x=10x-x^2\)
\(\Leftrightarrow x^2-24x+80=0\)
\(\Leftrightarrow x\left(x-20\right)-4\left(x-20\right)=0\)
\(\Leftrightarrow\left(x-20\right).\left(x-4\right)=0\)
\(\Leftrightarrow\left[{}\begin{matrix}x-20=0\\x-4=0\end{matrix}\right.\Leftrightarrow\left[{}\begin{matrix}x=20\left(l\right)\\x=4\left(n\right)\end{matrix}\right.\)
Vậy: Khối lượng quặng loại I là 4 tấn, khối lượng quặng loại I là: 10 – 4 = 6 tấn.
1.Tính khối lượng sắt có trong :
a. 100 tấn quặng hemetit chứa 60% Fe2O3
b. 100 tấn quặng manhetit chứa 69,6 % Fe3O4
2. Cần trộn hai loại quặng trên theo tỉ lệ nào để từ 1 tấn quặng đã trộn người ta điều chế được 0,5 tấn gang( chứa 96% sắt và 4% cacbon )?