Trộn 160 gam dung dịch CuSO4,10% và 240 gam dung dịch NaOH 5% thu được kết tủa A và dung dịch B
a) Lọc kết tủa ,rửa sạch thu được bao nhiêu gam chất rắn
b) Tính nồng độ % của các chất trong dung dịch B
Cho 200 gam dung dịch NaOH tác dụng với 250g dung dịch CuSO4 16% (biết phản ứng xảy ra hoàn toàn ) thu được kết tủa lọc rửa sạch kết tủa, đem nung thu được a gam chất rắn màu đen a) Viết các PTHH xảy ra b) Tính giá trị a c) Tính khối lượng của dung dịch thu được sau phản ứng troi oi cíu tui, tui cần gấp lắmm
a, \(2NaOH+CuSO_4\rightarrow Na_2SO_4+Cu\left(OH\right)_2\)
\(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
b, \(m_{CuSO_4}=250.16\%=40\left(g\right)\Rightarrow n_{CuSO_4}=\dfrac{40}{160}=0,25\left(mol\right)\)
Theo PT: \(n_{CuO}=n_{Cu\left(OH\right)_2}=n_{CuSO_4}=0,25\left(mol\right)\)
\(\Rightarrow a=m_{CuO}=0,25.80=20\left(g\right)\)
c, Ta có: m dd sau pư = m dd NaOH + m dd CuSO4 - mCu(OH)2 = 200 + 250 - 0,25.98 = 425,5 (g)
\(a)2NaOH+CuSO_4\rightarrow Cu\left(OH\right)_2+Na_2SO_4\\ Cu\left(OH\right)_2\xrightarrow[]{t^0}CuO+H_2O\\ b)n_{CuSO_4}=\dfrac{250.16}{100.160}=0,25mol\\ n_{CuSO_4}=n_{Cu\left(OH\right)_2}=n_{CuO}=0,25mol\\ a=m_{CuO}=0,25.80=20g\\ c)m_{dd}=200+250-0,25.98=425,5g\)
Cho 100 ml dung dịch H2 SO4 2m vào 100 ml dung dịch BaCl2 1M thu được dung dịch A và kết tủa B a) Tính khối lượng kết tủa B thu được b) Tính nồng độ mol các chất có trong dung dịch A c) để trung hòa dung dịch A thì cần bao nhiêu gam dung dịch NaOH 15%
a)
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
$n_{BaCl_2} = 0,1 < n_{H_2SO_4} = 0,2$ nên $H_2SO_4$ dư
$n_{BaSO_4} = n_{BaCl_2} = 0,1(mol)$
$m_{BaSO_4} = 0,1.233 = 23,3(gam)$
b)
A gồm :
$HCl : 0,1.2 = 0,2(mol)$
$H_2SO_4\ dư : 0,2 - 0,1 = 0,1(mol)$
$V_{dd} = 0,1 + 0,1= 0,2(lít)$
$C_{M_{HCl}} = \dfrac{0,2}{0,2} = 1M$
$C_{M_{H_2SO_4}} = \dfrac{0,1}{0,2} = 0,5M$
c)
$2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
$n_{NaOH} = 2n_{H_2SO_4\ dư} = 0,2(mol)$
$m_{dd\ NaOH} = \dfrac{0,2.40}{15\%} = 53,33(gam)$
Trộn 160 gam dung dịch natri hidroxit 20% với dung dịch đồng (II) nitrat 4% thu được dung dịch X và kết tủa Y. Lọc kết tủa Y , nung kết tủa Y đến khi khối lượng không đổi thu được chất rắn A. a)Tính khối lượng chất rắn A thu được . b)Tính khối lượng dung dịch đồng (II) nitrat 4% phản ứng. c)Tính nồng độ % của dung dịch X.
Cho 160 gam dung dịch CuSO4 nồng độ 10%phản ứng với 150 gam dung dịch NaOH 8%, thu được m gam kết tủa Cu(OH)2và dung dịch X. Tính m và nồng độ phần trăm mỗi chất tan trong dung dịch X
\(n_{CuSO_4}=\dfrac{160.10\%}{160}=0,1\left(mol\right)\)
\(n_{NaOH}=\dfrac{150.8\%}{40}=0,3\left(mol\right)\)
PTHH: CuSO4 + 2NaOH --> Cu(OH)2 + Na2SO4
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,3}{2}\) => CuSO4 hết, NaOH dư
PTHH: CuSO4 + 2NaOH --> Cu(OH)2 + Na2SO4
0,1------>0,2------->0,1------->0,1
=> m = 0,1.98 = 9,8 (g)
\(\left\{{}\begin{matrix}m_{NaOH_{dư}}=\left(0,3-0,2\right).40=4\left(g\right)\\m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\end{matrix}\right.\)
mdd sau pư = 160 + 150 - 9,8 = 300,2 (g)
\(\left\{{}\begin{matrix}C\%_{NaOH_{dư}}=\dfrac{4}{300,2}.100\%=1,33\%\\C\%_{Na_2SO_4}=\dfrac{14,2}{300,2}.100\%=4,73\%\end{matrix}\right.\)
\(m_{CuSO_4}=\dfrac{160.10}{100}=16\left(g\right)\\ n_{NaOH}=\dfrac{8.150}{100}=12\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}n_{CuSO_4}=\dfrac{16}{160}=0,1\left(mol\right)\\n_{NaOH}=\dfrac{12}{40}=0,3\left(mol\right)\end{matrix}\right.\)
PTHH: 2NaOH + CuSO4 ---> Cu(OH)2 + Na2SO4
LTL: \(0,1< \dfrac{0,3}{2}\rightarrow\) NaOH dư
Theo pt: \(\left\{{}\begin{matrix}n_{NaOH\left(pư\right)}=\dfrac{1}{2}n_{CuSO_4}=2.0,1=0,2\left(mol\right)\\n_{Na_2SO_4}=n_{Cu\left(OH\right)_2}=n_{CuSO_4}=0,1\left(mol\right)\end{matrix}\right.\)
\(\rightarrow m=0,1.98=9,8\left(g\right)\\ m_{dd}=160+150-9,8=300,2\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}C\%_{NaOH\left(dư\right)}=\dfrac{\left(0,3-0,2\right).40}{300,2}=1,33\%\\C\%_{Na_2SO_4}=\dfrac{0,1.142}{300,2}=4,73\%\end{matrix}\right.\)
Trộn dung dịch có chứa 0,1 mol CuSO4 và một dung dịch chứa 0,25 mol NaOH, lọc kết tủa, rửa sạch rồi đem nung đến khối lượng không đổi thu được m gam chất rắn. Giá trị m là *
\(CuSO_4+2NaOH->Cu\left(OH\right)_2+Na_2SO_4\)
bđ 0,1 0,25
pư 0,1............0,2...............0,1
spu 0...............0,05.............0,1
\(Cu\left(OH\right)_2-^{t^o}>CuO+H_2O\)
0,1.........................0,1
m CuO = 0,1.(64+16)=8g
Trộn 1 dung dịch có hòa tan 0,2 mol CuCl2 với dung dịch có hòa tan 20g NaOH, lọc tách được kết tủa và dung dịch trước nước lọc. Nung kết tủa đến khối lượng không đổi thu được a gam chất rắn a) Tính giá trị bằng số của a b) Tính khối lượng các chất có trong dung dịch nước lọc
a) \(n_{NaOH}=\dfrac{20}{40}=0,5\left(mol\right)\)
\(CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2+2NaCl\)
Lập tỉ lệ : \(\dfrac{0,2}{1}< \dfrac{0,5}{2}\)=> Sau phản ứng NaOH dư
\(n_{Cu\left(OH\right)_2}=n_{CuCl_2}=0,2\left(mol\right)\)
Dung dịch nước lọc gồm NaCl (0,4_mol); NaOH dư ( 0,1 mol)
\(Cu\left(OH\right)_2-^{t^o}\rightarrow CuO+H_2O\)
\(n_{CuO}=n_{Cu\left(OH\right)_2}=0,2\left(mol\right)\)
\(a=m_{CuO}=0,2.80=16\left(g\right)\)
b) \(m_{NaCl}=0,4.58,5=23,4\left(g\right);m_{NaOH}=0,1.40=4\left(g\right)\)
Cho 3,06 gam hỗn hợp bột X gồm Fe và Mg vào 100ml dung dịch Cu(NO3)2. Phản ứng xong, thu được 4,14 gam chất rắn và dung dịch Y. Thêm dung dịch NaOH dư vào dung dịch Y, lọc kết tủa, rủa sạch, sấy khô và nung trong không khí ở nhiệt độ cao đến khối lượng không đổi thì thu được 2,7 gam chất rắn. Nồng độ mol của dung dịch Cu(NO3)2 là
A. 0,25M
B. 0,45M
C. 0,35M
D. 0,3M.
Đáp án B
Có khối lượng chất rắn sau khi nung < mX
=> Chứng tỏ X phản ứng còn dư, Cu(NO3)2 phản ứng hết.
· Trường hợp 1: Mg phản ứng còn dư.
Áp dụng tăng giảm khối lượng có:
nMg phản ứng 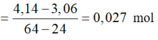
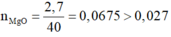 => Vô lý
=> Vô lý
· Trường hợp 2: Fe đã tham gia phản ứng.
Đặt số mol Mg và Fe phản ứng lần lượt là a, b.
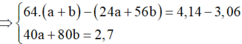
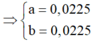
![]()
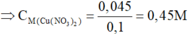
Cho 3,06 gam hỗn hợp bột X gồm Fe và Mg vào 100ml dung dịch Cu(NO3)2. Phản ứng xong, thu được 4,14 gam chất rắn và dung dịch Y. Thêm dung dịch NaOH dư vào dung dịch Y, lọc kết tủa, rủa sạch, sấy khô và nung trong không khí ở nhiệt độ cao đến khối lượng không đổi thì thu được 2,7 gam chất rắn. Nồng độ mol của dung dịch Cu(NO3)2 là
A. 0,25M
B. 0,45M
C. 0,35M
D. 0,3M
Chọn đáp án B.
Có khối lượng chất rắn sau khi nung < mX
=> Chứng tỏ X phản ứng còn dư, Cu(NO3)2 phản ứng hết.
· Trường hợp 1: Mg phản ứng còn dư.
Áp dụng tăng giảm khối lượng có:
nMg phản ứng = 4 , 14 - 3 , 06 64 - 24 = 0 , 027 mol
n M g O = 2 , 7 40 = 0 , 0675 > 0 , 027 => Vô lý
· Trường hợp 2: Fe đã tham gia phản ứng.
Đặt số mol Mg và Fe phản ứng lần lượt là a, b.
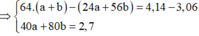
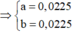
⇒ n C u N O 3 2 = 0 , 045 m o l
⇒ C M ( C u N O 3 2 ) = 0 , 045 0 , 1 = 0 , 45 M
Cho 4,58 gam hỗn hợp A gồm Zn, Fe và Cu vào cốc đựng 85 ml dung dịch C u S O 4 1M. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch B và kết tủa C. Nung C trong không khí đến khối lượng không đổi được 6 gam chất rắn D. Thêm dung dịch NaOH dư vào dung dịch B, lọc kết tủa thu được, rửa sạch rồi nung ở nhiệt độ cao đến khối lượng không đổi thu được 5,2 gam chất rắn E. Các phản ứng xảy ra hoàn toàn. % khối lượng mỗi kim loại trong hỗn hợp A (theo thứ tự Zn, Fe, Cu) là
A. 28,38%; 36,68% và 34,94%
B. 14,19%; 24,45% và 61,36%
C. 28,38%; 24,45% và 47,17%
D. 42,58%; 36,68% và 20,74%