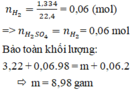Chia 7,72 gam hỗn hợp X gồm Fe và hai oxit kim loại MO, R2O3 thành hai phần bằng nhau. Dùng một lượng vừa đủ dung dịch H2SO4 loãng hòa tan hoàn toàn phần 1, thu được khí B và dung dịch D chứa 9,7 gam muối. Dẫn toàn bộ lượng khí B sinh ra qua ống đựng 1,6 gam CuO nung nóng, đến khi thu được 1,408 gam chất rắn thì đã có 80% lượng khí B tham gia phản ứng. Mặt khác, dẫn dòng khí CO dư qua phần 2 nugn nóng, sau khi phản ứng xảy ra hoàn toàn thu được 3,46 gam chất rắn. Biết rằng nguyên tử khối của M gấp 2,37 lần nguyên tử khối của R. Cho các phản ứng được thực hiện trong điều kiện không có không khí. Xác định 2 kim loại M, R và tính % khối lượng các chất trong hỗn hợp X.

Những câu hỏi liên quan
Hòa tan hoàn toàn 8,3 gam hỗn hợp hai kim loại Al và Fe bằng một lượng vừa đủ 200 ml dung dịch H2SO4 xM (loãng) thì thu được dung dịch (A) và 5,6 lít khí (đktc).a) Tính giá trị của x.b) Tính thành phần % về khối lượng các chất có trong (A)c) Tính nồng độ mol các chất có trong (A)d) Tính khối lượng dung dịch KOH 15% khi cho vào dung dịch (A) để d.1. Lượng kết tủa bé nhất d.2. Lượng kết tủa lớn nhất
Đọc tiếp
Hòa tan hoàn toàn 8,3 gam hỗn hợp hai kim loại Al và Fe bằng một lượng vừa đủ 200 ml dung dịch H2SO4 xM (loãng) thì thu được dung dịch (A) và 5,6 lít khí (đktc).
a) Tính giá trị của x.
b) Tính thành phần % về khối lượng các chất có trong (A)
c) Tính nồng độ mol các chất có trong (A)
d) Tính khối lượng dung dịch KOH 15% khi cho vào dung dịch (A) để
d.1. Lượng kết tủa bé nhất d.2. Lượng kết tủa lớn nhất
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Gọi x, y lần lượt là số mol Al, Fe
Theo đề bài ta có hệ pt
\(\left\{{}\begin{matrix}27x+56y=8,3\\\dfrac{3}{2}x+y=\dfrac{5,6}{22,4}=0,25\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
a)\(x=\dfrac{\dfrac{0,1.3}{2}+0,1}{0,2}=0,25M\)
b)\(\%m_{Al_2(SO_4)_3}=\dfrac{\dfrac{0,1}{2}.342}{\dfrac{0,1}{2}.342+0,1.152}.100=52,94\%\)
=> %mFeSO4=100-52,94=47,06%
c)\(CM_{Al_2(SO_4)_3}=\dfrac{0,05}{0,2}=0,25M\)
\(CM_{FeSO_4}=\dfrac{0,1}{0,2}=0,5M\)
d) 1> Thu được kết tủa bé nhất
-TH1 : Lượng KOH chỉ phản ứng với FeSO4 tạo kết tủa, không đủ để tạo kết tủa với Al2(SO4)3
\(2KOH+FeSO_4\rightarrow Fe\left(OH\right)_2+K_2SO_4\)
=> \(m_{ddKOH}=\dfrac{0,1.2.56}{15\%}=74,67\left(g\right)\)
TH2: Lượng KOH phản ứng với FeSO4 tạo kết tủa và tạo kết tủa với Al2(SO4)3 sau đó tan kết tủa của Al2(SO4)3
\(2KOH+FeSO_4\rightarrow K_2SO_4+Fe\left(OH\right)_2\)
\(6KOH+Al_2(SO_4)_3\rightarrow2Al\left(OH\right)_3+3K_2SO_4\)
\(Al\left(OH\right)_3+KOH\rightarrow KAlO_2+2H_2O\)
=>\(m_{ddKOH}=\dfrac{\left(0.1.2+0,05.6+0,1\right).56}{15\%}=224\left(g\right)\)
2> Thu được kết tủa lớn nhất :
Lượng KOH phản ứng với FeSO4 tạo kết tủa và tạo kết tủa với Al2(SO4)3 và không tan kết tủa của Al2(SO4)3
\(2KOH+FeSO_4\rightarrow K_2SO_4+Fe\left(OH\right)_2\)
\(6KOH+Al_2(SO_4)_3\rightarrow2Al\left(OH\right)_3+3K_2SO_4\)
=>\(m_{ddKOH}=\dfrac{\left(0.1.2+0,05.6\right).56}{15\%}=186,67\left(g\right)\)
Đúng 1
Bình luận (0)
Đặt \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{matrix}\right.\)
\(PTHH:2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(\left(mol\right)\) \(a\) \(1,5a\) \(0,5a\) \(1,5a\)
\(PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(\left(mol\right)\) \(b\) \(b\) \(b\) \(b\)
Ta có hpt: \(\left\{{}\begin{matrix}27a+56b=8,3\\1,5a+b=\dfrac{5,6}{22,4}\end{matrix}\right.\Leftrightarrow a=b=0,1\left(mol\right)\)
\(a.x=\dfrac{1,5a+b}{0,2}=\dfrac{0,15+0,1}{0,2}=1,25\left(M\right)\\ b.\%m_{Al}=\dfrac{27.0,1}{8,3}.100=32,53\left(\%\right)\\ \%m_{Fe}=100-32,53=67,47\left(\%\right)\\ c.C_{M_{Al_2\left(SO_4\right)_3}}=\dfrac{0,5a}{0,2}=0,25\left(M\right)\\ C_{M_{FeSO_4}}=\dfrac{b}{0,2}=0,5\left(M\right)\\ d.\)
\(PTHH:Al_2\left(SO_4\right)_3+6KOH\rightarrow3K_2SO_4+2Al\left(OH\right)_3\)
\(\left(mol\right)\) \(0,05\) \(0,3\) \(0,1\)
\(PTHH:FeSO_4+2KOH\rightarrow Fe\left(OH\right)_2+K_2SO_4\)
\(\left(mol\right)\) \(0,1\) \(0,2\)
\(PTHH:Al\left(OH\right)_3+KOH\rightarrow KAlO_2+2H_2O\)
\(\left(mol\right)\) \(0,1\) \(0,1\)
\(d.1.\) Lượng kết tủa bé nhất khi kết tủa \(Al\left(OH\right)_3\) sinh ra tan hết trong dd KOH
Khi đó: \(n_{KOH}=0,6\left(mol\right)\rightarrow m_{ddKOH}=\dfrac{0,6.100.56}{15}=224\left(g\right)\)
\(d.2.\) Lượng kết tủa lớn nhất khi KOH tác dụng vừa đủ với dd A
Khi đó: \(n_{KOH}=0,5\left(mol\right)\rightarrow m_{ddKOH}=\dfrac{0,5.56.100}{15}=186,67\left(g\right)\)
Đúng 0
Bình luận (0)
Bài 20. Hòa tan hoàn toàn 27,8 gam hỗn hợp X gồm Al và Fe vào 500 ml dung dịch H2SO4 loãng, vừa đủ thì thu được 17,353 lít khí thoát ra (ở đkc)
a. Tính thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp X
b. Tính nồng độ mol/lít của dung dịch H,SO, đã sử dụng.
a, Ta có: 27nAl + 56nFe = 27,8 (1)
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{17,353}{24,79}=0,7\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Fe}=0,4\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{27,8}.100\%\approx19,42\%\\\%m_{Fe}\approx80,58\%\end{matrix}\right.\)
b, \(n_{H_2SO_4}=n_{H_2}=0,7\left(mol\right)\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,7}{0,5}=1,4\left(M\right)\)
Đúng 2
Bình luận (0)
Hỗn hợp X gồm FeO, Fe2O3 và Fe3O4. Hòa tan hết m gam X vào dung dịch HCl vừa đủ thu được dung dịch muối Y. Chia Y làm hai phần bằng nhau: - Để oxi hóa hết các chất có trong dung dịch ở phần một cần vừa đủ 300ml dung dịch KMnO4 0,1M/H2SO4 (loãng). - Phần hai hòa tan tối đa 0,96 gam kim loại Cu. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là: A. 3,84 B. 7,68 C. 26,4 D. 13,2
Đọc tiếp
Hỗn hợp X gồm FeO, Fe2O3 và Fe3O4. Hòa tan hết m gam X vào dung dịch HCl vừa đủ thu được dung dịch muối Y. Chia Y làm hai phần bằng nhau:
- Để oxi hóa hết các chất có trong dung dịch ở phần một cần vừa đủ 300ml dung dịch KMnO4 0,1M/H2SO4 (loãng).
- Phần hai hòa tan tối đa 0,96 gam kim loại Cu.
Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là:
A. 3,84
B. 7,68
C. 26,4
D. 13,2
Đốt cháy hoàn toàn m gam hỗn hợp gồm 3 kim loại A,B,C thu được 16,6g hỗn hợp oxit. Hòa tan hoàn toàn 16,6 g hỗn hợp oxit trên bằng dung dịch H2SO4 loãng (vừa đủ). Cô cạn dung dịch sau PƯ được 24,6g muối khan. Tính m và khối lượng H2SO4 đã dùng
Gọi số mol H2O sinh ra là a (mol)
=> \(n_{H_2SO_4}=a\left(mol\right)\)
Theo ĐLBTKL: moxit + mH2SO4 = mmuối + mH2O
=> 16,6 + 98a = 24,6 + 18a
=> a = 0,1 (mol)
=> nO = 0,1 (mol)
=> mkim loại = 16,6 - 0,1.16 = 15 (g)
\(m_{H_2SO_4}=0,1.98=9,8\left(g\right)\)
Đúng 2
Bình luận (0)
Chia hỗn hợp X gồm K, AI và Fe thành hai phần bằng nhau. Cho phần một vào dung dịch KOH (dư) thu được 0,784 lít khí H2 (đktc). Cho phần hai vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hòa tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H2 (đktc). Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là A. 0,39; 0,54; 1,40. B. 0,78; 0,54;1,12 C. 0,39; 0,54; 0,56 D. 0,78; 1,08;0,56
Đọc tiếp
Chia hỗn hợp X gồm K, AI và Fe thành hai phần bằng nhau.
Cho phần một vào dung dịch KOH (dư) thu được 0,784 lít khí H2 (đktc).
Cho phần hai vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hòa tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H2 (đktc).
Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là
A. 0,39; 0,54; 1,40.
B. 0,78; 0,54;1,12
C. 0,39; 0,54; 0,56
D. 0,78; 1,08;0,56
Đốt cháy hoàn toàn 15 gam hỗn hợp gồm 3 kim loại A, B, C thu được 16,6 gam hỗn hợp oxit. Hòa tan hoàn toàn 16,6 gam hỗn hợp oxi trên bằng dung dịch H2SO4 loãng(vừa đủ).a.Thể tích dung dịch H2SO4 0,2M đã dùng.b.Tổng khối lượng muối sunfat tạo thành.
Đọc tiếp
Đốt cháy hoàn toàn 15 gam hỗn hợp gồm 3 kim loại A, B, C thu được 16,6 gam hỗn hợp oxit. Hòa tan hoàn toàn 16,6 gam hỗn hợp oxi trên bằng dung dịch H2SO4 loãng(vừa đủ).
a.Thể tích dung dịch H2SO4 0,2M đã dùng.
b.Tổng khối lượng muối sunfat tạo thành.
BTKL
mO2=16.6−15=1.6(g)
nO2=\(\dfrac{1,6}{32}\)=0.05(mol)
O2+4e→2O2−
0.05....0.2
2H++2e→H2
0.2......0.2
VH2SO4=\(\dfrac{0,2}{0,2}\)=1l
nH2O=nH2SO4=0.1(mol)
BTKL
mM=16.6+0.1⋅98−0.1⋅18=24.6(g)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 3,22 gam hỗn hợp X gồm Fe, Mg, Zn bằng lượng vừa đủ dung dịch H2SO4 loãng thu được 1,344 lít khí và dung dịch chứa m gam muối. Giá trị của m là
A. 9,25.
B. 8,98.
C. 7,25.
D. 10,27.
Đáp án B
Gọi M là kim loại chung cho các kim loại trong X với hóa trị n
Khí thu được là

Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 3,22 gam hỗn hợp X gồm Fe, Mg và Zn bằng 1 lượng vừa đủ dung dịch H 2 SO 4 loãng, thu được 1,344 lít khí hiđro (đktc) và dung dịch chứa m gam muối. Giá trị của m là
A. 9,52
B. 10,27
C. 8,98
D. 7,25
Hòa tan hoàn toàn 3,22 gam hỗn hợp X gồm Fe, Mg và Zn bằng 1 lượng vừa đủ dung dịch H2SO4 loãng, thu được 1,344 lít khí hidro (đktc) và dung dịch chứa m gam muối. Giá trị của m là:
A. 9,52
B. 10,27
C. 8,98
D. 7,25
Đáp án C
![]()
Bảo toàn khối lượng: 3,22 + 0,06.98 = m + 0,06.2
m = 8,98 gam
Đúng 0
Bình luận (0)