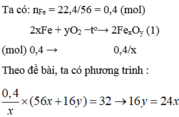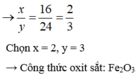Oxi hoá 22,4 gam sắt, thu được 32 gam oxit sắt. Xác định hoá trị của sắt trong oxit này.

Những câu hỏi liên quan
Oxi hoá 22,4 gam sắt, thu được 32 gam oxit sắt. Xác định tên và công thức của oxit sắt.
Câu 1: Oxi hoá 22,4 gam sắt, thu được 32 gam oxit sắt.
a) Xác định tên và công thức của oxit sắt.
b) Xác định hoá trị của sắt trong oxit này.
Tham khảo:
a) Ta có: nFe = 22,4/56 = 0,4 (mol)
2xFe + yO2 −to→ 2FexOy (1)
(mol) 0,4 → 0,4/x
Theo đề bài, ta có phương trình :
0,4/x(56x + 16y) = 32 → 16y = 24x → x/y= 16/24= 2/3
Chọn x=2, y=3 → Công thức oxit sắt : Fe2O3.
b) Hoá trị của sắt trong Fe2O3 là : III.
Đúng 0
Bình luận (0)
Tham khảo
a) Ta có: nFe = 22,4/56 = 0,4 (mol)
2xFe + yO2 −to→ 2FexOy (1)
(mol) 0,4 → 0,4/x
Theo đề bài, ta có phương trình :
0,4/x(56x + 16y) = 32 → 16y = 24x → x/y= 16/24= 2/3
Chọn x=2, y=3 → Công thức oxit sắt : Fe2O3.
b) Hoá trị của sắt trong Fe2O3 là : III.
Đúng 0
Bình luận (0)
Bài 5. a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4 gam chất rắn. Biết khối lượng mol phân tử của oxit sắt là 160 gam/mol. b) Chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư. Tính khối lượng kết tủa thu được.
a) Gọi CTHH của oxit sắt là $Fe_2O_n$
$Fe_2O_n + nCO \xrightarrow{t^o} 2Fe +nCO_2$
$n_{Fe} = \dfrac{22,4}{56} = 0,2(mol)$
$\Rightarrow n_{Fe_2O_n} = \dfrac{1}{2}n_{Fe} = 0,2(mol)$
$M_{oxit} = 56.2 + 16n = \dfrac{32}{0,2}=160$
Suy ra : n = 3
Vậy oxit cần tìm là $Fe_2O_3$
b) $n_{CO_2} = \dfrac{3}{2}n_{Fe} = 0,6(mol)$
$CO_2 +C a(OH)_2 \to CaCO_3 + H_2O$
$n_{CaCO_3} = n_{CO_2} = 0,6(mol)$
$m_{CaCO_3} = 0,6.100 = 60(gam)$
Đúng 1
Bình luận (0)
Chuyển hoá hoàn toàn 1,68 gam sắt thành một oxit sắt, sau đó hoà tan hết oxit sắt bằng dung dịch axit H2SO4 loãng 0,2M thu được dung dịch chứa 16,56 gam muối.
a) Xác định công thức phân tử của oxit sắt.
b) Tính thể tích dd H2SO4 đã dùng. Biết rằng lượng axit đem dùng dư 20% so với lượng cần thiết.
Bài 4: Trong phòng thí nghiệm, người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi để oxi hoá sắt ở nhiệt độ cao .
a. Tính số gam sắt và số gam khí oxi cần dùng để điều chế được 6,96g oxit sắt từ.
b. Tính số gam Kaliclorat cần dùng để có được lượng oxi dùng cho phản ứng trên.
a, \(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\)
PTHH: 3Fe + 2O2 ----to----> Fe3O4
Mol: 0,09 0,06 0,03
\(m_{Fe}=0,09.56=5,04\left(g\right)\)
\(m_{O_2}=0,06.32=1,92\left(g\right)\)
b,
PTHH: 2KClO3 ----to---> 2KCl + 3O2
Mol: 0,02 0,06
\(m_{KClO_3}=0,02.122,5=2,45\left(g\right)\)
Đúng 3
Bình luận (0)
trong phòng thí nghiệm, người ta điều chế oxit sắt tư Fe3O4 bằng cách dùng oxi hoá sắt ở nhiệt độ cao
a) Tính số gam sắt và số gam khí oxi cần dùng để điều chế được 2,32 g oxit sắt từ
b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên
a, PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Ta có: \(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01\left(mol\right)\)
Theo PT: \(n_{Fe}=3n_{Fe_3O_4}=0,03\left(mol\right)\Rightarrow m_{Fe}=0,03.56=1,68\left(g\right)\)
\(n_{O_2}=2n_{Fe_3O_4}=0,02\left(mol\right)\Rightarrow m_{O_2}=0,02.32=0,64\left(g\right)\)
b, PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Theo PT: \(n_{KMnO_4}=2n_{O_2}=0,04\left(mol\right)\Rightarrow m_{KMnO_4}=0,04.158=6,32\left(g\right)\)
Đúng 1
Bình luận (0)
Hãy xác định CTHH của 1 oxit sắt biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí CO thu được 22,4 gam Fe . Biết M của oxit sắt này là 160 gam .
CTHH của oxit sắt là FexOy
nfe =22,4/56=0,4 mol
pt : FexOy + yCO-> x Fe + y CO2
npứ : 0,4
Ta có : mFexOy =32g và mFexOy= mfe + mO
<=> mo= mFexOy - mfe
<=>mo=32-(0,4.56)=9,6g
=>no=9,6/16=0,6mol
=> x/y = nfe/no =0 ,4/0,6 =2/3
CTHH :Fe2 O3
Đúng 0
Bình luận (1)
Gọi CTHH của oxit sắt là FexOy
FexOy + yCO → xFe + yCO2
\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
theo pT: \(n_{Fe_xO_y}=\dfrac{1}{x}n_{Fe}=\dfrac{1}{x}\times0,4=\dfrac{0,4}{x}\left(mol\right)\)
Ta có: \(M_{Fe_xO_y}=32\div\dfrac{0,4}{x}\)
\(\Leftrightarrow160=80x\)
\(\Leftrightarrow x=2\)
Ta có: \(56\times2+16y=160\)
\(\Leftrightarrow112+16y=160\)
\(\Leftrightarrow16y=48\)
\(\Leftrightarrow y=3\)
Vậy CTHH của oxit sắt là Fe2O3
Đúng 0
Bình luận (0)
Gọi CTHH của oxit sắt là FexOy
FexOy + yCO → xFe + yCO2
nFe=22,456=0,4(mol)nFe=22,456=0,4(mol)
theo pT: nFexOy=1xnFe=1x×0,4=0,4x(mol)nFexOy=1xnFe=1x×0,4=0,4x(mol)
Ta có: MFexOy=32÷0,4xMFexOy=32÷0,4x
⇔160=80x⇔160=80x
⇔x=2⇔x=2
Ta có: 56×2+16y=16056×2+16y=160
⇔112+16y=160⇔112+16y=160
⇔16y=48⇔16y=48
⇔y=3⇔y=3
Vậy CTHH của oxit sắt là Fe2O3
Đúng 0
Bình luận (0)
a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4 gam chất rắn. Biết khối lượng mol phân tử của oxit sắt là 160 gam/mol.
b) Chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư. Tính khối lượng kết tủa thu được.
Đọc tiếp
a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4 gam chất rắn. Biết khối lượng mol phân tử của oxit sắt là 160 gam/mol.
b) Chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư. Tính khối lượng kết tủa thu được.
a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4 gam chất rắn. Biết khối lượng mol phân tử của oxit sắt là 160 gam/mol.
b) Chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư. Tính khối lượng kết tủa thu được.
Giải
a) Gọi CTHH của oxit sắt là: FexOy
PTHH: : FexOy + yCO ------> xFe + yCO2
Số mol Fe là

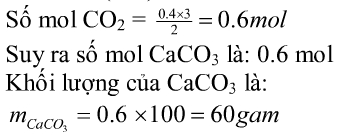
Đúng 0
Bình luận (0)
a/
mFe=22,4g
=> mO = 32-22,4=9,6g
Gọi công thức oxit sắt: FexOy
x:y=(22,4:56):(9,6:16)=2:3
=> CT: Fe2O3.
b/
nO=nC=nCO2=(9,6:16)=0,6mol
nCaCO3 =nCO2=0,6mol
=> mCaCO3 =0,6.100=60g
Đúng 1
Bình luận (0)
Công thức hoá học đơn giản nhất của một loại oxit của sắt, biết rằng trong oxit này có 7 gam sắt kết hợp với 2 gam oxi.
A. FeO B. Fe2O3 C. Fe3O4 D. Không có.