Một loại quặng có chứa 6,9% Al ,28,6% Fe ,còn lại là Si và O. Xác định CTHH của quặng trên

Những câu hỏi liên quan
Thành phần của 1 loại silicat là 32,06%Si, 48,85%O còn lại là Na và Al. Xác định CTHH của quặng này duwois dạng oxit
Một loại quặng sắt chứa 80% Fe2O3 và 10% SiO2. Hàm lượng các nguyên tử Fe và Si trong quặng này là :
A. 56% Fe và 4,7% Si
B. 54% Fe và 3,7% Si
C. 53% Fe và 2,7% Si
D. 52% Fe và 4,7% Si
Giả sử có 100 gam quặng sắt, khối lượng Fe2O3 là 80 gam và khối lượng SiO2 là 10 gam
Số mol Fe2O3 là nFe2O3 = 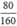 = 0,5(mol)
= 0,5(mol)
nFe = 2 x nFe2O3 = 0,5.2 = 1(mol)
→ mFe = 1.56 = 56(g)
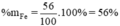
Tương tự tính cho Si , %Si = 4,7%
Đáp án là A.
Đúng 0
Bình luận (0)
Một loại quặng sắt chứa 80% Fe2O3 và 10% SiO2. Hàm lượng các nguyên tử Fe và Si trong quặng này là
A. 56% Fe và 4,7% Si.
B. 54% Fe và 3,7% Si.
C. 53% Fe và 2,7% Si.
D. 52% Fe và 4,7% Si.
Giả sử có 100 gam quặng sắt thì khối lượng Fe2O3 là 80 gam và khối lượng SiO2 là 10 gam
=> \(n_{Fe}=2n_{Fe_2O_3}=2.\dfrac{80}{160}=1\left(mol\right)\\ n_{Si}=n_{SiO_2}=\dfrac{10}{60}=\dfrac{1}{6}\left(mol\right)\)
Ta có :
\(\%Fe=\dfrac{m_{Fe}}{m_{quặng}}.100=\dfrac{1.56}{100}=56\%\\ \%Si=\dfrac{m_{Si}}{m_{quặng}}=\dfrac{\dfrac{1}{6}.28}{100}=4,7\%\)
=> Chọn A
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
A là quặng chứa 60% Fe2O3 , B là quặng chứa 69,6% Fe3O4 ( các tạp chất còn lại trong A , B đều không chứa Fe ) . Người ta trộn quặng A và B thu được quặng D . Từ 1 tấn quặng D có thể điều chế được tối đa 0,48 tấn Fe . Tính tỉ lệ khối lượng quặng A và B đem trộn.
Đặt mA = a (tấn); mB = b (tấn)
Giả sử a + b = 1 (tấn) (1)
\(m_{Fe_2O_3\left(A\right)}=a.60\%=0,6a\left(tấn\right)=6.10^5a\left(g\right)\)
=> \(n_{Fe_2O_3\left(A\right)}=\dfrac{6.10^5a}{160}=3750a\left(mol\right)\Rightarrow n_{Fe\left(A\right)}=7500a\left(mol\right)\)
\(m_{Fe_3O_4\left(B\right)}=b.69,6\%=0,696b\left(tấn\right)=696.10^3b\left(g\right)\)
=> \(n_{Fe_3O_4\left(B\right)}=\dfrac{696.10^3b}{232}=3000b\left(mol\right)\Rightarrow n_{Fe\left(B\right)}=9000b\left(mol\right)\)
\(n_{Fe\left(tổng\right)}=\dfrac{0,48.10^6}{56}=\dfrac{60000}{7}\left(mol\right)\)
=> \(7500a+9000b=\dfrac{60000}{7}\) (2)
(1)(2) => \(a=\dfrac{2}{7}\left(tấn\right);b=\dfrac{5}{7}\left(tấn\right)\)
=> \(\dfrac{a}{b}=\dfrac{2}{5}\)
Đúng 2
Bình luận (0)
A là quặng chứa 60% Fe2O3 , B là quặng chứa 69,6% Fe3O4 ( các tạp chất còn lại trong A , B đều không chứa Fe ) . Người ta trộn quặng A và B thu được quặng D . Từ 1 tấn quặng D có thể điều chế được tối đa 0,48 tấn Fe . Tính tỉ lệ khối lượng quặng A và B đem trộn.
Đặt mA = a (tấn); mB = b (tấn)
Giả sử a + b = 1 (tấn) (1)
\(m_{Fe_2O_3\left(A\right)}=a.60\%=0,6a\left(tấn\right)=6.10^5a\left(g\right)\)
=> \(n_{Fe_2O_3\left(A\right)}=\dfrac{6.10^5a}{160}=3750a\left(mol\right)\Rightarrow n_{Fe\left(A\right)}=7500a\left(mol\right)\)
\(m_{Fe_3O_4\left(B\right)}=b.69,6\%=0,696b\left(tấn\right)=696.10^3b\left(g\right)\)
=> \(n_{Fe_3O_4\left(B\right)}=\dfrac{696.10^3b}{232}=3000b\left(mol\right)\Rightarrow n_{Fe\left(B\right)}=9000b\left(mol\right)\)
\(n_{Fe\left(tổng\right)}=\dfrac{0,48.10^6}{56}=\dfrac{60000}{7}\left(mol\right)\)
=> \(7500a+9000b=\dfrac{60000}{7}\) (2)
(1)(2) => \(a=\dfrac{2}{7}\left(tấn\right);b=\dfrac{5}{7}\left(tấn\right)\)
=> \(\dfrac{a}{b}=\dfrac{2}{5}\)
Đúng 0
Bình luận (0)
Bài 1:Hợp chất A_2B_{ } có PTK94.Trong nguyên tử A có tổng số hạt là 58.Tìm CTHH của hợp chất và tính khối lượng của từng nguyên tố trong9,4 gam hợp chất.Bài 2:sHợp chất A có % khối lương của C, H lần lượt là 48,65%; 8,11% còn lại là oxi. Xác định CTHH của A( Biết trong A chứa 8 nguyên tủ oxi(Bài 3:Quặng A chứa 64% Fe_2O_3. Quặng B chứa 39.6%Fe_3O_4a.Tính khối lượng Fe trong1 tấn quặng A và Bb. Trộn quăng A và B theo tỉ lệ mm_A:m_B3:5 được 0,8 tấn quặng C. Tính khối lương Fe trong quặng CCác bn...
Đọc tiếp
Bài 1:
Hợp chất \(A_2B_{ }\) có PTK=94.Trong nguyên tử A có tổng số hạt là 58.Tìm CTHH của hợp chất và tính khối lượng của từng nguyên tố trong9,4 gam hợp chất.
Bài 2:s
Hợp chất A có % khối lương của C, H lần lượt là 48,65%; 8,11% còn lại là oxi. Xác định CTHH của A( Biết trong A chứa 8 nguyên tủ oxi(
Bài 3:
Quặng A chứa 64% \(Fe_2O_3\). Quặng B chứa \(39.6\%Fe_3O_4\)
a.Tính khối lượng Fe trong1 tấn quặng A và B
b. Trộn quăng A và B theo tỉ lệ m\(m_A:m_B=3:5\) được 0,8 tấn quặng C. Tính khối lương Fe trong quặng C
Các bn cố gắng nha
Mk cần gấp lắm
![]()
Một loại quặng sắt manhetit chứa 90% F e 3 O 4 . Tính khối lượng của Fe có trong 1 tấn quặng trên.
Đổi 1 tấn = 1000 kg
nFe2O3 = 1000 . 90% : 160 = 5,625 (kmol)
nFe = 5,625 . 3 = 16,875 (kmol)
mFe = 16,875 . 945 (kg)
Đúng 1
Bình luận (0)
Một quặng X chứa 64% Fe2O3 và quặng Y chứa 69,6% Fe3O4. Trộn a tấn quặng X với b tấn quặng Y thu được một loại quặng Z.Biết từ một tấn quặng Z có thể điều chế được 481,25kg gang chứa 4% cacbon( gang là hợp chất gồm Fe và C)
%Fe = 100% -4% = 96%
$m_{Fe} = 481,25.96% = 462(gam)$
$n_{Fe} = 462 : 56 = 8,25(kmol)$
Ta có : $a + b = 1(1)$
$m_{Fe_2O_3} = 1000a.64\% = 640a(kg)$
$\to n_{Fe_2O_3} = 640a : 160 = 4a(kmol)$
$m_{Fe_3O_4} = 1000b.69,6\% = 696b(kg)$
$\to n_{Fe_3O_4} = 696b : 232 = 3b(kmol)$
Bảo toàn nguyên tố với Fe :
$4a.2 + 3b.3 = 8,25(2)$
Từ (1)(2) suy ra a = 0,75(tấn) ; b = 0,25(tấn)
Đúng 3
Bình luận (0)
có 2 loại quặng Fe quặng loại I chứa 70% Fe quặng loại II chứa 40% Fe người ta trộn một lượng quặng loại I và 1 lượng quặng loại II thì được một hỗn hợp quặng 60% Fe , nếu lấy tăng hơn lúc đầu 5 tấn quặng loại I và lấy giảm hơn lúc đầu 5 tấn quặng loại II thì được hỗn hợp chứa 65% fe tính kim loại mỗi quặng đem trộn lúc đầu





















