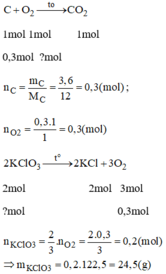khi nung nóng kali clorat KClO3 (có chất xúc tácMnO2), chất này bị phân hủy tạo thành kali clorua KCl và khí oxi. Hãy tính khối lượng kali clorat cần thiết để sinh ra một lượng khí oxi đủ để đốt cháy hết 3,6 gam cacbon?

Những câu hỏi liên quan
Khi đun nóng kali clorat K C l O 3 ( có chất xúc tác), chất này bị phân hủy tạo thành kali clorua và khí oxi.
Tính khối lượng kali clorua cần thiết để sinh ra một lượng oxi đủ đốt cháy hết 3,6g cacbon.
Nung nóng kali clorat có xúc tác là MnO2 thu được kali clorua và khí oxi. a. Nung nóng 12,25 gam kali clorat thu được 6,8 gam kali clorua. Tính hiệu suất của phản ứng này. b. Tính khối lượng kali clorat cần dùng để điều chế được 6,72 lít khí oxi (đktc). Biết hiệu suất phản ứng là 85%.c. Tính khối lượng oxi điều chế được khi phân hủy 24,5 g kali clorat. Biết hiệu suất phản ứng là 80%.
Đọc tiếp
Nung nóng kali clorat có xúc tác là MnO2 thu được kali clorua và khí oxi.
a. Nung nóng 12,25 gam kali clorat thu được 6,8 gam kali clorua. Tính hiệu suất của phản ứng này.
b. Tính khối lượng kali clorat cần dùng để điều chế được 6,72 lít khí oxi (đktc). Biết hiệu suất phản ứng là 85%.
c. Tính khối lượng oxi điều chế được khi phân hủy 24,5 g kali clorat. Biết hiệu suất phản ứng là 80%.
2KClO3-to\xt->2KCl+3O2
0,1------------------0,1
n KClO3=\(\dfrac{12,25}{122,5}\)=0,1 mol
=>m KCl=0,1.74,5=7,45g
H=\(\dfrac{6,8}{7,45}.100\)=91,275%
b)
2KClO3-to\xt->2KCl+3O2
0,2-------------------------0,3 mol
n O2=\(\dfrac{6,72}{22,4}\)=0,3 mol
H=85%
=>m KClO3=0,2.122,5.\(\dfrac{100}{85}\)=28,82g
c)
2KClO3-to\xt->2KCl+3O2
0,2------------------------0,3
n KClO3=\(\dfrac{24,5}{122,5}\)=0,2 mol
H=80%
=>m O2=0,3.32.\(\dfrac{80}{100}\)=10,4g
Đúng 3
Bình luận (0)
Nung 260 kg kali clorat(KClO3) tạo ra 120 kg kali clorua (KCl) và 110 kg khí oxi có PTHH: KClO3 to--> KCl +O2. Tính tỉ lệ phần trăm về khối lượng kali clorat đã phản ứng
\(PTHH:2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
Theo định luật bảo toàn khối lượng ta có:
\(m_{KClO_3\left(pư\right)}=m_{KCl}+m_{O_2}=120+110=230\left(kg\right)\)
Tỉ lệ phần trăm về khối lượng kali clorat phản ứng:
\(\dfrac{230}{260}.100\%\approx88,46\%\)
Đúng 3
Bình luận (0)
Để điều chế oxi trong phòng thí nghiệm người ta phân hủy kali clorat (KClO3) thu được kali clorua (KCl ) và khí oxi (O2).a. Tính thể tích khí oxi (đktc) thu được khi phân hủy 12,25 gam KClO3.b. Tính thể tích không khí chứa lượng oxi trên biết rằng c. Dùng toàn bộ lượng oxi trên cho tác dụng với 28 gam sắt. Sau phản ứng chất nào còn dư ? (Cho biết:K 39; Cl 35,5 ; O 16; Fe 56) Bài làm:
Đọc tiếp
Để điều chế oxi trong phòng thí nghiệm người ta phân hủy kali clorat (KClO3) thu được kali clorua (KCl ) và khí oxi (O2).
a. Tính thể tích khí oxi (đktc) thu được khi phân hủy 12,25 gam KClO3.
b. Tính thể tích không khí chứa lượng oxi trên biết rằng ![]() =
= ![]()
c. Dùng toàn bộ lượng oxi trên cho tác dụng với 28 gam sắt. Sau phản ứng chất nào còn dư ?
(Cho biết:K = 39; Cl = 35,5 ; O = 16; Fe = 56)
Bài làm:
a.\(n_{KClO_3}=\dfrac{m_{KClO_3}}{M_{KClO_3}}=\dfrac{12,25}{122,5}=0,1mol\)
\(2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\)
2 2 3 ( mol )
0,1 0,15
\(V_{O_2}=n_{O_2}.22,4=0,15.22,4=3,36l\)
b.\(V_{kk}=V_{O_2}.5=3,36.5=16,8l\)
c.\(n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{28}{56}=0,5mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
3 2 1 ( mol )
0,5 > 0,15 ( mol )
0,225 0,15 ( mol )
\(m_{Fe\left(du\right)}=n_{Fe\left(du\right)}.M_{Fe}=\left(0,5-0,225\right).56=15,4g\)
Đúng 1
Bình luận (0)
Khi nung KCliO3 (kali clorat),chất này phân hủy thành KCl và sinh ra 16,8 lít khí O2 a) Viết phương trình hóa học xảy ra b) Tính khối lượng Kali clorat cần dùng cho biết K=39;O=16;Cl=35,5
nO2 = 16,8 : 22,4 = 0,75 (mol)
2KMnO4 -t--> K2MnO4 + MnO2 + O2
1,5 <-------------------------------0,75(mol)
=> mKClO3 = 1,5 . 122,5 = 183,75 ( g)
Đúng 1
Bình luận (0)
Khi phân hủy hoàn toàn 24,5 g muối kali clorat KClO3 thu được 9,6g khí oxi và muối kali clorua KCl
a.Viết công thức về khối lượng của phản ứng xảy ra
b.Tính khối lượng muối kali clorua thu được
Xem chi tiết
PTHH:
\(2KClO_3\rightarrow2KCl+3O_2\)
BTKL:
\(m_{KClO_3}=m_{KCl}+m_{O_2}\)
\(\Leftrightarrow m_{KCl}=m_{KClO_3}-m_{O_2}=24,5-9,6=14,9g\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 3,6 gam magie trong khí oxi trên thì khối lượng kali clorat cần dùng.
A. Tính thể tích khí oxi (đktc) cần dùng?
B. Nếu dùng dịch KCLO3(có xúc tác MnO2) để điều chế lượng khí oxi trên thì khối lượng kali clorat cần dùng là bao nhiêu?
(O=16,CL=35,5,K=39,Mn=55)
2Mg+O2-to>2MgO
0,15---0,075 mol
2KClO3-to->2KCl+3O2
0,05-----------------------0,075
n Mg=\(\dfrac{3,6}{24}\)=0,15 mol
=>VO2=0,075.22,4=1,68l
=>m KClO3=0,05.122,5=6,125g
Đúng 3
Bình luận (0)
a. \(n_{Mg}=\dfrac{3.6}{24}=0,15\left(mol\right)\)
PTHH : 2Mg + O2 ----to----> 2MgO
0,15 0,075
\(V_{O_2}=0,075.22,4=1,68\left(l\right)\)
b. PTHH : 2KClO3 \(\xrightarrow[MnO_2]{t^o}\) 2KCl + 3O2
0,05 0,075
\(m_{KClO_3}=0,05.122,5=6,125\left(g\right)\)
Đúng 1
Bình luận (0)
Nung 39,4 gam kali clorat (KClO3) sinh ra 14,9 gam kali clorua (KCl) và khí oxi.
a. Lập phương trình hoá học.
b. Biết sau phản ứng, khối lượng chất rắn giảm 4,8 gam, tính % khối lượng kali clorat tham gia phản
ứng.
Nung nóng kali clorat KClO3 thu được 3,36 lít khí oxi (đktc) và muối kali clorua KCL
a) Viết phương trình phản ứng
b) Tính khối lượng KClO3 cần dùng.
c) Tính khối lượng muối Kali clorua thu được
a) 2KClO3 --to--> 2KCl + 3O2
b) \(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,1<----------0,1<---0,15
=> \(m_{KClO_3}=0,1.122,5=12,25\left(g\right)\)
c) \(m_{KCl}=0,1.74,5=7,45\left(g\right)\)
Đúng 2
Bình luận (0)