Dựa vào tính chất hóa học của muối cacbonat, hãy nêu tính chất hóa học của muối CaCO3 và viết các phương trình hóa học minh họa.
Giúp mình với!
1,tính chất hóa học của AXIT viết 5 phương trình minh họa
2,tính chất hóa học của BAZO viết 5 phương trình minh họa
3,tính chất hóa học của MUỐI viết 5 phương trình minh họa
4,tính chất hóa học của NHÔM viết 5 phương trình minh họa
5,tính chất hóa học của SẮT viết 5 phương trình minh họa
6,tính chất hóa học của CLO viết 5 phương trình minh họa
7,ĐIỀU KIỆN XẢY RA PHẢN ỨNG TRAO ĐỔI
HELP ME!!!!! MK ĐG CẦN GẤP
nêu tính chất hóa học của muối và viết phương trình hóa học
Tác dụng với kim loại
\(Mg+FeSO_4\rightarrow MgSO_4+Fe\)
Tác dụng với axit:
\(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
Tác dụng với dd bazo:
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
Tác dụng vơi dd muối:
\(NaCl+AgNO_3\rightarrow AgCl+NaNO_3\)
Phản ứng phân hủy muối:
\(CaCO_3\xrightarrow[]{t^0}CaO+CO_2\)
`#3107.101107`
`@` Tính Chất Hóa Học của Muối:
`1)` Phản ứng với Kim Loại
Kim Loại + Muối `\rightarrow` Muối Mới + Kim Loại Mới
\(\text{Fe + CuSO}_4\rightarrow\text{ FeSO}_4+\text{Cu}\)
`2)` Phản ứng với Acid
Acid + Muối `\rightarrow` Muối Mới + Acid Mới
Điều kiện: sản phẩm có chất kết tủa hoặc có khí
\(\text{BaCl}_2+\text{H}_2\text{SO}_4\rightarrow\text{ BaSO}_4+\text{2HCl}\)
`3)` Phản ứng với muối
Muối + Muối `\rightarrow` 2 Muối Mới
Điều kiện: sản phẩm kết tủa
\(\text{BaCl}_2+\text{Na}_2\text{SO}_4\rightarrow\text{ BaSO}_4+\text{ 2NaCl}\)
`4)` Phản ứng với base
Muối + Base `\rightarrow` Muối Mới + Base Mới
\(\text{CuSO}_4+\text{2NaOH}\rightarrow\text{ Cu(OH)}_2+\text{Na}_2\text{SO}_4.\)
Chọn dụng cụ, hóa chất cần thiết, nêu cách tiến hành, cho biết hiện tượng và viết phương trình phản ứng để chứng minh :
a. Tính chất hóa học của bazo (natri hidroxit tác dụng với muối).
b. Tính chất hóa học của muối (bari clorua tác dụng với axit).
Tham khảo:
a. Dụng cụ, hóa chất:
- Dụng cụ: ống nghiệm, kẹp gỗ.Hóa chất: dung dịch NaOH, dung dịch FeCl3.
- Cách tiến hành:
+ Nhỏ vài giọt dung dịch NaOH vào ống nghiệm có chứa 1 ml dung dịch FeCl3.
+ Lắc nhẹ ống nghiệm.
- Hiện tượng – giải thích: Ta thấy kết tủa nâu đỏ xuất hiện, kết tủa đó là \(Fe\left(OH\right)_3\)
\(PTHH:3NaOH+FeCl_3\rightarrow Fe\left(OH\right)_3\downarrow+3NaCl\)
- Kết luận: Bazơ tác dụng với muối tạo thành muối mới và bazơ mới.
b. Dụng cụ, hóa chất:
- Dụng cụ: ống nghiệm, kẹp gỗ.Hóa chất: dung dịch BaCl2, dung dịch H2SO4 loãng.
- Cách tiến hành:
+Nhỏ vài giọt dung dịch BaCl2 vào ống nghiệm có chứa 1 ml dung dịch H2SO4 loãng.
- Hiện tượng – giải thích: Dung dịch xuất hiện kết tủa trắng, là BaSO4.
\(PTHH:BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
- Kết luận: Muối tác dụng với axit tạo thành muối mới và axit mới.
1. thế nào là phản ứng trao đổi? viết 3 phương trình hóa học minh họa?
2. tính chất hóa học đặo trưng ( khác so với axit ) của H2SO4 đặc.
3. tính chất hóa học của các hợp chất: Oxit, Axit, Bazơ, Muối.
4. điều chế 1 số hợp chất quan trong: SO2, CaO, H2SO4, Ca(OH)2, NaCL.
5. pha chế dung dịch H2SO4 loãng từ dung dịch H2SO4 đặc.
6. pha chế dung dịch Ca(OH)2 từ CaO.
7. hiện tượng 1 số thí nghiệm:
a. cho dd NaSO4 vào dd BaCL2.
b. cho dd Na2CO3 vào dd HCL.
c. đinh sắt cho vào dd CuSO4.
d. cho dd H2SO4 vào dd BaCL2.
e. cho dd H2SO4 đặc vào đường saccarozơ.
f. cho dd ALCL3 vào dd NaOH ( có dư).
g. cho nước cất vào CaO, sau đó cho dd phenolphtalein.
cho dd NaCO4 vào dd CaCL2.
( cần gấp ạ)
Câu 1: Nêu tính chất hóa học của O2 . Viết phương trình minh họa. Chỉ rõ vai trò của O2 trong phản ứng.
Câu 2: Nêu tính chất hóa học của S . Viết phương trình minh họa. Chỉ rõ vai trò của S trong từng phản ứng.
Câu 3: Nêu tính chất hóa học của H2S. Viết phương trình minh họa.Chỉ rõ vai trò của H2S trong mỗi phản ứng.
Câu 4: Nêu tính chất hóa học của SO2. Viết phương trình minh họa. Trong phản ứng nào SO2 thể hiện tính khử, tính oxi hóa? Trong phản ứng nào SO2 là oxit axit?
Mình nghĩ cái này thuộc kiến thức cơ bản, bạn nên tự học trong SGK thì hơn là đi đăng câu hỏi ở Hoc24
Nêu thành phần hóa học và tính chất hóa học của nước? Viết phương trình phản ứng minh họa
Câu 6:(1 điểm). Nêu tính chất hóa học của rượu etylic, mỗi tính chất viết một phương trình hóa học minh họa
Trình bày tính chất hóa học của nước và viết các phương trình hóa học minh họa
Tính chất hóa học của nước :
Nước có thể tác dụng với một số kim loại ở nhiệt độ thường :
Pt : Ca + 2H2O \(\rightarrow\) Ca(OH)2 + H2
Na + 2H2O \(\rightarrow\) 2NaOH + H2
Tác dụng với oxit bazo :
Pt : CaO + H2O \(\rightarrow\) Ca(OH)2
K2O + H2O \(\rightarrow\) 2KOH
Tác dụng với oxit axit
Pt : SO3 + H2O \(\rightarrow\) H2SO4
P2O5 + 3H2O \(\rightarrow\) 2H3PO4
Chúc bạn học tốt
Tính chất hh của nước:
✱Tác dụng với kim loại:
VD: Na + H2O → NaOH + \(\dfrac{1}{2}\)H2↑
Ca + 2 H2O → CaOH + H2↑
✱Tác dụng với oxit bazơ:
VD: K2O + H2O → KOH
BaO + H2O → Ba(OH)2
✱Tác dụng với oxit axit:
VD: CO2 + H2O → H2CO3
SO2 + H2O → H2SO3
Tính chất hóa học của nước :
Nước có thể tác dụng với một số kim loại ở nhiệt độ thường :
Pt : Ca + 2H2O →→ Ca(OH)2 + H2
Na + 2H2O →→ 2NaOH + H2
Tác dụng với oxit bazo :
Pt : CaO + H2O →→ Ca(OH)2
K2O + H2O →→ 2KOH
Tác dụng với oxit axit
Pt : SO3 + H2O →→ H2SO4
P2O5 + 3H2O →→ 2H3PO4
Nêu những tính chất hóa học giống và khác nhau giữa silic và cacbon. Viết các phương trình hóa học để minh họa ?
Tính chất giống nhau
- Đều có tính oxi hoá
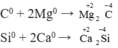
- Đều có tính khử
Tác dụng với phi kim
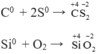
Tác dụng với hợp chất:
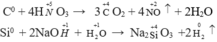
Câu 2: Dựa vào các số oxi hóa của Cacbon hãy đự đoán tính chất hóa học (Tính khử, tính oxi hóa) của C, CO, CO2, H2CO3. Mỗi tính chất viết 1 phương trình chứng minh.
Số oxi hóa của cacbon: -4, 0, +2, +4
Tính khử: \(C+O_2\underrightarrow{t^o}CO_2\)
Tính oxi hóa: \(C+2H_2\underrightarrow{t^o}CH_4\)