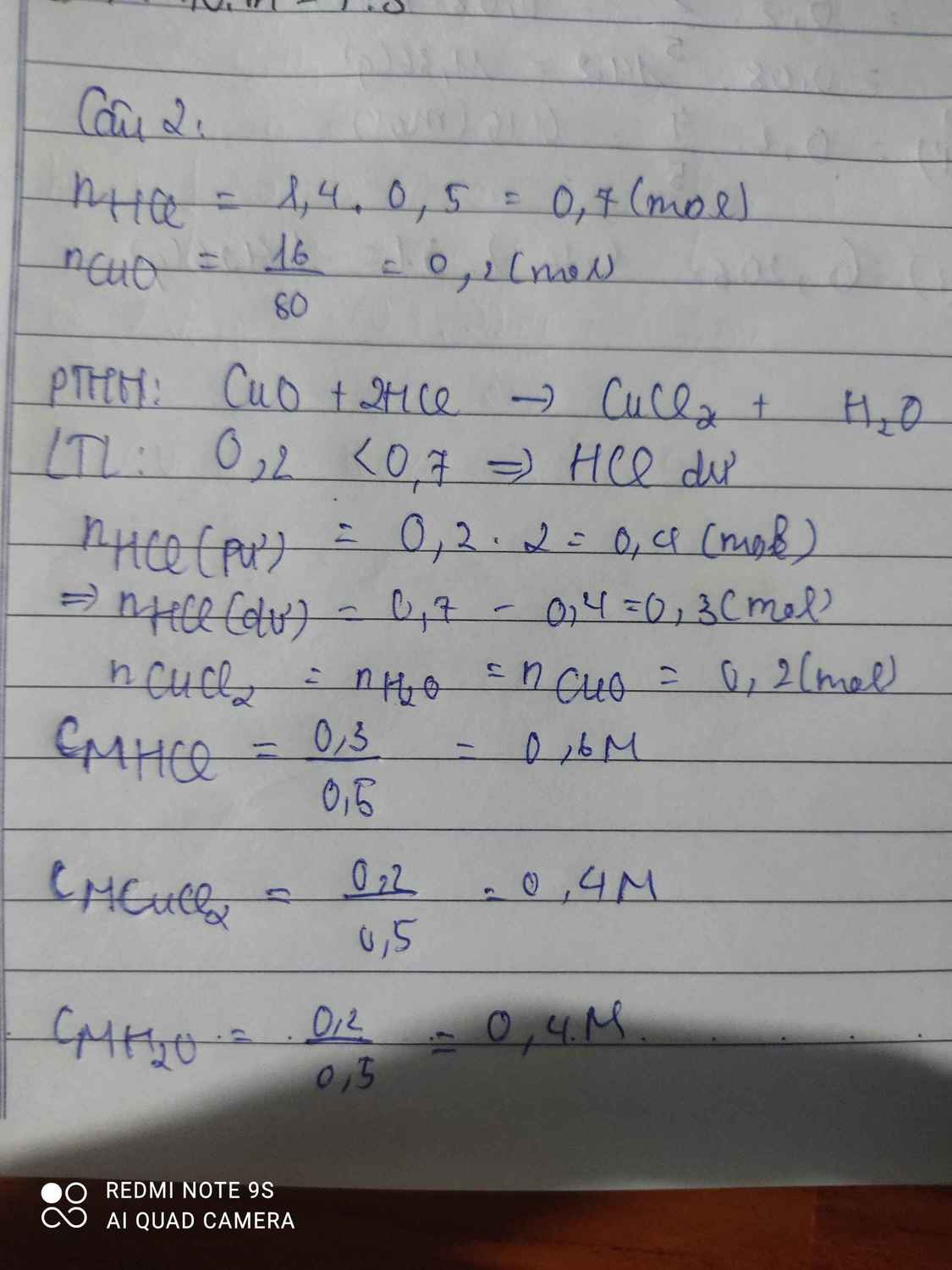Khi dẫn 2,24 lit H2S qua 500 ml dung dich NaOH có nồng độ lần lưot là 0,1M; 0,2 M; 0,3M; 0,4M; 0,5M thu dưoc dung dịch A. Xác định nồng đo mol/ các chất trong dung dịch sau phản ứng.

Những câu hỏi liên quan
Cho 500 ml dung dịch NaOH 1,8 M phản ứng với 500 ml dung dịch FeCl3 0,8 M thu được dung dịch A và chất rắn B.
Xác định: Khối lượng chất rắn B và nồng độ mol/lit mỗi chất trong dung dịch A .
nNaOH=0,5. 1,8=0,9(mol)
nFeCl3=0,8.0,5=0,4(mol)
PTHH: 3 NaOH + FeCl3 -> Fe(OH)3 + 3 NaCl
Vì: 0,9/3 < 0,4/1
=>FeCl3 dư, NaOH hết, tính theo nNaOH
Ta có: nFe(OH)3= nFeCl3(p.ứ)=nNaOH/3=0,9/3=0,3(mol)
nNaCl=nNaOH=0,9(mol)
nFeCl3(dư)=0,4-0,3=0,1(mol)
=>m(rắn)=mFe(OH)3= 108. 0,3= 32,4(g)
Vddsau=0,5+0,5=1(l)
=>CMddFeCl3(dư)=0,1/1=0,1(M)
CMddNaCl=0,9/1=0,9(M)
Đúng 2
Bình luận (0)
Câu 2: Cho 500 ml dung dịch HCl 1,4 M phản ứng với 16 gam CuO thu được dung dịch A. Xác định khối lượng và nồng độ mol/lit mỗi chất trong dung dịch A .
CuO + 2HCl ------> CuCl2 + H2O
nHCl bđ = 0.5.1.4 = 0.7
nCuO = \(\dfrac{16}{80}\)= 0.2 mol
=> nHCl pư = 0.4 mol
=> nHCl dư = 0.3 mol
Dung dịch A gồm CuCl2 và HCl dư
mCuCl2 = 0.2.135 = 27g
mHCl dư = 0.3.36.5 = 10.95g
CM CuCl2 = \(\dfrac{0,2}{0,5}\)= 0.4M
CM HCl dư =\(\dfrac{0,3}{0,5}\) = 0.6M
Đúng 2
Bình luận (0)
cho 69,6 g MnO tác dụng với dung dịch HCl đặc , dư . Dẫn khí thoát ra đi vào 500 ml dung dịch NaOH 4M ( ở nhiệt độ thường ) : a) viết phương trình hóa học của các phản ứng xảy ra ; b) xác định nồng độ mol của những chất có trong dung dịch sau phản ứng . Biết rằng thể tích của dung dịch sau phản ứng thay đổi không đáng kể .
Trung hòa 100 ml dung dịch CH3COOH 0,3M bằng dung dịch NaOH 1,5M. a) Tính thể tích dung dịch NaOH đã dùng ? b) Tính khối lượng muối thu được sau phản ứng ? c) Tính nồng độ mol của chất tan có trong dung dịch sau phản ứng ( biết thể tích thay đổi không đáng kể) ? Biết C= 12; O= 16; H = 1 ; Na=23
a) \(n_{CH_3COOH}=0,1.0,3=0,03\left(mol\right)\)
PTHH: CH3COOH + NaOH --> CH3COONa + H2O
0,03---->0,03--------->0,03
=> \(V_{dd.NaOH}=\dfrac{0,03}{1,5}=0,02\left(l\right)\)
b) mCH3COONa = 0,03.82 = 2,46 (g)
c) \(C_{M\left(CH_3COONa\right)}=\dfrac{0,03}{0,1+0,02}=0,25M\)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 3,4 gam hợp chất A, thu được 2,24 lít khí
SO
2
(đktc) và 1,8 gam
H
2
O
. Dẫn khí
SO
2
thu được ở trên vào 146,6 gam dung dịch, trong đó có hoà tan 0,3 mol NaOH. Hãy xác định nồng độ phần trăm các chất có trong dung dịch sau phản ứng.
Đọc tiếp
Đốt cháy hoàn toàn 3,4 gam hợp chất A, thu được 2,24 lít khí SO 2 (đktc) và 1,8 gam H 2 O . Dẫn khí SO 2 thu được ở trên vào 146,6 gam dung dịch, trong đó có hoà tan 0,3 mol NaOH. Hãy xác định nồng độ phần trăm các chất có trong dung dịch sau phản ứng.
Nồng độ phần trăm của các chất trong dung dịch :
Biết số mol NaOH (0,3 mol) nhiều hơn 2 lần số mol SO 2 (0,1 mol) vậy sản phẩm là muối Na 2 SO 3 . Ta có PTHH :
SO 2 + 2NaOH → Na 2 SO 3 + H 2 O
- Khối lượng của dung dịch sau phản ứng :
m dd = 146,6 + 3,4 = 150 (g)
- Khối lượng các chất có trong dung dịch sau phản ứng :
m Na 2 SO 3 = 126.0,1 = 12,6g
m NaOH dư = 40.(0,3 - 0,2) = 4g
- Nồng độ phần trăm các chất trong dung dịch sau phản ứng :
C % Na 2 SO 3 = 12,6/150 x 100% = 8,4%
C % NaOH dư = 4/150 x 100% = 2,67%
Đúng 0
Bình luận (0)
Dẫn từ từ 13,44 lít khí CO2 ở đktc vào 500 ml dung dịch NaOH 1,5. Tính nồng độ mol/l của các chất có trong dung dịch sau phản ứng.
$n_{CO_2} = \dfrac{13,44}{22,4} = 0,6(mol) ; n_{NaOH} = 0,5.1,5 = 0,75(mol)$
Ta có :
$1 < n_{NaOH} : n_{CO_2} = 0,75 : 0,6 = 1,25 < 2$ nên sản phẩm có $Na_2CO_3(a\ mol) ; NaHCO_3(b\ mol)$
Ta có :
$n_{CO_2} = a + b = 0,6(mol)$
$n_{NaOH} = 2a + b = 0,75(mol)$
Suy ra: a = 0,15 ; b = 0,45
$C_{M_{Na_2CO_3}} = \dfrac{0,15}{0,5} = 0,3M$
$C_{M_{NaHCO_3}} = \dfrac{0,45}{0,5} = 0,9M$
Đúng 2
Bình luận (0)
Hòa tan hết 17,05 gam hỗn hợp Zn và Al vào 500 ml dung dịch HCl 2M, thu được 9,52 lít H2 (đktc).a/ Tính khối lượng mỗi kim loại trong hỗn hợp đầu. 13 gam + 4,05 gamb/ Tính nồng độ mol các chất trong dung dịch sau phản ứng. 0,4M + 0,3M + 0,3Mc/ Tính nồng độ % các chất trong dung dịch sau phản ứng, biết dung dịch HCl ban đầu có khối lượng riêng là 1,05 g/ml. 5,03
Đọc tiếp
Hòa tan hết 17,05 gam hỗn hợp Zn và Al vào 500 ml dung dịch HCl 2M, thu được 9,52 lít H2 (đktc).
a/ Tính khối lượng mỗi kim loại trong hỗn hợp đầu. 13 gam + 4,05 gam
b/ Tính nồng độ mol các chất trong dung dịch sau phản ứng. 0,4M + 0,3M + 0,3M
c/ Tính nồng độ % các chất trong dung dịch sau phản ứng, biết dung dịch HCl ban đầu có khối lượng riêng là 1,05 g/ml. 5,03
a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Gọi: \(\left\{{}\begin{matrix}n_{Zn}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\) ⇒ 65x + 27y = 17,05 (1)
Ta có: \(n_{H_2}=\dfrac{9,52}{22,4}=0,425\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}+\dfrac{3}{2}n_{Al}=x+\dfrac{3}{2}y=0,425\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=0,2\left(mol\right)\\n_{Al}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=0,2.65=13\left(g\right)\\m_{Al}=0,15.27=4,05\left(g\right)\end{matrix}\right.\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{ZnCl_2}=n_{Zn}=0,2\left(mol\right)\\n_{AlCl_3}=n_{Al}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{ZnCl_2}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\\C_{M_{AlCl_3}}=\dfrac{0,15}{0,5}=0,3\left(M\right)\end{matrix}\right.\)
c, Ta có: m dd HCl = 1,05.500 = 525 (g)
m dd sau pư = mhh + m dd HCl - mH2 = 541,2 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{ZnCl_2}=\dfrac{0,2.136}{541,2}.100\%\approx5,03\%\\C\%_{AlCl_3}=\dfrac{0,15.133,5}{541,2}.100\%\approx3,7\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Cho 2,61 gam MnO2 vào 18,25 gam dung dịch HCl 30% sau phản ứng thu được dung dịch a và khí b dẫn khí thu được sau phản ứng dẫn qua 50 ml dung dịch NaOH 2 m ở nhiệt độ thường thu được dung dịch X
a)Tính nồng độ phần trăm chất trong dung dịch a b)Tính nồng độ mol lít chất trong dung dịch X Giả sử thể tích dung dịch không thay đổi
Cho 4,35 g MnO2 tác dụng với dung dịch HCl đặc, dư. Dẫn khi thoát ra đi vào 300ml dung dịch NaOH có nồng độ 0,1 M (ở nhiệt độ thường).
a) Viết phương trình hoá học của các phản ứng xảy ra.
b) Xác định nồng độ mol của những chất có trong dung dịch sau phản ứng
Xem chi tiết
\(n_{MnO_2} = \dfrac{4,35}{87} = 0,05(mol)\)
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
0,05..................................0,05..................(mol)
\(n_{NaOH} = 0,3.0,1 = 0,03(mol)\)
2NaOH + Cl2 → NaCl + NaClO + H2O
0,03........0,05.....0,015.......0,015....................(mol)
Vậy :
\(C_{M_{NaCl}} = C_{M_{NaClO}} = \dfrac{0,015}{0,3} = 0,05M\)
Đúng 4
Bình luận (0)