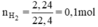Cho các kim loại Al và Zn vs các dung dịch axit HCl và H2SO4 loãng.
a.Viết tất cả các ptpư điều chế H2 từ các chất trên.
b.Phải dùng bao nhiêu gam nhôm,bao nhiêu gam kẽm để từ mỗi kim loại điều chế đc 13,44l khí H2(ở đktc).
c.Nếu dùng một lượng bôt nhôm và bột kẽm có khối lượng bằng nhauthì trường hợp nào sinh đc nhiều khí H2 hơn?