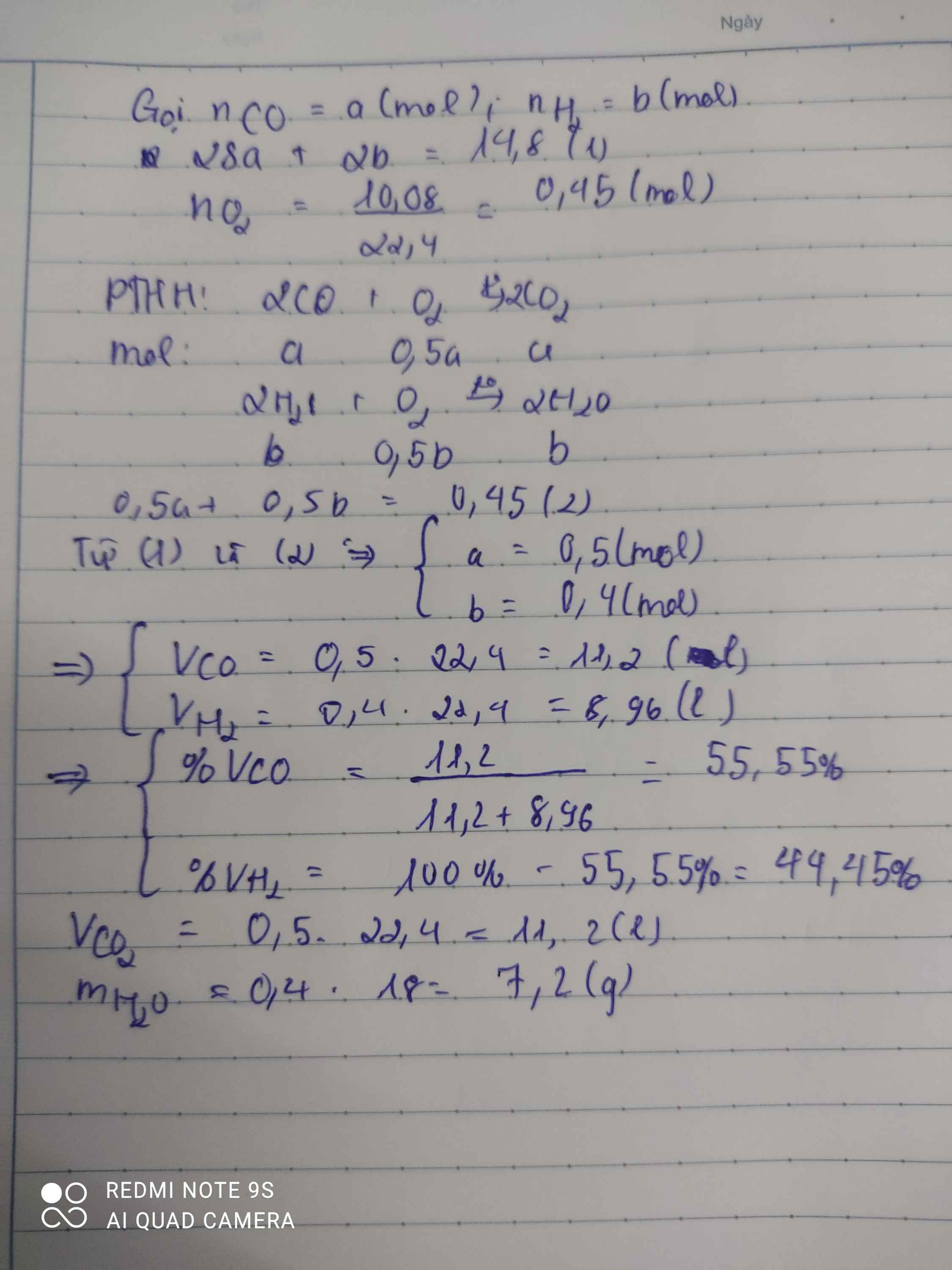Đốt 9,84(g) hỗn hợp gồm CO2 và S trong đó CO2 chiếm 2,44% về khối lượng. Tính thành phần % thể tích các khí sinh ra.

Những câu hỏi liên quan
Đốt cháy hoàn toàn 10 g hỗn hợp gồm C và S (trong đó C chiếm 36 % về khối lượng). Hãy tính:
Thể tích không khí cần dùng (biết oxi chiếm 20% thể tích không khí).
Thể tích hỗn hợp khí CO2 và SO2 sinh ra. Biết các khí đều đo ở đktc.
\(m_C=10.36\%=3,6\left(g\right)\Rightarrow n_C=0,3\left(mol\right)\)
\(m_S=10-3,6=6,4\left(g\right)\Rightarrow n_S=0,2\left(mol\right)\)
\(C+O_2-^{t^o}\rightarrow CO_2\)
\(S+O_2-^{t^o}\rightarrow SO_2\)
\(n_{O_2}=0,3+0,2=0,5\left(mol\right)\)
Vì oxi chiếm 20% thể tích không khí
=> \(V_{kk}=\dfrac{0,5.22,4}{20\%}=56\left(lít\right)\)
\(n_{hh}=n_{CO_2}+n_{SO_2}=0,3+0,2=0,5\left(mol\right)\)
=> \(V_{hh}=0,5.22,4=11,2\left(lít\right)\)
Đúng 2
Bình luận (0)
PTHH: C+O2→CO20,3mol:0,3mol→0,3molC+O2→CO20,3mol:0,3mol→0,3mol
S+O2→SO20,2mol:0,2mol→0,2molS+O2→SO20,2mol:0,2mol→0,2mol
mS=10−3,6=6,4(g)⇔nS=6,432=0,2(mol)mS=10−3,6=6,4(g)⇔nS=6,432=0,2(mol)
VO2=(0,3+0,2)22,4=11,2(l)VO2=(0,3+0,2)22,4=11,2(l)
mhh=mCO2+mSO2=0,3.44+0,2.64=26(g)
Đúng 0
Bình luận (0)
Bài 1: Đốt cháy hoàn toàn 10 Kg hỗn hợp gồm C và S (trong đó C chiếm 36 % về khối lượng). Hãy tính:
a) Thể tích không khí cần dùng (biết oxi chiếm 20% thể tích không khí).
b) Thể tích hỗn hợp khí CO2 và SO2 sinh ra. Biết các khí đều đo ở đktc.
\(a,m_C=10.36\%=3,6\left(kg\right)=3600\left(g\right)\\ n_C=\dfrac{3600}{12}=300\left(mol\right)\\ m_S=10-3,6=6,4\left(kg\right)=6400\left(g\right)\\ n_S=\dfrac{6400}{32}=200\left(mol\right)\\ C+O_2\rightarrow\left(t^o\right)CO_2\\ S+O_2\rightarrow\left(t^o\right)SO_2\\ n_{O_2\left(tổng\right)}=n_C+n_S=300+200=500\left(mol\right)\\ V_{O_2\left(tổng\right)\left(đktc\right)}=500.22,4=11200\left(l\right)\\ V_{kk}=\dfrac{100}{20}V_{O_2\left(tổng\right)\left(đktc\right)}=5.11200=56000\left(l\right)\\ b,V_{hh\left(CO_2,SO_2\left(đktc\right)\right)}=22,4.\left(n_C+n_S\right)=22,4.\left(300+200\right)=11200\left(l\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 8 g hỗn hợp gồm CH4 và c2h4 trong đó CH4 chiếm 30% về khối lượng. Tính khối lượng mỗi khí trong 8 g hỗn hợp ban đầu .Tính khối lượng khí CO2 sinh ra
Xem chi tiết
\(m_{CH_4} = 8.30\% = 2,4(gam)\\ m_{C_2H_4} = 8 - 2,4 = 5,6(gam)\\ CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O\\\)
Theo PTHH :
\(n_{CO_2} = n_{CH_4} + 2n_{C_2H_4} = \dfrac{2,4}{16} + \dfrac{5,6}{28}.2 = 0,55(mol)\\ \Rightarrow m_{CO_2} = 0,55.44 = 24,2(gam)\)
Đúng 1
Bình luận (0)
\(m_{CH_4}=0.3\cdot8=2.4\left(g\right)\)
\(n_{CH_4}=\dfrac{2.4}{16}=0.15\left(mol\right)\)
\(m_{C_2H_4}=8-2.4=5.6\left(g\right)\)
\(n_{C_2H_4}=\dfrac{5.6}{28}=0.2\left(mol\right)\)
\(CH_4+2O_2\underrightarrow{t^0}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^0}2CO_2+2H_2O\)
\(n_{CO_2}=2\cdot0.15+0.2=0.5\left(mol\right)\)
\(m_{CO_2}=0.5\cdot44=22\left(g\right)\)
Đúng 0
Bình luận (0)
Đốt 9,84(g) hỗn hợp gồm Cacbon và lưu huỳnh trong đó Cacbonchiếm 2,44% về khối lượng. Tính thành phần % thể tích các khí sinh ra.
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 14,8 g hỗn hợp khí gồm CO và H2 cần dùng 10,08 l khí O2 Tính:
a. Thành phần % về thể tích mỗi khí trong hỗn hợp ban đầu(đktc)
b. Thể tích khí CO2 và khối lượng nước thu được(đktc)
Câu 4: Đốt cháy một hỗn hợp gồm CH4 và C2H2 có thể tích là 33,6 lít (đktc) thu được 56 lít khí CO2 (đktc).a. Xác định thành phần % về thể tích các khí trong hỗn hợp?b. Tính khối lượng của oxi cần để đốt cháy hoàn toàn hỗn hợp khí trên?
Đọc tiếp
Câu 4: Đốt cháy một hỗn hợp gồm CH4 và C2H2 có thể tích là 33,6 lít (đktc) thu được 56 lít khí CO2 (đktc).
a. Xác định thành phần % về thể tích các khí trong hỗn hợp?
b. Tính khối lượng của oxi cần để đốt cháy hoàn toàn hỗn hợp khí trên?
a, \(CH_4+2O_2\underrightarrow{t^o}CO_2+H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Ta có: \(n_{CH_4}+n_{C_2H_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\left(1\right)\)
Theo PT: \(n_{CO_2}=n_{CH_4}+2n_{C_2H_2}=\dfrac{56}{22,4}=2,5\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,5\left(mol\right)\\n_{C_2H_2}=1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,5.22,4}{33,6}.100\%\approx33,33\%\\\%V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
b, Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=3,5\left(mol\right)\Rightarrow m_{O_2}=3,5.32=112\left(g\right)\)
Đúng 3
Bình luận (1)
Đốt cháy hỗn hợp gồm H2 và Cacbon oxit có khối lượng là 13,6 g cần dùng hết 17,92 lít khí CO2 điều kiện chuẩn .biết rằng sản phẩm gồm CO2 và hơi nước
a.phương trình khối lượng mỗi khí trong hỗn hợp đầu
b.thành phần % về thể tích của hỗn hợp đầu
$2H_2 + O_2 \xrightarrow{t^o} 2H_2O$
$2CO + O_2 \xrightarrow{t^o} 2CO_2$
$n_{CO} = n_{CO_2} = \dfrac{17,92}{22,4} = 0,8(mol)$
$\Rightarrow n_{H_2} = \dfrac{13,6 - 0,8.28}{2} = -4,4<0$
$\to$ Sai đề
Đúng 1
Bình luận (0)
Đốt cháy hỗn hợp khí gồm CH4, C2H2 trong không khí thì thu được 6,72 lít khí CO2 (đktc) a. Tính thành phần % khối lượng và thành phần % thể tích của mỗi khí trong hỗn hợp biết thể tích khí CH4 là 1,12 lít b. Tính thể tích không khí cần dùng để đốt cháy hết lượng hỗn hợp trên
a) \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,05-->0,1------->0,05
2C2H2 + 5O2 --to--> 4CO2 + 2H2O
0,125<--0,3125<----0,25
=> \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,05}{0,05+0,125}.100\%=28,57\%\\\%V_{C_2H_2}=\dfrac{0,125}{0,05+0,125}.100\%=71,43\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,05.16}{0,05.16+0,125.26}.100\%=19,753\%\\\%m_{C_2H_2}=\dfrac{0,125.26}{0,05.16+0,125.26}.100\%=80,247\%\end{matrix}\right.\)
b) \(n_{O_2}=0,1+0,3125=0,4125\left(mol\right)\)
=> \(V_{O_2}=0,4125.22,4=9,24\left(l\right)\)
=> Vkk = 9,24.5 = 46,2 (l)
Đúng 0
Bình luận (2)
Nung hỗn hợp X gồm FeCO3, FeS và Fe(NO3)2 trong không khí ở nhiệt độ cao, đến phản ứng hoàn toàn, thu được Fe2O3 duy nhất và hỗn hợp Y gồm CO2, SO2, NO2, N2; trong đó SO2 chiếm 8,75% về thể tích và thể tích khí NO2 gấp đôi thể tích khí CO2. Các khí đều đo cùng điều kiện áp suất và nhiệt độ; trong không khí, O2 chiếm 20% về thể tích, còn lại là N2. Phần trăm khối lượng của FeCO3 trong hỗn hợp X là A. 31,10%. B. 25,17%. C. 65,10%. D. 13,92%.
Đọc tiếp
Nung hỗn hợp X gồm FeCO3, FeS và Fe(NO3)2 trong không khí ở nhiệt độ cao, đến phản ứng hoàn toàn, thu được Fe2O3 duy nhất và hỗn hợp Y gồm CO2, SO2, NO2, N2; trong đó SO2 chiếm 8,75% về thể tích và thể tích khí NO2 gấp đôi thể tích khí CO2. Các khí đều đo cùng điều kiện áp suất và nhiệt độ; trong không khí, O2 chiếm 20% về thể tích, còn lại là N2. Phần trăm khối lượng của FeCO3 trong hỗn hợp X là
A. 31,10%.
B. 25,17%.
C. 65,10%.
D. 13,92%.
Đáp án A

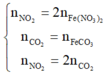
![]()

n S O 2 = 8 , 75 % n Y → b = 8 , 75 % ( 3 a + b + 4 c ) B T N T ( O ) : 3 a + 6 a + 2 c = 3 a + 1 , 5 b + 2 a + 2 b + 4 a → c = 1 , 75 a
→ b = 7 8 a
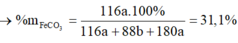
Đúng 0
Bình luận (0)