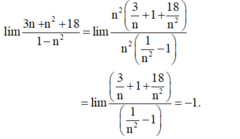n2.n.n5=711chia73

Những câu hỏi liên quan
Câu 9: Có các khí: NH3, CO, CO2, N2. Khối lượng mol của những khí nào bằng nhau:
A. NH3, N2 B. CO, CO2 C. CO2, N2 D. CO, N2
D
MCO = 12 + 16 = 28(g/mol)
MN2 = 14.2 = 28(g/mol)
Đúng 2
Bình luận (0)
Trong phản ứng hóa học nào sau đây, nitơ thể hiện tính khử?A. 3Mg +
N
2
→
M
g
3
N
2
B. 2Al +
N
2
→ 2AlNC.
N
2
+ 3
H
2
→ 2
N
H
3
D.
N
2
+...
Đọc tiếp
Trong phản ứng hóa học nào sau đây, nitơ thể hiện tính khử?
A. 3Mg + N 2 → M g 3 N 2
B. 2Al + N 2 → 2AlN
C. N 2 + 3 H 2 → 2 N H 3
D. N 2 + O 2 → 2NO
2. Khi nói về chiết suất giữa hai môi trường với n1,n2 lần lượt là chiết suất của môi trường 1 và môi trường 2. Biểu thức chỉ đúng Nokia quan hệ giữa n1,n2 A. n12= n2. n1 B. n12.n21=1 C. n12= n2/n1 D. n1.n2=1
Gọi n1, n2 lần lượt là chiết suất của môi trường A và môi trường B đối với một ánh sáng đơn sắc. Chiết suất tỉ đối của môi trường A so với môi trường B là: n12=\(\dfrac{n1}{n2}\)
Đúng 0
Bình luận (0)
l i m 3 n + n 2 + 18 1 - n 2 bằng
A. 3
B. 18
C. -1
D. 1
hỗn hợp khí A gồm 5,6 lít khí NH3, 11,2 lít khí N2, 28 lít không khí . biết khí N2 chiếm 4/5 thể tích không khí và M không khí = 29g
a/ tính % về thể tích khí N2 trong A
b/ tính % về số mol của khí N2 trong A
c/ tính % khối lượng của khí N2 trong A
a) \(V_{N_2\left(kk\right)}=28.\dfrac{4}{5}=22,4\left(l\right)\)
\(\Rightarrow V_{N_2\left(A\right)}=22,4+11,2=33,6\left(l\right)\)
=> \(\%V_{N2\left(A\right)}=\dfrac{33,6}{5,6+11,2+28}.100=75\%\)
b) Ta có % về thể tích cũng là % về số mol
=> %nN2(A) = 75%
c)\(n_{N_2\left(A\right)}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\)
\(\Rightarrow\%m_{N_2\left(A\right)}=\dfrac{1,5.28}{\dfrac{5,6}{22,4}.17+\dfrac{11,2}{22,4}.28+\dfrac{28}{22,4}.29}.100=77,06\%\)
Đúng 1
Bình luận (0)
nhập vào 2 số nguyên dương n1,n2 (n1 bé hơn n2) đếm xem từ n1 đến n2 có bao nhiêu số chẵn
#include <bits/stdc++.h>
using namespace std;
long long a,b,i,dem;
int main()
{
cin>>a>>b;
dem=0;
for (i=a; i<=b; i++) if (i%2==0) dem++;
cout<<dem;
}
Đúng 1
Bình luận (0)
Var n1,n2,i,dem:integer;
Begin
Write('Nhap n1 = ');readln(n1);
Write('Nhap n2 = ');readln(n2);
For i:=n1 to n2 do
If i mod 2 = 0 then dem:=dem+1;
Write('Co ',dem,' so chan');
Readln;
End.
Đúng 0
Bình luận (0)
N2--->NH3--->NH4Cl--->NH3--->NH4NO3--->N2
N2 + 3H2 = 2NH3
NH3 + HCL = NH4Cl
NH4Cl = NH3 + HCL
NH3 + HNO3 = NH4NO3
2NH4NO3 = 2N2 + O2 + 4H2O
Đúng 0
Bình luận (0)
Hỗn hợp khí A gồm N2 và H2 có: dA/N2=0,35
a) Tìm % n2?%H2
b)Tìm %khối lượng của mỗi khí trong hỗn hợp
\(GS:n_A=1\left(mol\right)\)
\(n_{N_2}=a\left(mol\right),n_{H_2}=b\left(mol\right)\)
\(\Leftrightarrow a+b=1\left(1\right)\)
\(M_A=0.35\cdot28=9.8\left(\dfrac{g}{mol}\right)\)
\(m_A=9.8\cdot1=9.8\left(g\right)\)
\(\Leftrightarrow28a+2b=9.8\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.3,b=0.7\)
\(\%n_{N_2}=\dfrac{0.3}{1}\cdot100\%=30\%\)
\(\%n_{H_2}=70\%\)
\(\%m_{N_2}=\dfrac{0.3\cdot28}{9.6}\cdot100\%=87.5\%\)
\(\%m_{H_2}=12.5\%\)
\(\)
Đúng 1
Bình luận (1)
a) Gọi n N2 = a(mol) ; n H2 = b(mol)
Coi n A = 1(mol)
M A = 0,35.28 = 9,8 (g/mol)
Ta có :
a + b = 1
28a + 2b = 9,8.1
Suy ra a = 0,3 ; b = 0,7
%V N2 = 0,3/1 .100% = 30%
%V H2 = 0,7/1 .100% = 70%
b)
%m N2 = 0,3.28/9,8 . 100% = 85,71%
%m H2 = 100%- 85,71% = 14,29%
Đúng 1
Bình luận (0)
Câu 27: Khí nào trong các khí sau: CO2, N2, SO2, NH3 nhẹ hơn không khí?A.NH3, N2 B.SO2, CO2 C.O2, N2 NH3, SO2
Đọc tiếp
Câu 27: Khí nào trong các khí sau: CO2, N2, SO2, NH3 nhẹ hơn không khí?
A.NH3, N2 B.SO2, CO2 C.O2, N2 NH3, SO2
cho các khí:CO,N2,O2,Cl2,H2.các khí nhẹ hơn không khí là:
A. N2,H2,CO
B. N2,O2,Cl2
C. CO,Cl2
D. Cl2,O2
cho các khí:CO,N2,O2,Cl2,H2.các khí nhẹ hơn không khí là:
A. N2,H2,CO
B. N2,O2,Cl2
C. CO,Cl2
D. Cl2,O2
vì
\(d_{N_2}=\dfrac{14.2}{29}=0,9\Rightarrow nhẹ hơn kk\)
\(d_{H_2}=\dfrac{1.2}{29}=0,06\Rightarrow nhẹ hơnkk\\ d_{CO}=\dfrac{12+16}{29}=0,9\Rightarrow nhẹ hơn kk\)
Đúng 1
Bình luận (0)
Chọn A (Lí giải: Loại B vì Cl2 và O2 nặng hơn không khí. Loại C vì Cl2 nặng hơn không khí. Loại D vì lí do tương tự B)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời