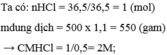Hòa tan hoàn toàn 0.2g natrioxit vào 500ml nước. Biết khối lượng riêng của nước là 1g/ml. Tính nồng độ phần trăm dung dịch thu được

Những câu hỏi liên quan
89. Hoà tan hoàn toàn 0,1mol natrioxit vào 50ml nước. Biết khối lượng riêng của nước là 1g/ml. Nồng độ phần trăm của dung dịch thu được là:A. 14,2% B. 8,1% C. 6,1% D. 7,5%90.Cho các bazơ sau: Fe(OH)3(a) ; NaOH(b) ; Ba(OH)2(c) ; Mg(OH)2(d).1. Các bazơ bị nhiệt phân huỷ là:A. a,c,d;B. a,b,c,d; C. a,d; D. b,c,d2. Các bazơ tác dụng được với SO2 là :A. a,b,d;B. a,b,c,d; C. a,c,d;D. b,c3. Các bazơ tác dụng được với dung dịch H2SO4 là: A. a,c; B. a,b,c,...
Đọc tiếp
89. Hoà tan hoàn toàn 0,1mol natrioxit vào 50ml nước. Biết khối lượng riêng của nước là 1g/ml. Nồng độ phần trăm của dung dịch thu được là:
A. 14,2% | B. 8,1% | C. 6,1% | D. 7,5% |
90.Cho các bazơ sau: Fe(OH)3(a) ; NaOH(b) ; Ba(OH)2(c) ; Mg(OH)2(d).
1. Các bazơ bị nhiệt phân huỷ là:
A. a,c,d; | B. a,b,c,d; | C. a,d; | D. b,c,d |
2. Các bazơ tác dụng được với SO2 là :
A. a,b,d; | B. a,b,c,d; | C. a,c,d; | D. b,c |
3. Các bazơ tác dụng được với dung dịch H2SO4 là:
A. a,c; | B. a,b,c,d; | C. a,d; | D. b,c,d |
4. Các bazơ làm dung dịch phenol phtalein hoá đỏ là :
A. a,d; | B. a,b,c,d; | C. a,c,d; | D. b,c |
89. Hoà tan hoàn toàn 0,1mol natrioxit vào 50ml nước. Biết khối lượng riêng của nước là 1g/ml. Nồng độ phần trăm của dung dịch thu được là:
A. 14,2% | B. 8,1% | C. 6,1% | D. 7,5% |
90.Cho các bazơ sau: Fe(OH)3(a) ; NaOH(b) ; Ba(OH)2(c) ; Mg(OH)2(d).
1. Các bazơ bị nhiệt phân huỷ là:
A. a,c,d; | B. a,b,c,d; | C. a,d; | D. b,c,d |
2. Các bazơ tác dụng được với SO2 là :
A. a,b,d; | B. a,b,c,d; | C. a,c,d; | D. b,c |
3. Các bazơ tác dụng được với dung dịch H2SO4 là:
A. a,c; | B. a,b,c,d; | C. a,d; | D. b,c,d |
4. Các bazơ làm dung dịch phenol phtalein hoá đỏ là :
A. a,d; | B. a,b,c,d; | C. a,c,d; | D. b,c |
Đúng 1
Bình luận (0)
89.Na2O + H2O -> 2NaOH
0.1 0.2
\(mH2O=D\times V=1\times50=50g\)
\(C\%NaOH=\dfrac{0.1\times40\times100}{50+6.2}=7.1\%\)
90.1A 90.2D 90.3B 90.4D
Đúng 0
Bình luận (0)
Hòa tan 36,5 gam HCl vào nước, thu được 500ml dung dịch có khối lượng riêng D = 1,1 g/ml. Tính nồng độ mol và nồng độ phần trăm của dung dịch thu được.
Hòa tan hoàn toàn 10.6g Na2CO3 vào nước được 200ml dung dịch Na2CO3 . Tính nồng độ phần trăm và nồng độ mol của dung dịch trên. Biết khối lượng riêng của dung dịch là 1.05g/ml
\(n_{Na_2CO_3}=\dfrac{10,6}{106}=0,1\left(mol\right)\\ \rightarrow C_{M\left(Na_2CO_3\right)}=\dfrac{0,1}{0,2}=0,5M\)
Ta có: \(C\%=\dfrac{C_M.M}{10.D}\)
\(\rightarrow C\%=\dfrac{0,5.106}{10.1,05}=5,05\%\)
Đúng 1
Bình luận (0)
cho 3,45g một kim loại R thuộc nhóm IA hòa tan hoàn toàn vào 500ml nước được dung dịch A và 1,68l khí ở đktc
a.xách định tên kim loại R
b.tính nồng độ % và nồng độ và nồng đọ mol của dung dịch A biết khối lượng riêng của nước là 1g/ml và coi thể tích dung dịch A = thể tích của nước
HD:
R + H2O ---> ROH + 1/2H2
a) Số mol H2 = 1,68/22,4 = 0,075 mol = 1/2 số mol của R. Suy ra nguyên tử khối của R = 3,45/2.0,075 = 23 (Na).
b) Số mol NaOH = 0,075.2 = 0,15 mol.
Khối lượng dd sau phản ứng = 3,45 + 500 - 2.0,075 = 503.435 g
Suy ra C% = 0,15.40/503.435 = 1,19%; CM = 0,15/0,5 = 0,3 M.
Đúng 0
Bình luận (0)
Hòa tan 30 g NaCl vào 170 gam nước, được dung dịch có khối lượng riêng 1,1 gam/ml. Tính nồng độ phần trăm và nồng độ mol của dung dịch thu được
\(C\%=\dfrac{30}{170}.100\%=17,647\%\)
\(V_{\text{dd}}=\left(30+170\right)1,1=220ml\)
\(n_{NaCl}=\dfrac{30}{58,5}=0,513mol\)
\(C_M=\dfrac{0,513}{0,22}=0,696M\)
\(C\%_{NaCl}=\dfrac{30}{170+30}.100\%=15\%\\ C_M=C\%.\dfrac{10D}{M}=10.\dfrac{10.1,1}{58,5}=1,88M\)
Đúng 1
Bình luận (1)
Đốt cháy hoàn toàn a gam P thu được chất rắn X hòa tan hoàn toàn X vào 500ml dung dịch nước ta được axit có nồng độ 24,5% Tính a (D=1g/ml)
mddH3PO4= 500(g)
=>mH3PO4=500.24,5=122,5(g)
=>nH3PO4=1,25(mol)
PTHH: 4P +5 O2 -to-> 2 P2O5
P2O5 +3 H2O -> 2 H3PO4
nP2O5=1,25/2=0,625(mol)
=>nP=1,25(mol)
=>a=mP=1,25.31=38,75(g)
Chúc em học tốt!
Đúng 2
Bình luận (3)
\(n_{H_3PO_4}=\dfrac{500.1.24,5\%}{98}=1,25\left(mol\right)\)
Bảo toàn nguyên tố P : \(n_P=n_{H_3PO_4}=1,25\left(mol\right)\)
=> \(m_P=1,25.31=38,75\left(g\right)\)
Đúng 2
Bình luận (1)
Hòa tan 10 g đường vào 120ml nước. Tính nồng độ % của dung dịch (Biết khối lượng riêng của nước là 1g/ml)
$m_{H_2O} = D.V = 1.120 = 120(gam)$
$m_{dung\ dịch} = m_{đường} + m_{nước} = 10 + 120 = 130(gam)$
$C\%_{đường} = \dfrac{10}{130} = 7,69\%$
Đúng 2
Bình luận (0)
a) Hòa tan hoàn toàn 8g NaOH vào nước thu được 120g dung dịch. Tính nồng độ mol của dung dịch thu được? Biết dung dịch có khối lượng riêng là 1,2 g/ml.
b) Một dung dịch NaOH có khối lượng riêng là 1,2 g/ml. Khi đem 180 gam dung dịch này đi cô cạn thì thu được 21,6 gam NaOH. Tính nồng độ mol của dung dịch đã dùng
a.\(n_{NaOH}=\dfrac{8}{40}=0,2mol\)
\(V_{dd}=\dfrac{120}{1,2}=100ml=0,1l\)
\(C_{M_{NaOH}}=\dfrac{0,2}{0,1}=2M\)
b.\(n_{NaOH}=\dfrac{21,6}{40}=0,54mol\)
\(V_{dd}=\dfrac{180}{1,2}=150ml=0,15l\)
\(C_{M_{NaOH}}=\dfrac{0,54}{0,15}=3,6M\)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn a gam P thu được chất rắn X hòa tan hoàn toàn X vào 500ml dung dịch nước ta được axit có nồng độ 24,5% Tính a(D=1g/ml)
4P + 5O2 = 2P2O5 (1)
P2O5 + 3H2O = 2H3PO4 (2)
ta có: mddH3PO4= v.D= 500.0,1= 50g
mH3PO4 = C%.mdd:100= 24,5%.50:100= 12,25g
nH3PO4= \(\dfrac{m}{M}\) = 12,25:98=0,125mol
thế vào ptr 2 tính được số mol P2O5=0,125.\(\dfrac{1}{2}\)=0,0625mol
thế số mol của P2O5 vào ptr 1 ta tính được số mol P=0,0625.4:2=0,125mol
mP= n.M= 0,125.31= 3,875g hay a= 3,875g
![]() nếu sai sửa dùm mình nhé
nếu sai sửa dùm mình nhé
Đúng 0
Bình luận (3)