| Tên thí nghiệm | Cách làm | Hiện tượng PTHH |
|
Điều chế H2 Thu khí H2 |
||
| CuO + H2 | ||
| Đốt cháy H2 | ||
| Hỗn hợp nổ |
nêu phương pháp và vẽ hình thí nghiệm điều chế H2 trong phòng thí ngiệm. Nêu các cách thu khí vào bình và giải thích, Viết PTHH phản ứng ?

Dựa vào tính chất H2 tan rất ít trong nước.
PTHH:
Fe + H2SO4 -> FeSO4 + H2
Fe + 2HCl -> FeCl2 + H2
Zn + H2SO4 -> ZnSO4 + H2
Zn + 2HCl -> ZnCl2 + H2
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
2Al + 6HCl -> 2AlCl3 + 3H2
Trong phòng thí nghiệm: để điều chế được CuO bằng cách khử Cu và khí H2 ở nhiệt độ cao
a) Viết phản ứng xảy ra
b) tính số gam Cu và khí H2 để điều chế được 80g CuO
Giúp em với mn ơi
Sửa đề
Trong phòng thí nghiệm: để điều chế được Cu bằng cách khử CuO bằng khí H2 ở nhiệt độ cao
a) Viết phản ứng xảy ra
b) tính số gam Cu và khí H2 để điều chế được 80g CuO
Giải
\(a)PTHH:CuO+H_2\xrightarrow[]{t^0}Cu+H_2O\\ b)n_{CuO}=\dfrac{80}{80}=1\left(mol\right)\\ CuO+H_2\underrightarrow{t^0}Cu+H_2O\\ n_{CuO}=n_{Cu}=n_{H_2}=1mol\\ m_{Cu}=1.64=64\left(g\right)\\ V_{H_2}=1.22,4=22,4\left(l\right)\)
Trong phòng thí nghiệm, khi điều chế khí H2, người ta thu H2 vào bình bằng cách đặt ngược(úp) bình, vì:
Nêu cách điều chế và thu khí H2 và O2 trong phòng thí nghiệm? Giải thích tại sao sử dụng cách thu đó
điều chế H2 từ pứ kim loại vs axit loại 1
thu cả ở đẩy nước, và úp bình (do H2 nhẹ hơn kk)
điều chế o2 từ phân hủy các chất giàu oxi
thu đc ở đâye nước và ngửa bình do (O2 nặng hơn kk)
2h2o -> 2h2 + o2
đk phản ứng nhiệt độ
Bằng pp đẩy kk và đẩy nước:
- Đẩy nước: vì H2 và O2 đều ít tan trong nước
- Đẩy kk:
+ O2: ngửa bình vì O2 nặng hơn kk
+ H2: úp ngược bình vì H2 là khí nhẹ nhất trong các khí hay nhẹ hơn kk
Câu 26: Trong phòng thí nghiệm, khi điều chế khí H2, người ta thu H2 vào bình bằng cách đặt úp bình, vì
A. khí H2 nhẹ hơn không khí.
B. khí H2 nặng hơn không khí.
C. khí H2 nặng gần bằng không khí.
D. khí H2 nhẹ hơn khí oxi.
Câu 27: Nhiệt độ và áp suất ở điều kiện thường của chất khí là
A. 00C, 20 atm. B. 00C, 1 atm.
C. 10C, 0 atm. D. 200C, 1 atm
26.A
27.D
#Fiona
Chúc bạn học tốt !
Tick đúng giúp mik vs ạ
Câu 12: Khi thu khí H2 vào ống nghiệm bằng cách đẩy không khí, ta úp ngược ống nghiệm vì khí H2:
A. Tan ít trong nước B. Nặng hợn không khí
C. Nhẹ hơn không khí D. Nhiệt độ hóa lỏng thấp
Câu 13: Để điều chế khí hiđro trong phòng thí nghiệm, người ta cho các kim loại Mg, Al, Zn, Fe tác dụng với dung dịch H2SO4 loãng. Nếu lấy cùng một khối lượng thì kim loại nào cho nhiều khí hiđro nhất?
A. Mg B. Al C. Zn D. Fe
Câu 14: Hòa tan hoàn toàn 10,2 gam hỗn hợp (Mg và Al) vào dung dịch H2SO4 loãng, thu được 8,96 lít khí hiđro (đktc). Khối lượng của Mg và Al lần lượt là:
A. 4,8 gam và 5,4 gam B. 8,4 gam và 4,5 gam
C. 5,8 gam và 4,4 gam D. 3,4 gam và 6,8 gam
Câu 15: Một học sinh tiến hành thí nghiệm điều chế khí hiđro bằng cách cho kim loại Fe tác dụng với dung dịch H2SO4 loãng, thu được 3,36 lít khí hiđro (đktc). Khối lượng của Fe cần dùng là bao nhiêu?
A. 8,4 gam B. 6,8 gam C. 9,2 gam D. 10,2 ga
Nêu nguyên liệu và cách điều chế khí H2 và O2 trong PHÒNG THÍ NGHIỆM
H2 : kim loại và axit
O2 : những chất giàu Oxi và dễ phân hủy : KClO3 , KMnO4 , ...
-Nguyên liệu điều chế khí o2 là: hợp chất giàu o2 và dễ phân hủy ở nhiệt độ cao
VD:KMnO4,KNO3...
-Nguyên liệu điều chế khí H2 là:HCl,H2SO4
Ba thí nghiệm được tiến hành với những khối lượng Zn bằng nhau và với 50 cm 3 dung dịch loãng H 2 SO 4 2M. PTHH của phản ứng :
Zn + H 2 SO 4 → Zn SO 4 + H 2
Bảng dưới đây cho biết các điều kiện của mỗi thí nghiệm :
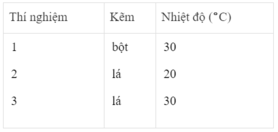
Khí hiđro thu được trong mỗi thí nghiệm được ghi lại theo những khoảng cách nhất định về thời gian cho đến khi phản ứng kết thúc, được biểu diễn bằng đồ thị sau :
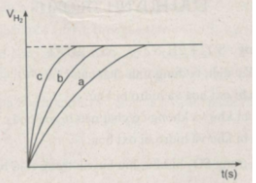
Rút ra được những nhận xét gì khi so sánh hiện tượng phản ứng của :
- Thí nghiệm 1 và thí nghiệm 3 ?
- Thí nghiệm 2 và thí nghiệm 3 ?
Nhận xét:
- Khí hiđro được giải phóng ở thí nghiệm 1 nhiều, nhanh hơn ở thí nghiệm 3. Vì diện tích tiếp xúc của Zn với H 2 SO 4 ở thí nghiệm 1 lớn hơn. trong khi đó nhiệt độ của dung dịch axit là như nhau.
- Khí hiđro được giải phóng ở thí nghiệm 3 nhiều, nhanh hơn ở thí nghiệm 2. Vì nhiệt độ của dung dịch H 2 SO 4 ở thí nghiệm 3 cao hơn, trong khi đó diện tích tiếp xúc giữa Zn và axit là như nhau.
2. (1,0 điểm) Trong phòng thí nghiệm, khí X được điều chế và thu vào bình tam giác như hình vẽ bên (Hình 1.1): a. Hình 1.1 mô tả cách thu khí X bằng phương pháp nào? b. Khí X có thể là khí nào trong các khí sau: H2, Cl2, O2, NH3, CH4, SO2, CO2, HCl, H2S, C2H4? Giải thích?
|
Trong phòng thí nghiệm ngươi ta điều chế khí H2 bằng cách cho kim loại
nhôm tác dụng với dung dịch axitClohidric (HCl) Sau phản ứng thu được muối nhôm cloru
(AlCl3) và 4 48 lít khí hidro điều kiện tiêu chuẩn
Hãy viết phương trình phản ứng xảy ra
b Tính hối lượng kim loại nhôm thu được sau phản ứng
c. Tính hối lượng muối thu được sau phản ứng .
(Biết H = 1, Cu = 64, O =16, Fe = 56, Cl = 35,5, Al = 27)
giúp mik với ạaa
2Al + 6HCL → 2AlCl3 + 3H2
b) nH2 = 4,48 : 22,4= 0,2 mol => nAl = nAlCl3 = 0,2 : 3 . 2 = \(\dfrac{2}{15}\) mol
mAl = \(\dfrac{2}{15}\).27=3.6 g
mAlCl3 = \(\dfrac{2}{15}\)(27+35,5.3) = 17,8 g
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
a, PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
_____2/15___________2/15____0,2 (mol)
b, \(m_{Al}=\dfrac{2}{15}.27=3,6\left(g\right)\)
c, \(m_{AlCl_3}=\dfrac{2}{15}.133,5=17,8\left(g\right)\)
Bạn tham khảo nhé!