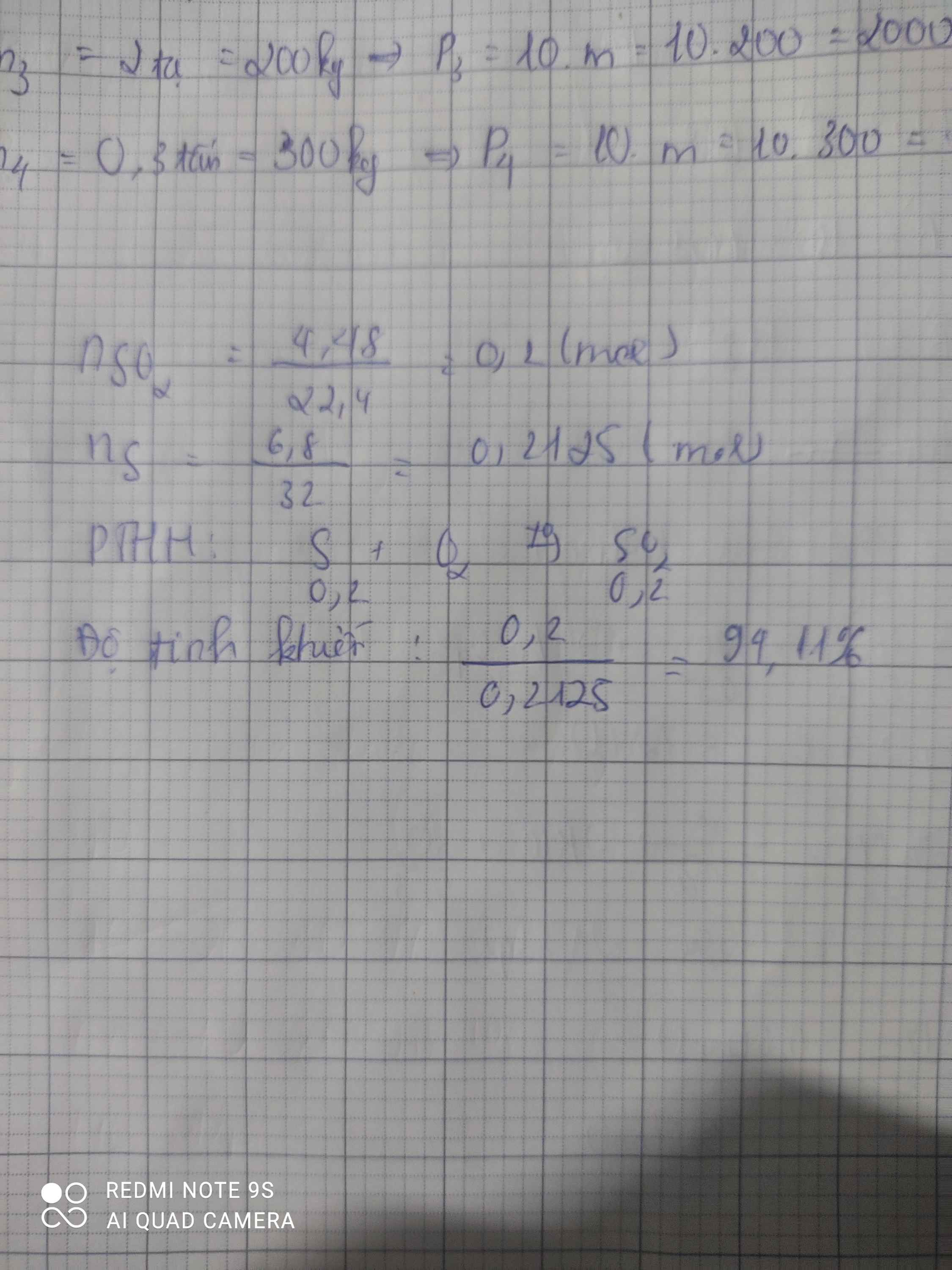Đốt cháy hoàn toàn 14,11g P chứa tạp chất trong oxi tinh khiết,thu đc 49,7g P2O5. xác định độ tinh khiết của mẫu phot-pho

Những câu hỏi liên quan
Đốt cháy hết 24,11g P có lẫn tạp chất trong oxi tinh khiết thu được 49,7g P205 .Xác định độ tinh khiết của P.
nP2O5 = \(\dfrac{49,7}{142}\)= 0.35 (mol)
4P + 5O2 -> 2 P2O5
4 : 5 : 2
0,7 < - 0,35 (mol)
mP = 0,7. 31 = 21,7 (g)
C%mP2O5 = \(\dfrac{21,7}{24,11}.100\%\)\(\approx\)90%
Đúng 0
Bình luận (0)
Ta có PTHH :
4P + 5O2 ---> 2P2O5
Theo đề bài ta có :
nP2O5 = 49,7 : 142 = 0,35(mol)
=> nP(PƯ) = 0,35 . 2 = 0,7(mol)
=> mP(PƯ) = 0,7 . 31 = 21,7(g)
=> H = 21,7 . 100% : 24,11 = 90%
Đúng 0
Bình luận (0)
đốt cháy 4g bột than (chứa C và tạp chất rắn trơ ko cháy ) thu đc 6,72 lít khí CO2 ở đktc.tính độ tinh khiết của than
\(PTHH:C+O_2\underrightarrow{t^o}CO_2\)
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Từ PTHH ta có
Đốt 1 mol C thì sinh ra 1 mol CO2
=> Đốt 0,3 mol C thì sinh ra 0,3 mol CO2
\(\Rightarrow m_C=0,3.12=3,6\left(g\right)\)
\(\Rightarrow\%C=\dfrac{3,6}{4}=90\%\)
Vậy độ tinh khiết của than là 90%
Đúng 1
Bình luận (0)
đốt cháy 6,8g 1 mẫu lưu huỳnh không tinh khiết trong khí O2 dư người ta thu được 4,48l khí SO2 ở đktc.Hãy xác định độ tinh khiết của mẫu s
\(n_{SO_2}=\dfrac{4.48}{22,4}=0,2\left(mol\right)\)
PTHH : S + O2 ---to---> SO2
0,2 0,2
\(m_S=0,2.32=6,4\left(g\right)\)
Độ tinh khiết của lưu huỳnh là
\(\dfrac{6,4}{6,8}.100\%=94,11\%\)
Đúng 1
Bình luận (0)
S+O2-to>SO2
0,2----------0,2
n SO2=\(\dfrac{4,48}{22,4}\)=0,2 mol
=>m S=0,2.32=6,4g
=>độ tinh khiết là \(\dfrac{6,4}{6,8}\).100=94,11%
Đúng 1
Bình luận (0)
Đốt cháy 15 gam một mẫu cacbon không tinh khiết trong khí oxi dư, thu được 17,92 lít khí CO2 (ở đktc). Độ tinh khiết của mẫu cacbon trên là:
Đọc tiếp
Đốt cháy 15 gam một mẫu cacbon không tinh khiết trong khí oxi dư, thu được 17,92 lít khí CO2 (ở đktc). Độ tinh khiết của mẫu cacbon trên là:
\(n_{CO_2}=\dfrac{17,92}{22,4}=0,8\left(mol\right)\)
PT: \(C+O_2\underrightarrow{t^o}CO_2\)
Theo PT: \(n_C=n_{CO_2}=0,8\left(mol\right)\)
\(\Rightarrow m_C=0,8.12=9,6\left(g\right)\)
Độ tinh khiết của mẫu C là: \(\dfrac{9,6}{15}.100\%=64\%\)
Đúng 2
Bình luận (0)
GIÚP MÌNH VỚI GẤP Ạ
đốt cháy hoàn toàn 3.4 gam một mẫu lưu huỳnh không tinh khiết trong khí oxi dư, thu được 2.24 lít ( đktc ) khí SO2. độ tinh khiết của mẫu lưu huỳnh là:
a. 97.12%
b.94.12%
c. 96.12%
d. 95.12%
\(n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: S + O2 --to--> SO2
0,1<--------------0,1
=> \(\%S=\dfrac{32.0,1}{3,4}.100\%=94,12\%\)
=> B
Đúng 2
Bình luận (0)
đốt cháy 21 gam 1 mẫu sắt không tinh khiết trong oxi dư người ta thu được 23,2 gam oxit sắt từ Fe3O4. tính độ tinh khiết của mẫu sắt đã dùng
PTHH: 3Fe + 2O2 → Fe3O4
Số mol của Fe3O4 là: 23,2 : 232 = 0,1 (mol)
Số mol của Fe là: 0,1 . 3 = 0,3 (mol)
Khối lượng Fe nguyên chất tham gia phản ứng là:
0,3 . 56 = 16,8 gam
% tinh khiết của mẩu sắt là: (16,8:21).100% = 80%
Đúng 0
Bình luận (1)
đốt cháy 21 gam 1 mẫu sắt không tinh khiết trong oxi dư người ta thu được 23,2 gam oxit sắt từ Fe3O4. tính độ tinh khiết của mẫu sắt đã dùng
giúp mình nhá
PTHH: 3Fe + 2O2 → Fe3O4
Số mol của Fe3O4 là: 23,2 : 232 = 0,1 (mol)
Số mol của Fe là: 0,1 . 3 = 0,3 (mol)
Khối lượng Fe nguyên chất tham gia phản ứng là:
0,3 . 56 = 16,8 gam
% tinh khiết của mẩu sắt là: (16,8:21).100% = 80%
Đúng 0
Bình luận (1)
Ta có PT:
3Fe + 2O2 ---> Fe3O4
n\(Fe_3O_4\)=\(\frac{23,2}{232}\)=0,1(mol)
Theo PT ta có:
nFe tinh khiết = 3n\(Fe_3O_4\)= 3.0,1=0,3(mol)
mFe tinh khiết = 0,3.56 = 16,8(g)
Độ tinh khiết của sắt đã dùng
= \(\frac{16,8}{21}\).100%=80%
Đốt cháy 3,25g một mẫu lưu huỳnh không tinh khiết trong không khí có oxi dư, người ta thu được 2,24 lit khí sunfuro(dktc). Bằng cách nào ta có thể tính được nồng độ tinh khiết của mẫu lưu huỳnh đã dùng?
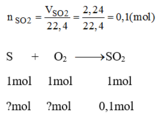
Theo pt: 1 mol S tham gia phản ứng sinh ra 1 mol S O 2
Số mol của lưu huỳnh tham gia phản ứng:
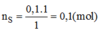
Khối lượng của lưu huỳnh tinh khiết: m S = n S . M S =0,1.32=3,2(g)
Độ tinh khiết của mẫu lưu huỳnh:
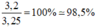
Đúng 0
Bình luận (0)
tính khối lượng oxi cần dùng để đốt cháy hoàn toàn
a) 1 tấn than chứa 95 phần trăm C. Các tạp chất còn lại không chyas
b) 4kg khí metan(CH4) tinh khiết
giúp mình với
A/Khoi luong C nguyen chat=1.(95/100)=0,95 tan
C + O2---->Co2
0,95 0,95
mO2=0,95 tan
B/ CH4 + 3/2 O2---> CO2 + 2H2O
0,25 mol 0,375
mO2=12g
m
Đúng 0
Bình luận (0)




 90 phần trăm
90 phần trăm