tính lượng quặng sắt có 69,6% fe304 để điều chế 12,6 tấn fe

Những câu hỏi liên quan
tính lượng quặng sắt có chứa 69,6% Fe3O4 để điều chế 12,6 tấn sắt
ai giúp e vs
12.6 tấn sắt = 12600 kg
MFe3O4 = 56*3 + 16*4= 232 (g/mol)
Trong 232 g Fe3O4 có 168 g Fe
x g Fe3O4 (= 12600 g Fe
mFe304 = x = 12600*232 : 168 = 17400 (kg)
KL quặng sắt chứa 69,6% Fe304 là
17400 * 100 : 69.6 = 25000 (kg)
Đúng 0
Bình luận (0)
Để điều chế 12,6 tấn sắt cần bao nhiêu tấn quặng sắt có chứa 69,6% Fe3O4. Bt hiệu suất của quá trình phản ứng là 98%
Mong chỉ giáo
https://i.imgur.com/SbXQHzb.jpg
1.Tính khối lượng sắt có trong :
a. 100 tấn quặng hemetit chứa 60% Fe2O3
b. 100 tấn quặng manhetit chứa 69,6 % Fe3O4
2. Cần trộn hai loại quặng trên theo tỉ lệ nào để từ 1 tấn quặng đã trộn người ta điều chế được 0,5 tấn gang( chứa 96% sắt và 4% cacbon )?
A là quặng chứa 60% Fe2O3 , B là quặng chứa 69,6% Fe3O4 ( các tạp chất còn lại trong A , B đều không chứa Fe ) . Người ta trộn quặng A và B thu được quặng D . Từ 1 tấn quặng D có thể điều chế được tối đa 0,48 tấn Fe . Tính tỉ lệ khối lượng quặng A và B đem trộn.
Đặt mA = a (tấn); mB = b (tấn)
Giả sử a + b = 1 (tấn) (1)
\(m_{Fe_2O_3\left(A\right)}=a.60\%=0,6a\left(tấn\right)=6.10^5a\left(g\right)\)
=> \(n_{Fe_2O_3\left(A\right)}=\dfrac{6.10^5a}{160}=3750a\left(mol\right)\Rightarrow n_{Fe\left(A\right)}=7500a\left(mol\right)\)
\(m_{Fe_3O_4\left(B\right)}=b.69,6\%=0,696b\left(tấn\right)=696.10^3b\left(g\right)\)
=> \(n_{Fe_3O_4\left(B\right)}=\dfrac{696.10^3b}{232}=3000b\left(mol\right)\Rightarrow n_{Fe\left(B\right)}=9000b\left(mol\right)\)
\(n_{Fe\left(tổng\right)}=\dfrac{0,48.10^6}{56}=\dfrac{60000}{7}\left(mol\right)\)
=> \(7500a+9000b=\dfrac{60000}{7}\) (2)
(1)(2) => \(a=\dfrac{2}{7}\left(tấn\right);b=\dfrac{5}{7}\left(tấn\right)\)
=> \(\dfrac{a}{b}=\dfrac{2}{5}\)
Đúng 2
Bình luận (0)
A là quặng chứa 60% Fe2O3 , B là quặng chứa 69,6% Fe3O4 ( các tạp chất còn lại trong A , B đều không chứa Fe ) . Người ta trộn quặng A và B thu được quặng D . Từ 1 tấn quặng D có thể điều chế được tối đa 0,48 tấn Fe . Tính tỉ lệ khối lượng quặng A và B đem trộn.
Đặt mA = a (tấn); mB = b (tấn)
Giả sử a + b = 1 (tấn) (1)
\(m_{Fe_2O_3\left(A\right)}=a.60\%=0,6a\left(tấn\right)=6.10^5a\left(g\right)\)
=> \(n_{Fe_2O_3\left(A\right)}=\dfrac{6.10^5a}{160}=3750a\left(mol\right)\Rightarrow n_{Fe\left(A\right)}=7500a\left(mol\right)\)
\(m_{Fe_3O_4\left(B\right)}=b.69,6\%=0,696b\left(tấn\right)=696.10^3b\left(g\right)\)
=> \(n_{Fe_3O_4\left(B\right)}=\dfrac{696.10^3b}{232}=3000b\left(mol\right)\Rightarrow n_{Fe\left(B\right)}=9000b\left(mol\right)\)
\(n_{Fe\left(tổng\right)}=\dfrac{0,48.10^6}{56}=\dfrac{60000}{7}\left(mol\right)\)
=> \(7500a+9000b=\dfrac{60000}{7}\) (2)
(1)(2) => \(a=\dfrac{2}{7}\left(tấn\right);b=\dfrac{5}{7}\left(tấn\right)\)
=> \(\dfrac{a}{b}=\dfrac{2}{5}\)
Đúng 0
Bình luận (0)
1. Tính khối lượng sắt có trong:
a. 100 tấn quăng hematit chứa 60% Fe2O3
b. 100 tấn quặng manhetit chứa 69,6% Fe3O4
2. Cần trộn 2 loại quặng trên theo tỉ lệ nào để từ 1 tấn quặng đã trộn người ta điều chế được 0,5 tấn gang( chứa 96% sắt và 4% cacbon)?
X là quặng hematit chứa 60% Fe2O3, Y là quặng manhetit chứa 69,6% Fe3O4.
a, Từ 1 tấn quặng X hoặc Y điều chế được tối đa bao nhiêu kg sắt kim loại?
b, Cần trộn X và Y theo tỉ lệ khối lượng là bao nhiêu để được quặng Z mà từ 1 tấn Z có thể điều chế được 05 tấn gang chứa 4% cacbon.
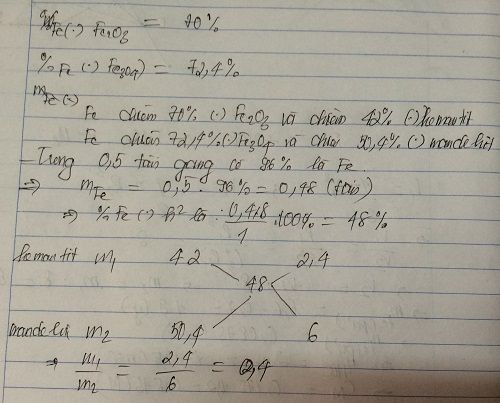
đề sai sai nha !
X là quặng hematit chứa 60% Fe2O3, Y là quặng manhetit chứa 69,6% Fe3O4. Cần trộn X, Y theo tỉ lệ khối lượng như thế nào để được quặng Z mà từ 1 tấn quặng Z có thể điều chế được 0,5 tấn gang chứa 96% sắt?OK!
Đúng 0
Bình luận (0)
Một quặng X chứa 64% Fe2O3 và quặng Y chứa 69,6% Fe3O4. Trộn a tấn quặng X với b tấn quặng Y thu được một loại quặng Z.Biết từ một tấn quặng Z có thể điều chế được 481,25kg gang chứa 4% cacbon( gang là hợp chất gồm Fe và C)
%Fe = 100% -4% = 96%
$m_{Fe} = 481,25.96% = 462(gam)$
$n_{Fe} = 462 : 56 = 8,25(kmol)$
Ta có : $a + b = 1(1)$
$m_{Fe_2O_3} = 1000a.64\% = 640a(kg)$
$\to n_{Fe_2O_3} = 640a : 160 = 4a(kmol)$
$m_{Fe_3O_4} = 1000b.69,6\% = 696b(kg)$
$\to n_{Fe_3O_4} = 696b : 232 = 3b(kmol)$
Bảo toàn nguyên tố với Fe :
$4a.2 + 3b.3 = 8,25(2)$
Từ (1)(2) suy ra a = 0,75(tấn) ; b = 0,25(tấn)
Đúng 3
Bình luận (0)
A là quặng chứa 60% Fe2O3 , B là quặng chứa 69,6% Fe3O4 ( các tạp chất còn lại trong A , B đều không chứa Fe ) . Người ta trộn quặng A và B thu được quặng D . Từ 1 tấn quặng D có thể điều chế được tối đa 0,48 tấn Fe . Tính tỉ lệ khối lượng quặng A và B đem trộn.
- Gọi khối lượng quặng ở quặng A và B đem trộn lần lượt là x, y (x, y>0)
=> Tỉ lệ khối lượng cần tìm là : \(\frac{x}{y}\) .
\(m_{Fe_2O_3}=60\%x=0,6x\)
=> \(n_{Fe_2O_3}=\frac{m}{M}=\frac{0,6x}{160}\left(mol\right)\)
=> \(n_{\left(Fe\right)}=2n_{Fe_2O_3}=\frac{3x}{400}\left(mol\right)\)
\(m_{Fe_3O_4}=69,6\%y=0,696y\)
=> \(n_{Fe_3O_4}=\frac{m}{M}=\frac{0,696y}{232}\left(mol\right)\)
=> \(n_{\left(Fe\right)}=3n_{Fe_3O_4}=\frac{9y}{1000}\left(mol\right)\)
-> \(n_{\left(Fe\right)}=n_{\left(Fe\right)}+n_{\left(Fe\right)}=n_{Fe}=\frac{3x}{400}+\frac{9y}{1000}\left(mol\right)\)
Mà \(n_{Fe}=\frac{m}{M}=\frac{0,48}{56}\left(mol\right)\)
=> \(\frac{3x}{400}+\frac{9y}{1000}=\frac{0,48}{56}\)( I )
Ta có : 1 tấn quặng D .
=> \(m_D=m_{Fe_2O_3}+m_{Fe_3O_4}=0,6x+0,696y=1\left(II\right)\)
- Giải hệ phương trình từ ( I ) và ( II ) ta được :
\(\left\{{}\begin{matrix}x=\frac{118}{7}\\y=-\frac{275}{21}\end{matrix}\right.\) ( ***** )
Vậy ..... bạn xem lại đề nha ( KHÔNG CHẮC MÌNH ĐÚNG THAM KHẢO )
Đúng 0
Bình luận (0)



















