Giúp mk vs
Nguyên tố Y có tổng các loại hạt là 21
Xác định số E, P, N, A của Y.
Nguyên tử của một nguyên tố có tổng số các loại hạt là 34 trong đó số hạt không mạng điện là 12.Xác định số p,số n,số e của nguyên tử nguyên tố đó
Giúp e với
Ta có:
\(\left\{{}\begin{matrix}p+e+n=34\\n=12\end{matrix}\right.\)
mà \(p=e\) (trung hòa về điện)
\(\Rightarrow2p+n=34\\ \Rightarrow2p+12=34\\ \Rightarrow p=e=11\)
Ta có: \(p+e+n=34\) Mà số p = số e
\(\Rightarrow\) \(2p+n=34\left(1\right)\)
Ta lại có: \(2p-n=12\left(2\right)\)
Từ ( 1 ) và ( 2 ) ta có hệ phương trình sau:
\(\left\{{}\begin{matrix}2p+n=34\\2p-n=12\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p=12,e=12\\n=11\end{matrix}\right.\)
( 12 là xấp xỉ làm tròn của 11,5 nha )
Trong nguyên tử một nguyên tố A có tổng số các loại hạt là 58. Biết số hạt p ít hơn số hạt n là 1 hạt. Xác định số hạt P,N,E ? . giúp mình với các bạn
a) nguyên tử X có tổng số 3 loại hạt p,n và e bằng 52 hạt trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt
b) một nguyên tử của nguyên tố Y có tổng số hạt là 28 (p,n và e) và số hạt không mang điện chiếm xấp xỉ 35,7%
hãy xác định số p,n và e và vẽ sơ đồ đơn giản của nguyên tử X,Y
a. Nguyên tử X:
\(\left\{{}\begin{matrix}2P+N=52\\2P-N=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=17=E=Z\\N=18\end{matrix}\right.\)
Sơ đồ đơn giản:
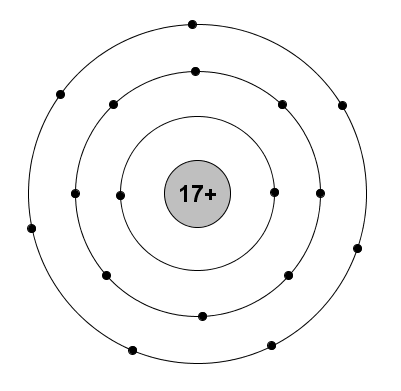
b. * Nguyên tử Y:
\(\left\{{}\begin{matrix}2P+N=28\\N\approx35,7\%.28=10\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=E=Z=9\\N=10\end{matrix}\right.\)
Sơ đồ cấu tạo nguyên tử Y:
Em tham khảo nha!
a.
Gọi: pX , eX , nX là các hạt trong X.
Khi đó :
\(2p_X+n_X=52\)
\(2p_X-n_X=16\)
\(\Rightarrow p_X=17,n_X=18\)

b.
Gọi: pY , eY , nY là các hạt trong Y.
Khi đó :
\(2p_Y+n_Y=28\)
\(n_Y=35.7\%\cdot28=10\) \(\Rightarrow p_Y=9\)
Nguyên tử của nguyên tố A có số tổng các loại hạt nguyên tử là 58. Trong đó số hạt mang điện nhiều hơn hạt không mang điện 18 hạt .xác định e , p, n
tổng các loại hạt nguyên tử là 58 nên ta có:
2p+n=58 (1)
mà hạt mang điện nhiều hơn hạt ko mang điện là 18 =>
2p-n=18 (2)
từ (1,2) => ta có hệ pt
=> p=e=19
n=20
Nguyên tử nguyên tố Y có tổng số các loại hạt là 34. Xác định nguyên tố Y
trong một nguyên tố
số proton p luôn = số electron
ta có
n + p + e = 34
p = e => n + 2p = 34
mặt khác
p < n < 1,3p ( đây là tỉ lệ có sẵn ko phải cm)
<=> n = 12 , p = e = 11
để tìm nguyên tố X bạn cần tìm số khối A = Z + N = p + n = 23
nguyên tố X là Na ( natri - 23)
gọi số hạt electron của nguyên tử là ''e''
gọi số hạt proton của nguyên tử là ''p''
gọi số hạt nơtron ủa nguyên tử là ''n''
\(\rightarrow\) p+e+n=34
\(\Leftrightarrow\) 2p+n=34(vì số p=số e)
\(\Rightarrow\) n=34-2p
mà 1\(\le\) \(\frac{n}{p}\) \(\le\) 1,5
\(\Rightarrow\) \(1\le\frac{34-2p}{p}\le1,5\)
\(\Leftrightarrow\) \(\begin{cases}34-2p\ge1p\\34-2p\le1,5p\end{cases}\)
\(\Leftrightarrow\begin{cases}34\ge3p\\34\le3,5p\end{cases}\) \(\Leftrightarrow\begin{cases}p\le11,3\\p\ge9,7\end{cases}\)
nếu p=11,e=11\(\Rightarrow\) n=12
vậy Y là cacbon(C)
chúc bạn học tốt (like mình nha)![]()
nguyên tử của một nguyên tố có tổng số các loại hạt là 28, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 8. Xác định số p, số n, số e của nguyên tử nguyên tố đó. Vẽ mô hình nguyên tử. Xác định vị trí của nguyên tố đó trong bảng tuần hoàn.
Tổng số các loại hạt là 28, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 8
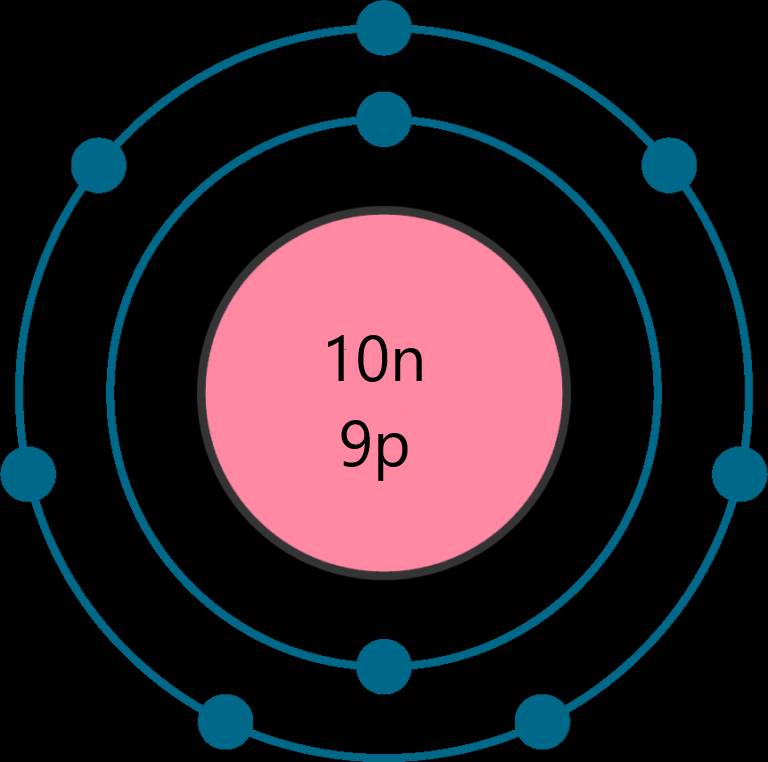
⇒ Số neutron là 10 hạt
Số proton là 9 hạt
Số electron là 9 hạt
⇒ Nguyên tố Fluorine - ô số 9, chu kì 2, nhóm VIIA trong bảng tuần hoàn
Cho mk hỏi bài này của hóa 8 nha mấy bn
1) Nguyên tử X có tổng số hạt là 49. Số hạt không mang điện bằng 53,125% số hạt mang điện. Tính số hạt mỗi loại và xác định nguyên tử X.
2) Nguyên tử Y có tổng số hạt là 36. Số hạt ko mang điện thì bằng 1 nửa hiệu số giữa tổng số hạt với số hạt mang điện tích âm. Tính số hạt mỗi loại và xác định tên nguyên tố Y.
Mình cần gấp lắm ạ. Ai giải đc giúp mình với ạ
nguyên tử y có tổng số các loại hạt là 36 số hạt ko mang điện bàng 1 nửa hiệu số giữa tổng số hạt mang điện âm xác định tên của nguyên tố y
gọi số hạt proton,electron, notron lần lượt là p,e,n
do p=e=>p+e=2p
ta có hpt: \(\begin{cases}2p+n=36\\n=\frac{1}{2}\left(36-p\right)\end{cases}\)
<=>\(\begin{cases}p=12\\n=12\end{cases}\)
=> p=12=> Y là Mg
1:Tổng số hạt cơ bản của nguyên tử nguyên tố X là 36.Trong đó số hạt mang điện gấp đôi số hạt không mang điện.Xác định số hiệu nguyên tử và số khối của nguyên tử X?
2:Tổng số hạt trong nguyên tử là Y là 54 hạt,trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 14.
a)Xác định các loại hạt trong Y b)Xác định đơn vị điện tích hạt nhân của Y c)Viết kí hiệu nguyên tử Y
3:Nguyên tử R có tổng số hạt là 115.Số hạt mang điện nhiều hơn số hạt không mang điện là 25.Xác định nguyên tử R từ đó suy ra STT của R?
-Mình cần rất gấp,các bạn giúp mình với!-
1. Ta có tổng số hạt cơ bản của nguyên tố X là 36 , suy ra
p + e + n = 36 => 2p + n = 36
Số hạt mang điện gấp đôi số hạt không mang điện : 2p = 2n => p = n
Vậy : 3p = 36 => p = 12 => số p = số e = số z = 12
Số khối : A = p + n = 12 + 12 = 24
2.
a, Ta có tổng số hạt cơ bản là 54 hạt.
=> p+e+n=54 => 2p+n=54(1)
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 14
=> 2p-n=14(2)
Từ (1) và (2) ta có hệ pt:
2p-n=14
2p+n=54
<=> p=17
n=20
Vậy e=17, p=17, n=20
b, số hiệu nguyên tử Z=17
c, kí hiệu: Cl
3.
Ntử R có tổng số hạt cơ bản là 115
=> p+e+n=115
=>2p+n=115(1)
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 25
=> 2p-n=25(2)
Từ (1)&(2) => ta có hệ phương trình
=>2p+n=115
2p-n=25
<=>p=35
n=45
=> e=35, p=35, n=45
=> R là Br
STT của Br là 35