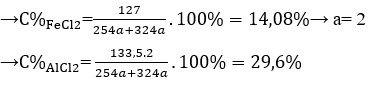1) cho 13,4 g hỗn hợp X gồm:Mg,Fe,Al phản ứng vừa đủ với dung dịch có chứa 36,5 g HCL,mgam hỗn hợp với muối.Y gồm :Alcl3 ,Mgcl2 ,Fecl2 .Tính m

Những câu hỏi liên quan
cho 13,4 g hỗn hợp X gồm Mg,Al,Fe phản ứng vừa đủ với dung dịch có chứa 36,5 g HCl thu được \(m_{_{ }g}\) hỗn hợp muối Y gồm \(AlCl_3\),\(MgCl_2\),\(FeCl_{_{ }3}\). tính M
n HCl = \(\dfrac{m}{M}=\dfrac{36,5}{36,5}=1\left(mol\right)\)
=> n Cl- = n HCl = 1 mol
=> m Cl- = 1*35,5 = 35,5 (g)
m Muối = m hỗn hợp + m Cl- = 13,4 +35,5 =48,9(g)
pthh:
Mg + 2 HCl ---> MgCl2 + H2
2Al + 6HCl ----> 2AlCl3 + 3H2
Fe + HCl ---> FeCl2 + H2
Đúng 0
Bình luận (0)
Cho 22,2 gam hỗn hợp X gồm Fe, Al, Zn tác dụng vừa đủ với dung dịch có chứa 38,325 gam HCl, thu được m gam hỗn hợp muối A l C l 3 , F e C l 2 , Z n C l 2 và 1,05 gam khí hidro. Tính khối lượng muối thu được.
Cho 13,5 gam hỗn hợp X gồm Mg, Al,Fe, Zn tác dụng với một lượng dung dịch chứa HCl (dư) được V(l) khí H2(đktc) và 66,75 (g) hỗn hợp Y gồm MgCl2, AlCl3, FeCl2, ZnCl2. a) Viết PTHH xảy ra? b) Tìm V?
Xem chi tiết
a)
\(Mg + 2HCl \to MgCl_2 + H_2\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ Zn + 2HCl \to ZnCl_2 + H_2\)
b)
Gọi : \(n_{H_2} = a(mol) \Rightarrow n_{HCl} = 2a\)
Bảo toàn khối lượng :
\(13,5 + 2a.36,5 = 66,75 + 2.a\\ \Rightarrow a = 0,75\\ \Rightarrow V = 0,75.22,4 = 16,8(lít)\)
Đúng 2
Bình luận (0)
a) Mg + 2 HCl -> MgCl2 + H2
2Al + 6 HCl -> 2 AlCl3 + 3 H2
Fe + 2 HCl -> FeCl2 + H2
Zn + 2 HCl -> ZnCl2 + H2
b) mY-mX=mCl
<=> mCl= 66,75-13,5=53,25(g)
=>nCl=53,25/35,5=1,5(mol)
=> nH2= nCl/2= 1,5/2=0,75(mol)
=>V=V(H2,đktc)=0,75.22,4=16,8(l)
Đúng 2
Bình luận (0)
Hoà tan m gam hỗn hợp X gồm Fe, Magie, Kẽm bằng một lượng vừa đủ dung dịch chứa 25,55 g HCl thu được dung dịch chứa 42,6 g hỗn hợp muối gồm FeCl2, MgCl2, ZnCl2 và 0,7 g H2.
a, Viết PTHH
b, Tính giá trị của m
a. PTHH:
Fe + 2HCl \(\rightarrow\)FeCl2 + H2
Mg + 2HCl \(\rightarrow\) MgCl2 + H2
Zn + 2HCl \(\rightarrow\)ZnCl2 + H2
b.
Áp dụng định luật bảo toàn khổi lượng ta có:
mA + mB = mC + mD
m = mC + mD - mB
m = 42,6 + 0,7 - 25,55
m = 17,75
Vậy khối lượng của X bằng 17,75 g
Đúng 0
Bình luận (0)
Cho 16.6 (g) hỗn hợp gồm al,fe tác dụng vừa đủ với dung dịch HCl 40% . Sau phản ứng thấy khối lượng dung dịch tăng thêm 15.6 (g) A) pthh B) tính khối lượng mỗi kim loại trg hỗn hợp C) tính C% của chất có trg dung dịch sau phản ứng
a, \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
b, Ta có: m dd tăng = mKL - mH2
⇒ mH2 = 16,6 - 15,6 = 1 (g) \(\Rightarrow n_{H_2}=\dfrac{1}{2}=0,5\left(mol\right)\)
Có: 27nAl + 56nFe = 16,6 (1)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=0,5\left(2\right)\)
Từ (1) và (2) ⇒ nAl = nFe = 0,2 (mol)
\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,2.27=5,4\left(g\right)\\m_{Fe}=0,2.56=11,2\left(g\right)\end{matrix}\right.\)
c, Theo PT: \(n_{HCl}=2n_{H_2}=1\left(mol\right)\Rightarrow m_{ddHCl}=\dfrac{1.36,5}{40\%}=91,25\left(g\right)\)
⇒ m dd sau pư = 91,25 + 15,6 = 106,85 (g)
Theo PT: \(\left\{{}\begin{matrix}n_{AlCl_3}=n_{Al}=0,2\left(mol\right)\\n_{FeCl_2}=n_{Fe}=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{AlCl_3}=\dfrac{0,2.133,5}{106,85}.100\%\approx24,98\%\\C\%_{FeCl_2}=\dfrac{0,2.127}{106,85}.100\%\approx23,77\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
\(2Al+6HCl->2AlCl_3+3H_2\\ Fe+2HCl->FeCl_2+H_2\\ n_{H_2}=\dfrac{16,6-15,6}{2}=0,5mol\\ n_{HCl}=1mol\\ n_{Al}=a;n_{Fe}=b\\ 27a+56b=16,6\\ 3a+2b=1\\ a=b=0,2\\ m_{Al}=0,2.27=5,4g\\ m_{Fe}=0,2.56=11,2g\\ m_{ddsau}=15,6+\dfrac{36,5}{0,4}=106,85g\\ C\%_{AlCl_3}=\dfrac{133,5.0,2}{106,85}.100\%=24,99\%\\ C\%_{FeCl_2}=\dfrac{127.0,2}{106,85}.100\%=23,77\%\)
Đúng 1
Bình luận (0)
Hoà tan hoàn toàn hỗn hợp X gồm Fe và Al bằng một lượng vừa đủ dung dịch HCl 36,5%, thu được dung dịch Y. Nồng độ của
F
e
C
l
2
trong dung dịch Y là 14,08%. Nồng độ phần trăm của
A
l
C
l
3
trong dung dịch Y là A. 29,6% B. 15,76% C. 30,2%. D. 11,4%
Đọc tiếp
Hoà tan hoàn toàn hỗn hợp X gồm Fe và Al bằng một lượng vừa đủ dung dịch HCl 36,5%, thu được dung dịch Y. Nồng độ của F e C l 2 trong dung dịch Y là 14,08%. Nồng độ phần trăm của A l C l 3 trong dung dịch Y là
A. 29,6%
B. 15,76%
C. 30,2%.
D. 11,4%
Cho 8,3 g hỗn hợp gồm Al và Fe phản ứng vừa đủ với 500 gam dung dịch HCl a% sau phản ứng thu được dung dịch chứa m gam muối và có 5,6 lít khí H2 thoát ra(dktc). Tính khối lượng mỗi kim loại, tính a và C% của các chất tan trong dung dịch sau phản ứng
Em đăng sang môn Hoá nha
Đúng 0
Bình luận (0)
Cho 8,3 g hỗn hợp gồm Al và Fe phản ứng vừa đủ với 500 gam dung dịch HCl a% sau phản ứng thu được dung dịch chứa m gam muối và có 5,6 lít khí H2 thoát ra(dktc). Tính khối lượng mỗi kim loại, tính a và C% của các chất tan trong dung dịch sau phản ứng
\(2Al+6HCl->2AlCl_3+3H_2\\ Fe+2HCl->FeCl_2+H_2\\ n_{Al}=a;n_{Fe}=b\\ 27a+56b=8,3\\ 1,5a+b=\dfrac{5,6}{22,4}=0,25\\ a=b=0,1\\ m_{Al}=27\cdot0,1=2,7g\\ m_{Fe}=8,3-2,7=5,6g\\ a=\dfrac{3a+2b}{500}\cdot36,5=3,65\%\\ m_{ddsau}=508,3-0,25\cdot2=507,8g\\ C\%_{AlCl_3}=\dfrac{133,5a}{507,8}=2,63\%\\ C\%_{FeCl_2}=\dfrac{127b}{507,8}=2,50\%\)
Đúng 1
Bình luận (0)
Cho 29,6g hỗn hợp Al ; Fe và Zn tác dụng vừa đủ với dung dịch HCl ở chúa 51,1 g HCL , thu được 14,2g H2 va hoa hop muoi Alcl3 ; fecl2 ; Zncl2 .
â, Viết sơ đồ phản ứng ?
b, Tính khối lượng hòa hợp muối thu được ?
a)\(X\left\{{}\begin{matrix}Al\\Fe\\Zn\end{matrix}\right.+HCl\rightarrow\left\{{}\begin{matrix}AlCl_3\\FeCl_2\\ZnCl_2\end{matrix}\right.+H_2}}\)
b)\(n_{H_2}=0,7\left(mol\right)\\ n_{H\left(H_2\right)}=n_{HCl\left(pu\right)}=n_{Cl\left(HClpu\right)}=1,4\left(mol\right)\\ m_{hh}=m_{KL}+m_{Cl}=29,6+35,5\cdot1,4=79,3\left(g\right)\)
Đúng 0
Bình luận (1)