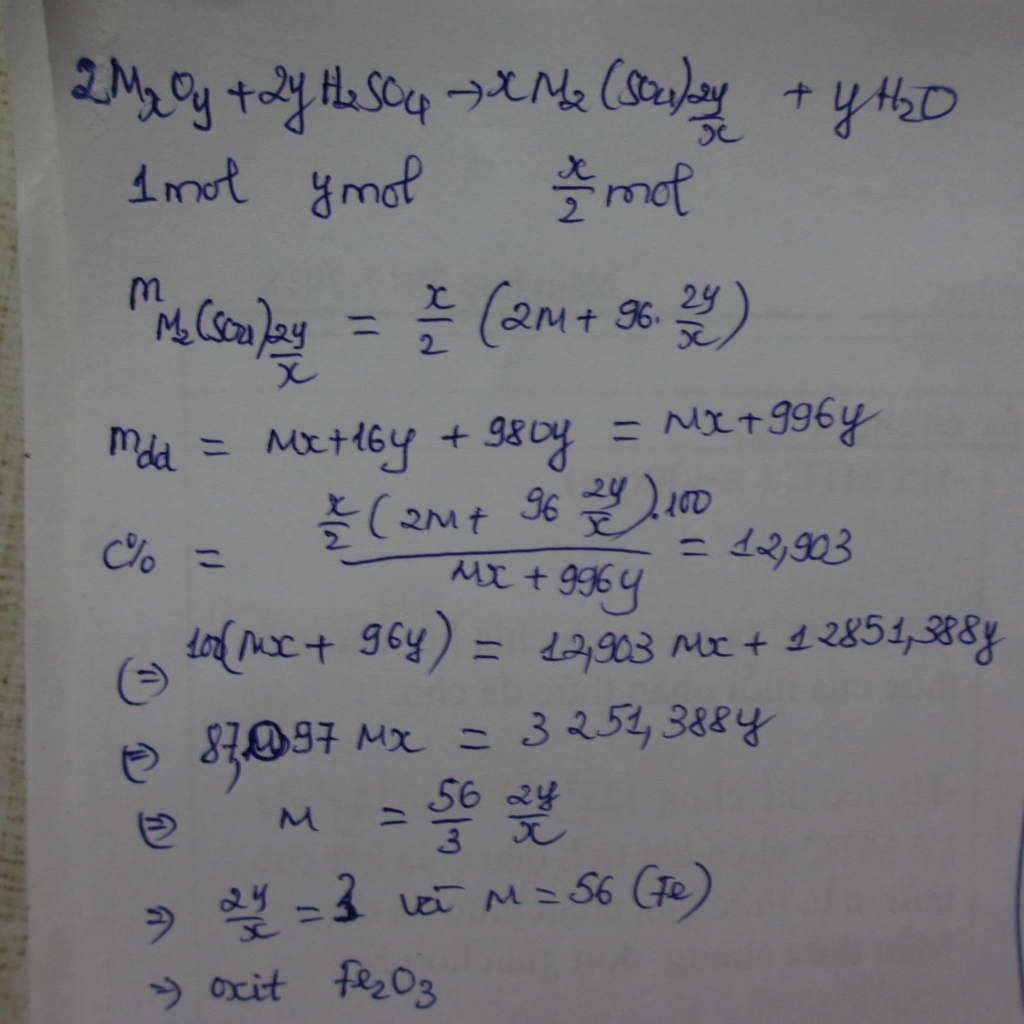44. người ta cho 24g so3 tan hết trong dd h2so4 loãng vừa đủ rồi cho dd sau phản ứng bay hơi hết với áp suất thấp thu được 84,3 g muối ngậm nước xác định công thức của muối này

Những câu hỏi liên quan
Cho 24g Fe2O3 tan hết trong dung dịch H2SO4 loãng vừa đủ rồi cho dung dịch sau phản ứng bay hơi hết dưới áp suất thấp thì thu được 84g muối ngậm nước. Xác định công thức muối.
\(n_{Fe_2O_3}=\dfrac{24}{160}=0,15\left(mol\right)\)
Gọi công thức muối ngậm nước là \(Fe_2\left(SO_4\right)_3.nH_2O\)
Bảo toàn nguyên tố Fe ta có
\(n_{Fe\left(Fe_2O_3\right)}=n_{Fe\left(Fe_2\left(SO_4\right)_3.nH_2O\right)}=0,15\cdot2=0,3\)\
\(m_{Fe_2\left(SO_4\right)_3.nH_2O}=\left(400+18n\right)\cdot0,15=84\\\Rightarrow n\approx9 \)
Suy ra công thức tinh thể là \(Fe_2\left(SO_4\right)_3.9H_2O\)
Đúng 0
Bình luận (0)
Hòa tan 10,8 g Mg vào dd H2SO4 20 % vừa đủ , sau khi phản ứng kết thúc thu được dd X . Làm lạnh dd X xuống 20 độ C thu được 14,76 g muối sunfat kết tinh ngậm nước tách ra và còn lại dd muối bão hòa có nồng độ 21,703 % . Xác định CT muối sunfat ngậm nước .
\(n_{Mg}=\dfrac{10,8}{24}=0,45\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
0,45-->0,45------>0,45--->0,45
=> \(m_{H_2SO_4}=0,45.98=44,1\left(g\right)\)
=> \(m_{ddH_2SO_4}=\dfrac{44,1.100}{20}=220,5\left(g\right)\)
mdd (20oC) = 10,8 + 220,5 - 0,45.2 - 14,76 = 215,64 (g)
\(m_{MgSO_4\left(dd.ở.20^oC\right)}=\dfrac{215,64.21,703}{100}=46,8\left(g\right)\)
=> nMgSO4 (tách ra) = \(0,45-\dfrac{46,8}{120}=0,06\left(mol\right)\)
=> nH2O (tách ra) = \(\dfrac{14,76-0,06.120}{18}=0,42\left(mol\right)\)
Xét nMgSO4 (tách ra) : nH2O (tách ra) = 0,06 : 0,42 = 1 : 7
=> CTHH: MgSO4.7H2O
Đúng 5
Bình luận (0)
Bài 1 Hòa tan 3,2 gam oxit M2Om trong một lượng vừa đủ dd H2SO4 10% thu được dd muối Sunfat 12,9%. Cô cạn dd muối rồi l làm lạnh dd thấy thoát ra 7,868 gam tinh muối sunfat với hiệu suất muối kết tinh là 70%. Hãy xác định công thức của tinh thể ngậm nước
đốt cháy hoàn toàn 12g muối sunfua kim loại R(R có hóa trị II không đổi ) thu được chất rắn A và khí B. hòa tan A bằng 1 lượng vừa đủ dd h2so4 14,5% thu được dd muối có nồng độ 33.33% . khi làm lạnh dd muối xuống nhiệt độ thấp hơn thì có 1 lượng tinh thể muối ngậm nước tách ra có khối lượng là 15,625 g. phần dd bảo hòa có nồng độ là 22,54% . xác định R và công thức của muối ngậm nước nói trên
Đọc tiếp
đốt cháy hoàn toàn 12g muối sunfua kim loại R(R có hóa trị II không đổi ) thu được chất rắn A và khí B. hòa tan A bằng 1 lượng vừa đủ dd h2so4 14,5% thu được dd muối có nồng độ 33.33% . khi làm lạnh dd muối xuống nhiệt độ thấp hơn thì có 1 lượng tinh thể muối ngậm nước tách ra có khối lượng là 15,625 g. phần dd bảo hòa có nồng độ là 22,54% . xác định R và công thức của muối ngậm nước nói trên
Hòa tan 2.8 g Fe trong dung dịch H2SO4 loãng vừa đủ rồi cho dung dịch sau phan ứng bay hơi hết dưới áp suất thu được 13.9 g muối ngâm nước . Xác định công thức muối ngậm nước.
giải cho mình với chiều ni mình thi loại rồi, mình sắp đi học rồi giải khẩn trương lên nếu ai làm được thì mình sẽ tích cho các nhiều.....
\(n_{Fe}=0,05\left(mol\right)\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Từ PTHH suy ra nFe=nFeSO4=0,05(mol)
Gọi CT tinh thể là FeSO4.nH2O
Co nFeSO4=nFeSO4.nH2O=> \(M_{FeSO_4.nH_2O}=\dfrac{13,9}{0,05}=152+18n=278\Rightarrow n=7\\ \Rightarrow\)
CT tinh thể là FeSO4.7H20
Đúng 1
Bình luận (0)
Vì bay hơi hết nước mới có tinh thể nên số mol muối bằng số mol tinh thể
Đúng 1
Bình luận (0)
Cho 8g một oxit kim loại hóa trị 2 tan hết trong 200g dd HCl ( vừa đủ và chưa rõ nồng độ). Cô cạn dd sau phản ứng thu được 19g muối a) xác định công thức oxit b) tính nồng độ % của dd HCl cần dùng
Xđ % khối lượng các chất có trong hh đầu ở các trường hợp sau:a. Cho H2SO4 loãng dư vào hh kẽm và magie cacbonat .Sau phản ứng thu 4,48 lít khí và cô cạn dd thu 28.1gam muối khanb.hh gồm Al2O3 , Na tan hết vào dd H2SO4 loãng vừa đủ tạo 7,26 g muối và giải phóng 336ml khí c.hh gồm Fe,Fe2O3 tan hết vào 92,2ml dd H2SO4 đặt,to, đủ thu đc dd chứa 100g muối .Khi cho dd thu đc tác dụng với dd Ba(OH)2 đủ cô cạn dd sau phản ứng đc a gam chất rắn B.Nung B đến khối lượng ko đổi đc x gam chất rắn C,tính a,...
Đọc tiếp
Xđ % khối lượng các chất có trong hh đầu ở các trường hợp sau:
a. Cho H2SO4 loãng dư vào hh kẽm và magie cacbonat .Sau phản ứng thu 4,48 lít khí và cô cạn dd thu 28.1gam muối khan
b.hh gồm Al2O3 , Na tan hết vào dd H2SO4 loãng vừa đủ tạo 7,26 g muối và giải phóng 336ml khí
c.hh gồm Fe,Fe2O3 tan hết vào 92,2ml dd H2SO4 đặt,to, đủ thu đc dd chứa 100g muối .Khi cho dd thu đc tác dụng với dd Ba(OH)2 đủ cô cạn dd sau phản ứng đc a gam chất rắn B.Nung B đến khối lượng ko đổi đc x gam chất rắn C,tính a,x?
a, Gọi \(\left\{{}\begin{matrix}n_{Zn}=a\left(mol\right)\\n_{MgCO_3}=b\left(mol\right)\end{matrix}\right.\)
\(n_{hhkhí\left(H_2,CO_2\right)}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
Zn + H2SO4 ---> ZnSO4 + H2
a a a
MgCO3 + H2SO4 ---> MgSO4 + CO2 + H2O
b b b
Hệ pt \(\left\{{}\begin{matrix}a+b=0,2\\161a+84b=28,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,1\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Zn}=0,1.65=6,5\left(g\right)\\m_{MgCO_3}=0,1.84-8,4\left(g\right)\end{matrix}\right.\\ \rightarrow\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{6,5}{6,5+8,4}=43,62\%\\\%m_{MgCO_3}=100\%-43,62\%=56,38\%\end{matrix}\right.\)
b, \(n_{H_2}=\dfrac{0,336}{22,4}=0,015\left(mol\right)\)
PTHH:
2Na + H2SO4 ---> Na2SO4 + H2
0,03 0,015 0,015
\(\rightarrow m_{Al_2\left(SO_4\right)_3}=7,26-0,015.142=5,13\left(g\right)\\ \rightarrow n_{Al_2\left(SO_4\right)_3}=\dfrac{5,13}{342}=0,015\left(mol\right)\)
Al2O3 + 3H2SO4 ---> Al2(SO4)3 + 3H2O
0,015 0,015
\(\rightarrow\left\{{}\begin{matrix}m_{Na}=0,03.23=0,69\left(g\right)\\m_{Al_2O_3}=0,015.102=1,53\left(g\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Na}=\dfrac{0,69}{0,69+1,53}=31,08\%\\\%m_{Al_2O_3}=100\%-31,08\%=68,92\%\end{matrix}\right.\)
c, Thiếu \(d_{H_2SO_4}\)
Đúng 1
Bình luận (0)
Hòa tan 4,8 g 1 oxit kim loại bằng dd H2SO4 10% vừa đủ, thu đc dd Muối có nồng độ 12,9%. Sau phản ứng, hạ nhiệt độ dd ấy có 13,488g muối P kết tinh với hiệu suất 80%. Xác định CT muối P
Gọi CTHH của oxit KL là A2On.
PT: \(A_2O_n+nH_2SO_4\rightarrow A_2\left(SO_4\right)_n+nH_2O\)
Ta có: \(n_{A_2O_n}=\dfrac{4,8}{2M_A+16n}\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n.n_{A_2O_n}=\dfrac{4,8n}{2M_A+16n}\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=\dfrac{4,8n}{2M_A+16n}.98=\dfrac{470,4n}{2M_A+16n}\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{\dfrac{470,4n}{2M_A+16n}}{10\%}=\dfrac{4704n}{2M_A+16}\left(g\right)\)
⇒ m dd sau pư = \(4,8+\dfrac{4704n}{2M_A+16}\left(g\right)\)
Theo PT: \(n_{A_2\left(SO_4\right)_n}=n_{A_2O_n}=\dfrac{4,8}{2M_A+16n}\left(mol\right)\)
\(\Rightarrow C\%_{A_2\left(SO_4\right)_n}=\dfrac{\dfrac{4,8.\left(2M_A+96n\right)}{2M_A+16}}{4,8+\dfrac{4704n}{2M_A+16n}}.100\%=12,9\%\)
\(\Rightarrow M_A\approx18,65m\)
Với m = 3, MA = 56 (g/mol) là thỏa mãn.
→ A là Fe.
Ta có: \(n_{Fe_2O_3}=\dfrac{4,8}{160}=0,03\left(mol\right)\)
Theo PT: \(n_{Fe_2\left(SO_4\right)_3}=n_{Fe_2O_3}=0,03\left(mol\right)\)
Gọi CTHH của muối P là Fe2(SO4)3.nH2O.
Có: H = 80% ⇒ nP = 0,03.80% = 0,024 (mol)
\(\Rightarrow M_P=\dfrac{13,488}{0,024}=562\left(g/mol\right)\)
\(\Rightarrow400+18n=562\Rightarrow n=9\)
Vậy: CTHH của P là Fe2(SO4)3.9H2O
Đúng 2
Bình luận (0)
): Hòa tan hoàn toàn m gam sắt (III) oxit bằng dd H2SO4 loãng 19,6 % (vừa đủ). Sau khi phản ứng kết thúc, thu được dd muối X. Cho toàn bộ lượng X tác dụng hết với dd BaCl2 dư thì thu được 34,95 gam kết tủa. Tính m và khối lượng dd H2SO4
Đọc tiếp
): Hòa tan hoàn toàn m gam sắt (III) oxit bằng dd H2SO4 loãng 19,6 % (vừa đủ). Sau khi phản ứng kết thúc, thu được dd muối X. Cho toàn bộ lượng X tác dụng hết với dd BaCl2 dư thì thu được 34,95 gam kết tủa. Tính m và khối lượng dd H2SO4