Có 2 lọ đựng dd HCl . Lọ thứ 1 có nồng độ 1 mol/l . Lọ thứ 2 có nồng độ 3 m/l . Hãy pha chế thành 50 ml dd HCl có nồng độ 2 M từ dd trên

Những câu hỏi liên quan
Bài 4 : Có 2 lọ đựng dd HCl . Lọ thứ nhất có nộng độ 1M , lọ thứ hai có nồng độ 3M .
Hãy pha thành 50 ml dd HCl có nồng độ 2M từ 2 dd trên.
Gọi số ml dd HCl ở lọ 1 và 2 lần lượt là:a;b(ml)
V của dd HCl 1M là:a
V của dd HCl 3M là:3b
Ta có: \(C_m=\dfrac{a+3b}{a+b}=2\left(a+b=50\right)\)
\(\Leftrightarrow a+3b=100\)
\(\Leftrightarrow2b=50\Leftrightarrow b=25\)
\(\Rightarrow a=25\)
Vậy để pha chế 50 ml dd HCl 2M thì ta cần đổ 25ml dd HCl 1M và 25ml dd HCl 3M
Đúng 0
Bình luận (0)
Có 2 lọ đựng dung dịch
H
2
S
O
4
. Lọ thứ nhất có nồng độ 1mol/l, lọ thứ hai có nồng độ 3 mol/l. Hãy tính toán và trình bày cách pha chế 50ml dung dịch
H
2
S
O
4
có nồng độ 1,5mol/l từ 2 dung dịch axit đã cho.
Đọc tiếp
Có 2 lọ đựng dung dịch H 2 S O 4 . Lọ thứ nhất có nồng độ 1mol/l, lọ thứ hai có nồng độ 3 mol/l. Hãy tính toán và trình bày cách pha chế 50ml dung dịch H 2 S O 4 có nồng độ 1,5mol/l từ 2 dung dịch axit đã cho.
Pha chế 50ml dung dịch H 2 S O 4 1,5M.
- Số mol H 2 S O 4 cần pha chế 50ml dung dịch H 2 S O 4 1,5M:
n H 2 S O 4 = CM.V = 1,5.0,05 = 0,075 (mol)
Gọi x(ml) là thể tích của dung dịch H 2 S O 4 1M (1)
Gọi y(ml) là thể tích của dung dịch H 2 S O 4 3M (2)
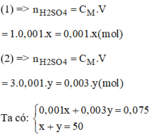
Giải hệ phương trình ta có: x = 37,5ml; y = 12,5ml
- Cách pha chế:
+ Đong lấy 37,5ml dung dịch H 2 S O 4 1M và 12,5ml dung dịch H 2 S O 4 3M cho vào bình, lắc đều, ta được 50ml dung dịch H 2 S O 4 1,5M.
Đúng 0
Bình luận (0)
Trong phòng thí nghiệm, một bạn học sinh đổ một lọ đựng 150 ml dd HCl 10% có D=1,047g/ml vào 1 lọ khác đựng 250 ml dd HCl 2M.Lắc nhẹ đều tay.Theo em, dd mới thu đc có nồng độ mol là bao nhiêu
Giải:
Số mol của dd HCl 10% là:
nHCl(1) = (C%.mdd)/(100.M) = (10.150.1,047)/(100.36,5) ≃ 0,43 (mol)
Số mol của dd HCl 2M là:
nHCl(2) = CM.V = 2.0,25 = 0,5 (mol)
Nồng độ mol của dd HCl thu được là:
CMHCl(3) = n/V = (0,43 + 0,5)/(0,15 + 0,25) = 2,325 (M)
Vậy ...
Đúng 0
Bình luận (1)
số mol của dd HCL 10% là:
nHCL=(C%.mdd)/(100.M)=(10.150.1.0,47)/(100.36,5)~0,43 (mol)
số mol của dd HCL 2M là:
nHCl=\(_{C_M}\).V=2.0,25=0,5(mol)
nồng đọ mol của dd HCL thu đc là:
\(C_m\)HCL=n/V=(0,43+0,5)/(0,15+0,25)=2,3(M)
vậy dung dịch mới thu được có nồng độ mol là 2,3M
Đúng 0
Bình luận (2)
trong phòng thí nghiệm có một lọ đựng 150ml dung dịch HCL 10% có khối lượng riêng là 10,47g/ml và lọ khác đựng 250ml dung dịch HCL 2M trộn 2 dung dịch axit vào với nhau ta được dung dịch HCl (dd A) tính nồng độ mol/lít
HCl 1 : Vdd(1) = mdd/D => mdd= Vdd. D
=> mHCl = (mdd . C%)/100 => số mol HCl
HCl 2 : số mol HCl 2 = CM. Vdd(2)
=> số mol tổng , Vtổng =Vdd1 + Vdd2
=> CM
bài này bạn xem lại dữ liệu khối lượng riêng nhé
Đúng 0
Bình luận (1)
Trong phòng thí nghiệm, 1 bạn học sinh đổ 1 lọ đựng 150 ml HCl 10% có D1,047g/ml vào một lọ khavs đựng 250ml dung dịch HCl 2M.Trộn 2 dd này với nhau sau cùng thu được một dd mới là dd A. Biết 40 ml dd A tác dụng vừa đủ với 2,7 g hỗn hợp 2 kim loại Zn và Fe.a)Tính nồng độ mol của dung dịch mới thu đượcbXác định thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp
Đọc tiếp
Trong phòng thí nghiệm, 1 bạn học sinh đổ 1 lọ đựng 150 ml HCl 10% có D=1,047g/ml vào một lọ khavs đựng 250ml dung dịch HCl 2M.Trộn 2 dd này với nhau sau cùng thu được một dd mới là dd A. Biết 40 ml dd A tác dụng vừa đủ với 2,7 g hỗn hợp 2 kim loại Zn và Fe.
a)Tính nồng độ mol của dung dịch mới thu được
bXác định thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp
Trộn 250 ml dd hỗn hợp HCl 0,08 mol/l và H2SO4 0,01 mol/l với 250 ml dd Ba(OH)2 có nồng độ x mol/l thu được m gam kết tủa và 500 ml dd có pH 12. Hãy tính m và x. A. 0,06M và 5,825 gam B. 0,01 M và 4,66 gam C. 0,06M và 0,5825 gam D. 0,0125M và 3,495 gam
Đọc tiếp
Trộn 250 ml dd hỗn hợp HCl 0,08 mol/l và H2SO4 0,01 mol/l với 250 ml dd Ba(OH)2 có nồng độ x mol/l thu được m gam kết tủa và 500 ml dd có pH = 12. Hãy tính m và x.
A. 0,06M và 5,825 gam
B. 0,01 M và 4,66 gam
C. 0,06M và 0,5825 gam
D. 0,0125M và 3,495 gam
Đáp án C
nBa(OH)2 = 0,25 x mol; nOH-= 0,5x mol
nH+ = 0,025 mol, nSO4(2-) = 0,0025 mol
H++ OH- → H2O
0,025 0,025 mol
Dung dịch sau phản ứng có pH = 12 nên OH- dư
nOH- dư = 0,5x- 0,025
[OH-] dư = nOH- dư/ Vdd = (0,5x- 0,025)/0,5 =10-2 suy ra a = 0,06 M
Ba2++ SO42- → BaSO4
0,015 0,0025 0,0025 mol
mBaSO4 = 0,5825 gam
Đúng 0
Bình luận (0)
1, dd HCl 37%, D=1,19g/ml. Nồng độ mol của dd là bn?
2, Nồng độ % của dd HCl 10,81M, D= 1,17g/ml là?
1.\(C_M=\dfrac{10.D.C\%}{M}=\dfrac{10.1,19.37}{36,5}\approx12,063M\)
2.\(C\%=\dfrac{C_M.M}{10.D}=\dfrac{10,81.36,5}{10.1,17}\approx33,724\%\)
Đúng 0
Bình luận (0)
Bài 1: Coi dd HCl đó chứa \(m=1,19g;V=1ml=0,001l\) (Phù hợp với D)
Theo bài ra ta có:
\(m_{HCl}=1,19.37\%=0,4403\left(g\right)\\ \Rightarrow n_{HCl}=\dfrac{0,4403}{36,5}=\dfrac{4403}{365000}\left(mol\right)\)
Do đó \(C_{M_{\text{dd}HCl}}=\dfrac{\dfrac{4403}{365000}}{0,001}\approx12,063M\)
Bài 2:
Coi dd HCl đó có
\(m=1,17g;V=1ml=0,001l\)
Theo gt ta có:
\(n_{HCl}=10,81.0,001=0,01081\left(mol\right)\\ \Rightarrow m_{HCl}=0,01081.36,5=0,394565\left(g\right)\)
Do đó \(\%C_{HCl}=\dfrac{0,394565.100\%}{1,17}\approx33,724\%4\%\)
Đúng 0
Bình luận (10)
a) dd axit HCl nồng độ 37% có D=1,19g/ml .tính nồng độ mol của dd
b) xác định nồng độ % của dd HCl 10,81 M có D =1,17g/mla) GS có x mol HCl
\(\Rightarrow m_{HCl}\)mHClHCl=36,5x
\(\Rightarrow m_{dd_{HCl}}\)=36,5x/37%=98,65x
\(\Rightarrow V_{dd}=\frac{m_{dd}}{D}\)=\(\frac{98,65x}{1,19}\)=82,9x (ml)
\(\Rightarrow CM_{dd_{HCl}}\)=x/0,0829x=12M
b) GS có x mol HCl
\(\Rightarrow m_{HCl}\)=36,5x
\(V_{dd_{HCl}}\)=x/10,81 lít
\(\Rightarrow m_{dd_{HCl}}\)=1/10,81.1000.1,17.x=108,233x
\(\Rightarrow\)C%=36,5/108,233.100%=33,72%
Đúng 0
Bình luận (0)
GS có x mol HClHCl
=>mHClHCl=36,5x
=>mdd HClHCl=36,5x/37%=98,65x
=>Vdd=mdd/D=98,65x/1,19=82,9x (ml)
=>CM dd HClHCl=x/0,0829x=12M
b) GS có x mol HClHCl
=>mHClHCl=36,5x
Vdd HClHCl=x/10,81 lít
=>mdd HClHCl=1/10,81.1000.1,17.x=108,233x
=>C%=36,5/108,233.100%=33,72%
Đúng 0
Bình luận (0)
1.Có 2 dd HCl và H2SO4 đựng trong các lọ riêng biệt .Hãy phân biệt.2) Có 3 dd HCl ; H2SO4 và HNO3 đựng trong các lọ riêng biệt .Hãy phân biệt.3) Có 4 dd HCl ; H2SO4 ; HNO3 và Na2SO4 đựng trong các lọ riêng biệt .Hãy phân biệt.4) Có 4 dd HCl ; H2SO4 ; NaOH và Na2SO4 đựng trong các lọ riêng biệt .Hãy phân biệt.
Đọc tiếp
1.Có 2 dd HCl và H2SO4 đựng trong các lọ riêng biệt .Hãy phân biệt.
2) Có 3 dd HCl ; H2SO4 và HNO3 đựng trong các lọ riêng biệt .Hãy phân biệt.
3) Có 4 dd HCl ; H2SO4 ; HNO3 và Na2SO4 đựng trong các lọ riêng biệt .Hãy phân biệt.
4) Có 4 dd HCl ; H2SO4 ; NaOH và Na2SO4 đựng trong các lọ riêng biệt .Hãy phân biệt.
2) Trích mẫu thử :
Cho dung dịch BaCl2 vào 3 mẫu thử :
+ Chất nào xuất hiện kết tủa trắng không tan trong axit : H2SO4
Pt : \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
Không hiện tượng : HCl , HNO3
Cho dung dịch AgNO3 vào 2 mẫu thử còn :
+ Chất nào xuất hiện kết tủa trắng : HCl
Pt : \(AgNO_3+HCl\rightarrow AgCl+HNO_3\)
Còn lại : HNO3
Chúc bạn học tốt
Đúng 1
Bình luận (0)
4) Trích mẫu thử :
Cho quỳ tím vào từng mẫu thử :
+ Hóa đỏ : HCl , H2SO4
+ Hóa xanh : NaOH
+ Không đổi màu : Na2SO4
Cho dung dịch BaCl2 vào 2 mẫu thử làm quỳ tím hóa đỏ :
+ Chất nào xuất hiện kết tủa trắng không tan trong axit : H2SO4
Pt : \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
Không hiện tượng : HCl
Chúc bạn học tốt
Đúng 1
Bình luận (0)
1) Trích mẫu thử :
Cho dung dịch BaCl2 vào từng mẫu thử :
+ Chất nào xuất hiện kết tủa trắng không atn trong axit : H2SO4
Pt : \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
Không hiện tượng : HCl
Chúc bạn học tốt
Đúng 0
Bình luận (0)





















